 На протяжении нескольких лет Европейское общество гипертензии (ESH) и Европейское общество кардиологов (ESC) ориентировались на рекомендации, выпущенные ВОЗ и Международным обществом гипертензии (ISH), несколько адаптируя их с учетом ситуации в Европе. В 2003 г было принято решение о публикации собственных рекомендаций ESH/ESC, так как руководства ВОЗ/ISH предназначаются для стран, значительно различающихся организацией медицинской помощи и экономическим положением, и содержат некоторые диагностические и лечебные рекомендации, которые могут оказаться недостаточно адекватными для европейских стран. В Европе система здравоохранения обеспечивает возможность более тщательной оценки сердечно-сосудистого риска и поражения органов-мишеней у больных артериальной гипертензией, а также использования более широкого круга антигипертензивных средств.
На протяжении нескольких лет Европейское общество гипертензии (ESH) и Европейское общество кардиологов (ESC) ориентировались на рекомендации, выпущенные ВОЗ и Международным обществом гипертензии (ISH), несколько адаптируя их с учетом ситуации в Европе. В 2003 г было принято решение о публикации собственных рекомендаций ESH/ESC, так как руководства ВОЗ/ISH предназначаются для стран, значительно различающихся организацией медицинской помощи и экономическим положением, и содержат некоторые диагностические и лечебные рекомендации, которые могут оказаться недостаточно адекватными для европейских стран. В Европе система здравоохранения обеспечивает возможность более тщательной оценки сердечно-сосудистого риска и поражения органов-мишеней у больных артериальной гипертензией, а также использования более широкого круга антигипертензивных средств.
Эта устаревшая редакция документа. См. Рекомендации по лечению артериальной гипертензии (ESH/ ESC) 2013
Содержание:
2. Определение и классификация гипертензии
2.1. Систолическое в сравнении с диастолическим и пульсовым АД
2.2. Классификация гипертензии
2.3. Общий сердечно-сосудистый риск
2.3.2. Оценка
2.3.3. Ограничения
3. Диагностическое обследование
3.1.2. Амбулаторное мониторирование АД
3.1.3. Домашнее АД
3.1.4. Изолированная офисная гипертензия или «гипертензия белого халата»
3.1.5. Изолированная амбулаторная или маскированная гипертензия
3.1.6. АД во время нагрузки и лабораторного стресса
3.1.7. Центральное АД
3.3. Физикальное обследование
3.4. Лабораторные исследования
3.5. Генетический анализ
3.6. Выявление признаков повреждения органов-мишеней
3.6.2. Сосуды
3.6.3. Почки
3.6.4. Исследование глазного дна
3.6.5. Головной мозг
4. Необходимость лечения артериальной гипертензии
4.2. Плацебоконтролируемые исследования
4.3. Сравнение более и менее агрессивной антигипертензивной терапии
4.4. Сравнение препаратов разных классов в исследованиях с твердыми конечными точками
4.4.2. Ингибиторы АПФ по сравнению с тиазидными диуретиками и бета-блокаторами
4.4.3. Ингибиторы АПФ по сравнению с антагонистами кальция
4.4.4. Антагонисты ангиотензиновых рецепторов по сравнению с другими препаратами
4.4.5. Исследования бета-блокаторов
4.4.6. Заключение
4.5.2. Стенка артерий и атеросклероз
4.5.3. Головной мозг и когнитивная функция
4.5.4. Функция и поражение почек
4.5.5. Развитие сахарного диабета
5. Подходы к лечению артериальной гипертензии
5.2. Цели лечения
5.2.2. Целевые значения АД у больных сахарным диабетом и пациентов очень высокого и высокого риска
5.2.3. Целевые значения домашнего и амбулаторного АД
5.2.4. Заключение
6.1.2. Умеренное употребление алкоголя
6.1.3. Ограничение потребления соли
6.1.4. Другие изменения диеты
6.1.5. Снижение массы тела
6.1.6. Физические нагрузки
6.2.2. Монотерапия
6.2.3. Комбинированная терапия
7. Подходы к лечению в особых ситуациях
7.2. Сахарный диабет
7.3. Цереброваскулярная болезнь
7.3.2. Когнитивная дисфункция и деменция
7.5. Фибрилляция предсердий
7.6. Недиабетическая нефропатия
7.7. Артериальная гипертензия у женщин
7.7.2. Гормонозаместительная терапия
7.7.3. Артериальная гипертензия у беременных
7.9. Резистентная гипертензия
7.10. Неотложные ситуации
7.11. Злокачественная гипертензия
8. Лечение сопутствующих факторов риска
8.2. Антитромбоцитарная терапия
8.3. Контроль гликемии
9. Скрининг и лечение вторичной гипертензии
9.2. Реноваскулярная гипертензия
9.3. Феохромоцитома
9.4. Первичный альдостеронизм
9.5. Синдром Кушинга
9.6. Обструктивное апноэ во сне
9.7. Коарктация аорты
9.8. Лекарственная гипертензия
1. Введение и цели
На протяжении нескольких лет Европейское общество гипертензии (ESH) и Европейское общество кардиологов (ESC) ориентировались на рекомендации, выпущенные ВОЗ и Международным обществом гипертензии (ISH), несколько адаптируя их с учетом ситуации в Европе. В 2003 г было принято решение о публикации собственных рекомендаций ESH/ESC, так как руководства ВОЗ/ISH предназначаются для стран, значительно различающихся организацией медицинской помощи и экономическим положением, и содержат некоторые диагностические и лечебные рекомендации, которые могут оказаться недостаточно адекватными для европейских стран. В Европе система здравоохранения обеспечивает возможность более тщательной оценки сердечно-сосудистого риска и поражения органов-мишеней у больных артериальной гипертензией, а также использования более широкого круга антигипертензивных средств.
Рекомендации ESH/ESC 2003 г были положительно встречены медицинским сообществом и широко цитировались в медицинской литературе последних лет. Однако с 2003 г подходы к диагностике и лечению артериальной гипертензии изменились, что послужило основанием для пересмотра указанных рекомендаций. При подготовке новых рекомендаций комитет, созданный ESH и ESC, решил следовать принципам разработки рекомендаций 2003 г:
- 1) подготовка оптимальных и сбалансированных рекомендаций для всех медицинских работников, наблюдающих больных артериальной гипертензией;
- 2) тщательный и критический анализ данных с разработкой конкретных рекомендаций по определенным вопросам (в рамках), а также публикация сокращенных рекомендаций, как это было сделано в 2003 г;
- 3) использование, в первую очередь, результатов крупных рандомизированных исследований, а также других данных, если они были получены в исследованиях, соответствующих высоким научным стандартам;
- 4) рекомендации освещают проблему в целом, в то время как лечение конкретных больных может значительно отличаться в зависимости от различных факторов (особенности личности, медицинский анамнез, культурологические факторы) и должно подбираться индивидуально;
- 5) отсутствие жесткой классификации рекомендаций по уровню или убедительности научных доказательств. По мнению комитета, использование подобной классификации часто затруднительно и касается, прежде всего, лечебных аспектов. Тем не менее, в тексте рекомендаций содержатся сведения о значении результатов рандомизированных и нерандомизированных исследований, мета-анализов и мнений экспертов.
Члены комитета, созданного ESH и ESC, принимали участие в подготовке настоящего документа, используя свой собственный научный и клинический опыт и критическую оценку всей доступной литературы. Большинство из них сотрудничает с фармацевтическими компаниями или государственными и частными лечебными организациями (научные исследования, конференции, консультации), однако все эксперты полагают, что это не отразилось на их суждениях. Лучшей гарантией независимости является качество их предыдущей и настоящей научной работы. Однако на сайтах ESH и ESC (www.eshonline.org и www.escardio.org) содержится информация о связях экспертов с фармацевтическими компаниями и государственными и частными организациями. Все затраты на подготовку рекомендаций были покрыты ESH и ESC.
2. Определение и классификация гипертензии
Издавна диастолическое АД считалось более важным фактором риска сердечно-сосудистой заболеваемости и смертности, чем систолическое АД. Это нашло отражение в первых рекомендациях JNC (Национального объединенного комитета США), в которых в классификацию артериальной гипертензии не были включены систолическое АД и изолированная систолическая гипертензия. В рандомизированные клинические исследования больных также практически всегда отбирали на основании значений диастолического АД. Однако в крупных эпидемиологических исследованиях было показано, что сердечно-сосудистая заболеваемость и смертность линейно связаны как с систолическим, так и диастолическим АД. Степень повышения риска инсульта превосходила таковую коронарных исходов; поэтому нарушения мозгового кровообращения считали наиболее важными осложнениями артериальной гипертензии. Однако в некоторых регионах Европы (хотя и не во всех) атрибутивный риск (т.е. дополнительная смертность, связанная с повышенным АД) коронарных осложнений превышает атрибутивный риск инсульта, так как в этих странах ИБС остается самым распространенным сердечно-сосудистым заболеванием. Кроме того, систолическое и диастолическое АД являются независимыми факторами риска развития сердечной недостаточности, поражения периферических артерий и терминальной нефропатии. Следовательно, артериальную гипертензию целесообразно считать основным фактором риска сердечно-сосудистых и родственных заболеваний. Этот факт, а также широкая распространенность повышенного АД в общей популяции объясняют, почему в отчете ВОЗ высокое АД было названо главной причиной общей смертности.
2.1. Систолическое в сравнении с диастолическим и пульсовым АД
В последние годы установлено, что у пожилых людей сердечно-сосудистый риск прямо пропорционален систолическому АД, а при любом значении систолического АД вероятность неблагоприятного исхода обратно пропорциональна диастолическому АД. Важная роль принадлежит также пульсовому АД (разнице систолического и диастолического АД). Прогностическое значение последнего показателя зависит от клинических особенностей пациентов. По данным самого крупного мета-анализа эпидемиологических исследований (61 исследование, почти 1 млн пациентов без явных сердечно-сосудистых заболеваний; 70%из них проживают в Европе), систолическое и диастолическое АД являются независимыми факторами риска инсульта и коронарной смертности; при этом вклад пульсового АД оказался небольшим, особенно у людей в возрасте до 55 лет. Напротив, у людей среднего и пожилого возраста с артериальной гипертензией, сочетавшейся с другими сердечно-сосудистыми факторами риска или ассоциированными клиническими состояниями, пульсовое АД было самым мощным фактором риска сердечно-сосудистых исходов.
Следует учитывать, что пульсовое АД является производным показателем, отражающим несовершенство первичных измерений. Верхними его границами предложено считать 50 или 55 мм рт. ст, хотя практические критерии оценки повышенного пульсового АД у пациентов разного возраста отсутствуют. Как указано в разделе 3.1.7, центральное пульсовое АД, которое (учитывая «феномен усиления» между периферическими артериями и аортой) является более точным показателем.
На практике артериальную гипертензию и риск (см. разделы 2.2 и 2.3) следует по-прежнему классифицировать на основании значений систолического и диастолического АД. В первую очередь, это касается порогового АД и целей лечения, так как указанные критерии использовались в рандомизированных контролируемых исследованиях у больных изолированной систолической и систоло-диастолической гипертензией. Однако пульсовое АД может быть использовано для идентификации пожилых пациентов с систолической гипертензией, относящихся к группе высокого риска. В таких случаях высокое пульсовое АД служит маркером повышенной жесткости крупных артерий и более тяжелого поражения органов-мишеней (см. раздел 3.6).
2.2 Классификация гипертензии
Распределение АД в популяции является унимодальным . Связь между сердечно-сосудистым риском и систолическим или диастолическим АД сохраняется при уровнях 115-110 и 75-70 мм рт. ст., соответственно. В связи с этим, с научной точки зрения, понятие «артериальная гипертензия» является спорным, а критерии его классификации – субъективными. Однако изменение общепринятой терминологии может привести к путанице, а использование существующих критериев облегчает диагностику и лечение. В связи с этим классификация артериальной гипертензии, предложенная в рекомендациях ESH/ESC 2003 г., была оставлена без изменений (табл. 1).
Таблица 1. Классификация значений АД (мм рт. ст.)
| Категория | Систолическое | Диастолическое | |
|---|---|---|---|
| Оптимальное | <120 | и | <80 |
| Нормальное | 120-129 | и/или | 80-84 |
| Высокое нормальное | 130-139 | и/или | 85-89 |
| Гипертензия 1 степени 140-159 | 140-159 | и/или | 90-99 |
| Гипертензия 2 степени | 160-179 | и/или | 100-109 |
| Гипертензия 3 степени | ≥180 | и/или | ≥110 |
| Изолированная систолическая гипертензия | ≥140 | и | <90 |
| Изолированную систолическую гипертензию следует классифицировать (степени 1, 2 и 3) на основании критериев диагностики систоло-диастолической гипертензии (используются значения систолического АД) при условии, что диастолическое АД <90 мм рт.ст. Артериальная гипертензия 1, 2 и 3 степени соответствует легкой, умеренной и тяжелой гипертензии. Однако последние термины использовать не следует, чтобы не путать с общим сердечно-сосудистым риском. | |||
Однако необходимо учитывать следующее:
- 1. Если значения систолического и диастолического АД находятся в разных категориях, то для количественной оценки общего сердечно-сосудистого риска, выбора лечения и анализа его эффективности следует использовать более высокое значение.
- 2. Изолированную систолическую гипертензию следует классифицировать (степени 1, 2 и 3) на основании критериев диагностики систоло-диастолической гипертензии (используются значения систолического АД). Как указано выше, низкие значения диастолического АД (например, 60-70 мм рт. ст.) рассматривают как дополнительный фактор риска.
- 3. Решение о необходимости антигипертензивной терапии следует принимать с учетом уровня и профиля общего сердечно-сосудистого риска. Например, высокое АД может быть основанием для лечения у пациентов группы высокого риска, в то время как в группе низкого риска лечение может не потребоваться. Данные, обосновывающие это положение, приведены в разделе 5.
В американских рекомендациях по артериальной гипертензии (JNC 7), опубликованных в 2003 г, нормальное и высокое нормальное АД были объединены термином «предгипертония», так как во фрамингемском исследовании было показано, что у таких пациентов вероятность развития артериальной гипертензии выше, чем у людей любого возраста с АД менее 120/80 мм рт. ст. (оптимальное нормальное АД).
Комитет ESH/ESC принял решение не пользоваться этой терминологией по следующим причинам:
- 1) даже во фремингемском исследовании риск развития артериальной гипертензии у пациентов с высоким нормальным АД (130-139/89 мм рт. ст.) был выше, чем у людей с нормальным АД (120-129/84 мм рт. ст.); поэтому объединение этих групп необоснованно;
- 2) термин «предгипертония» может послужить источником тревоги у пациентов и причиной необоснованных визитов к врачу и диагностических исследований
- 3) хотя в рекомендациях JNC 7 2003 г. модификация образа жизни была рекомендована всем пациентам с предгипертонией, на практике эта группа очень неоднородна. Если части пациентов какое-либо вмешательство не требуется (например, пожилой человек с АД 120/80 мм рт. ст.), то пациентам группы очень высокого или высокого риска (например, после инсульта или при наличии сахарного диабета), наоборот, показана фармакотерапия.
2.3. Общий сердечно-сосудистый риск
| Рамка 1. Общий сердечно-сосудистый риск |
|---|
|
2.3.1. Концепция
На протяжении долгого времени единственным или основным критерием при оценке необходимости в антигипертензивной терапии и выборе ее схемы служили значения АД. Хотя этот подход сохранился в отчете JNC 7, в рекомендациях ESH/ESC 2003 г. было указано, что при диагностике и лечении артериальной гипертензии следует учитывать общий сердечно-сосудистый риск. Это связано с тем, что только у небольшой части больных артериальной гипертензией отмечается изолированное повышение АД, в то время как у подавляющего большинства пациентов имеются дополнительные сердечно-сосудистые факторы риска. Установлена связь между тяжестью артериальной гипертензии и нарушениями обмена глюкозы и липидов. Артериальная гипертензия и метаболические факторы риска усиливают действие друг друга, поэтому общий сердечно-сосудистый риск превышает простую сумму отдельных факторов риска. Наконец, имеются данные о том, что у пациентов группы высокого риска пороговые значения АД, при которых следует начинать лечение, и целевые показатели должны быть ниже, чем у пациентов группы более низкого риска. Чтобы обеспечить максимальную эффективность затрат на лечение артериальной гипертензии, интенсивность антигипертензивной терапии должна быть пропорциональной общему сердечно-сосудистому риску.
2.3.2. Оценка
Оценка общего сердечно-сосудистого риска представляет собой простую задачу у пациентов с:
- 1) установленным диагнозом сердечно-сосудистого заболевания;
- 2) сахарным диабетом 2-го типа;
- 3) сахарным диабетом 1-го типа;
- 4) высоким уровнем отдельного фактора риска.
Во всех указанных случаях общий сердечно-сосудистый риск высокий, что является основанием для интенсивной борьбы с факторами риска (см. ниже). Однако большое число пациентов с артериальной гипертензией не принадлежит к указанным категориям, и для идентификации высокого риска и выбора стратегии лечения необходимо использование спе-циальных моделей.
Разработан ряд компьютерных методов расчета общего сердечно-сосудистого риска, т.е. абсолютного риска развития сердечно-сосудистого исхода в течение 10 лет.Однако некоторые модели основываются на результатах фрамингемского исследования, которые распространяются только на отдельные европейские популяции (учитывая значительные отличия заболеваемости коронарной болезнью сердца и инсультом). Недавно была разработана европейская модель, базирующаяся на крупной базе данных в рамках программы SCORE. Существуют таблицы SCORE, которые могут быть использованы в странах Европы с высокой и низкой сердечно-сосудистой заболеваемостью. Они позволяют оценить риск смерти от сердечно-сосудистых болезней (не только от ИБС) в течение 10 лет и откалибровать таблицу для конкретных стран, если имеются статистические данные о смертности и распространенности основных сердечно-сосудистых факторов риска.Модель SCORE была также использована для разработки Heart-Score, который рекомендован ESC для применения в рамках программ профилактики сердечно-сосудистых заболеваний (www.escardio.org).
В рекомендациях ESH/ESC 2003 г. общий сердечно-сосудистый риск классифицируется на основании рекомендаций ВОЗ/ISH , включая пациентов с «нормальным» или «высоким нормальным» АД. Эта классификация оставлена в настоящих рекомендациях (рис. 1). 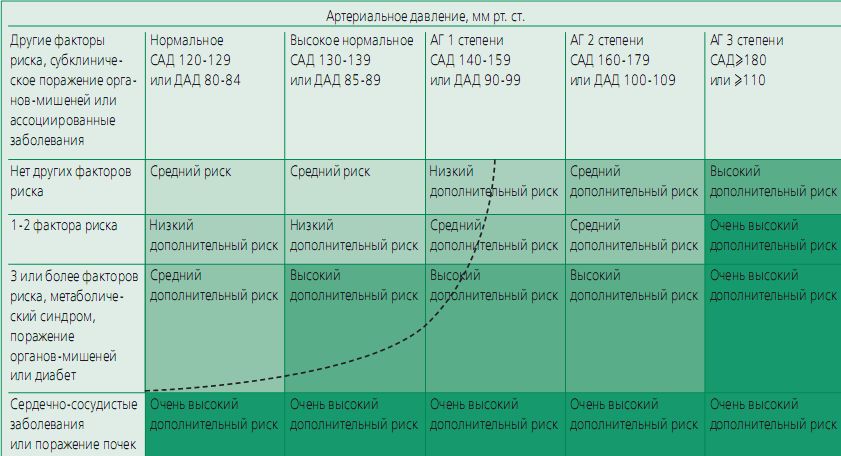
САД – систолическое АД, ДАД – диастолическое АД, АГ – артериальная гипертензия. Категории риска отражают риск развития фатальных и нефатальных сердечно-сосудистых исходов в течение 10 лет. Термин «дополнительный» указывает на то, что риск в каждой категории выше среднего. Пунктирная линия – вариабельность определения АГ в зависимости от общего сердечно-сосудистого риска.
Термины «низкий», «средний», «высокий» и «очень высокий» риск отражают примерный риск сердечно-сосудистой заболеваемости и смертности в течение ближайших 10 лет аналогично увеличению сердечно-сосудистого риска, который оценивают на основании данных фрамингемского исследования или модели SCORE. Термин «дополнительный», или «добавленный», свидетельствует о том, что во всех категориях относительный риск повышен по сравнению со средним. Хотя выделение категорий риска не позволяет дать такую же точную оценку риска, как использование специальных уравнений и количественных показателей, тем не менее, достоинством такого подхода является простота. В рекомендациях ВОЗ/ISH 2003 г. этот подход был дополнительно упрощен за счет объединения категорий высокого и очень высокого риска, которые считались сходными при решении вопроса о лечении. В настоящих рекомендациях были выделены категории высокого и очень высокого риска, т.е. закреплена отдельная роль вторичной профилактики у больных сердечно-сосудистыми заболеваниями. В таких случаях не только значительно выше общий сердечно-сосудистый риск, но и нередко требуется комбинированная фармакотерапия при любых значениях АД – от нормальных до высоких. Пунктирная линия на рис. 1 иллюстрирует, как общий сердечно-сосудистый риск влияет на критерии диагностики артериальной гипертензии, которыми можно считать значения АД, когда лечение приносит больше пользы, чем вреда.
В табл. 2 перечислены основные клинические параметры, которые следует использовать для стратификации риска. Они включают факторы риска (демографические, антропометрические, семейный анамнез ранних сердечно-сосудистых заболеваний, АД, курение, уровни глюкозы и липидов), поражение органов-мишеней и наличие сахарного диабета и ассоциированных клинических состояний, выделенных в рекомендациях 2003 г.
| Факторы риска | Бессимптомное поражение органов-мишеней |
|---|---|
- ХС >5,0 ммоль/л (190 мг%) или
- ХС ЛПНП >3,0 ммоль/л (115 мг%) или - ХС ЛПВП < 1,0 ммоль/л (40 мг%) у мужчин и < 1,2 ммоль/л (46 мг%) у женщин или - ТГ > 1,7 ммоль/л (150 мг%)
|
|
| Сахарный диабет | Сердечно-сосудистые заболевания или нефропатия |
|
|
| Сочетание 3-х из следующих 5-ти критериев свидетельствует о наличии метаболического синдрома: абдоминальное ожирение, изменения гликемии натощак, АД более 130/85 мм рт. ст., низкий холестерин ЛПВП и высокие ТГ (см. выше) | |
| *максимальный риск при концентрической ГЛЖ: повышение индекса массы миокарда левого желудочка и отношение толщины стенки и радиуса > 0,42. **формулаMDRD . *** формула Кокрофта-Голта, ХС – холестерин, ТГ – триглицериды, ГЛЖ – гипертрофия левого желудочка | |
Необходимо обратить внимание на следующие моменты:
1. Метаболический синдром представляет собой комбинацию факторов, которые часто сочетаются с высоким АД и значительно повышают сердечно-сосудистый риск. Это не означает, что он является самостоятельной нозологической формой.
2. Дополнительно подчеркивается важность выявления поражения органов-мишеней, так как их бессимптомные изменения указывают на прогрессирование сдвигов в рамках сердечно-сосудистого континуума и значительное увеличение риска по сравнению с таковым при наличии только факторов риска. В разделе 3.6 специально обсуждаются методы диагностики бессимптомного поражения органов-мишеней.
3. Перечень маркеров поражения почек расширен и включает в себя клиренс креатинина, который рассчитывают по формуле Кокрофта-Голта, или скорость клубочковой фильтрации, рассчитываемуюпоформуле MDRD, так как эти показатели позволяют точнее оценить сердечно-сосудистый риск, связанный с дисфункцией почек.
4. Микроальбуминурию в настоящее время считают необходимым компонентом оценки поражения органов-мишеней, учитывая простоту и относительную дешевизну метода ее определения.
5. Концентрическая гипертрофия левого желудочка – структурный параметр, вызывающий более значительное увеличение сердечно-сосудистого риска.
6. По возможности, рекомендуется оценивать повреждение различных тканей (сердца, сосудов, почек и головного мозга), так как мультиорганные изменения ассоциируются с более неблагоприятным прогнозом.
7. К числу факторов риска отнесено увеличение скорости пульсовой волны, являющееся ранним признаком повышения жесткости крупных артерий, хотя этот метод мало доступен в клинической практике.
8. Низкий лодыжечно-плечевой индекс (< 0,9) – достаточно простой показатель атеросклероза и повышенного общего сердечно-сосудистого риска.
9. Поражение органов-мишеней рекомендуется оценивать не только до (с целью стратификации риска), но и во время лечения, так как регресс гипертрофии левого желудочка и уменьшение протеинурии отражают протективное действие на сердечно-сосудистую систему.
10. Имеются основания для включения повышенной частоты сердечных сокращений (ЧСС) в список факторов риска, так как это ассоциируется с риском сердечно-сосудистой заболеваемости и смертности, а также общей смертности. Увеличение ЧСС повышает риск развития артериальной гипертензии и часто сочетается с метаболическими нарушениями и метаболическим синдромом. Однако, учитывая широкий диапазон нормальных значений ЧСС в покое (60-90/мин), в настоящее время невозможно выделить показатели, которые могли бы повысить точность стратификации общего сердечно-сосудистого риска.
11. В табл. 3 приведены основные критерии выделения групп высокого и очень высокого риска. Следует отметить, что наличие множественных факторов риска, сахарного диабета или поражения органов-мишеней однозначно указывает на высокий риск, даже при высоком нормальном АД.
| Систолическое АД ≥ 180 мм рт. ст. и/или диастолическое АД ≥ 110 мм рт. ст. |
| Систолическое АД > 160 мм рт. ст. в сочетании с низким диастолическим АД (< 70 мм рт. ст.) |
| Сахарный диабет |
| Метаболический синдром |
| ≥ 3-х сердечно-сосудистых факторов риска |
По крайней мере, один из следующих показателей бессимптомного поражения органов-мишеней:
|
| Сердечно-сосудистые заболевания или заболевание почек |
2.3.3. Ограничения
Все современные методы оценки сердечно-сосудистого риска не учитывают длительности воздействия фактора риска и предполагают количественный анализ только некоторых факторов риска, в то время как другим показателям уделяется меньшее внимание (например, физической активности и стрессам). Кроме того, значение поражения органов-мишеней для расчета общего риска зависит от тщательности обследования. В табл. 2 не указаны некоторые дополнительные маркеры поражения органов-мишеней в связи с трудностью оценки, недостаточно доказанным прогностическим значением или практическими проблемами (низкая доступность, зависимость результатов от опыта исследователя, отсутствие стандартизации, трудоемкость, инвазивность, затраты и т.д.). Однако эти показатели в настоящее время активно изучаются и могут оказаться полезными в ближайшем будущем. Поэтому они обсуждаются в разделе 3.6 и включены в табл. 4.
| Показатели | Прогностическое значение | Доступность | Затраты |
| Электрокардиография | ++ | ++++ | + |
| Эхокардиография | +++ | +++ | ++ |
| Толщина комплекса интима-меди | +++ | +++ | ++ |
| Жесткость артерий (скорость пульсовой волны) | +++ | + | ++ |
| Лодыжечно-плечевой индекс | ++ | ++ | + |
| Содержание кальция в коронарных артериях | + | + | ++++ |
| Состав ткани сердца/сосудов | ? | + | ++ |
| Циркулирующие маркеры коллагена | ? | + | ++ |
| Эндотелиальная дисфункция | ++ | + | +++ |
| Церебральные лакуны/поражение белого вещества | ? | ++ | ++++ |
| Скорость клубочковой фильтрации или клиренс креатинина | +++ | ++++ | + |
| Микроальбуминурия | +++ | ++++ | + |
Следует отметить также концептуальные ограничения предложенных рекомендаций. Целью оценки общего риска является оптимальное использование ограниченных средств для профилактики сердечно-сосудистых заболеваний, т.е. выбор профилактических вмешательств с учетом степени повышения риска. Организаторы здравоохрания часто стратифицируют абсолютный риск, чтобы выбрать порог, ниже которого лечение не рекомендуется. Существующий порог (20%-ный риск сердечно-сосудистых заболеваний в течение 10 лет) является спорным и упрощенным; было бы неправильным рекомендовать интенсивное лечение, если риск превышает указанное значение, и отказываться от активной профилактики, если риск ниже указанного показателя. Необходимо учитывать, что общий сердечно-сосудистый риск в значительной степени зависит от возраста. У молодых взрослых людей (особенно женщин) риск редко оказывается высоким даже при наличии более одного фактора риска, однако у них четко увеличен относительный риск (по сравнению со сверстниками). Напротив, у большинства людей старше 70 лет часто отмечается высокий общий риск, хотя он повышен незначительно по сравнению с таковым у пациентов того же возраста. В связи с этим, средства затрачиваются, в основном, на пожилых людей, у которых ожидаемая продолжительность жизни ограниченна, несмотря на лечение, в то время как молодым людям с высоким относительным риском уделяется мало внимания, хотя при отсутствии лечения длительное воздействие факторов риска может привести к частично необратимым изменениям и возможному сокращению ожидаемой продолжительностижизни. Как уже указывалось в рекомендациях ESH/ESC 2003 г., этих ограничений можно избежать, если выбирать стратегию ведения молодых пациентов на основании относительного риска. Для этого может быть использован индекс HeartScore (www.escardio.org) с учетом рекомендаций по профилактике сердечно-сосудистых заболеваний в клинической практике, предложенных четвертой объединенной рабочей группой европейских обществ. Необходимо помнить, что у молодых людей, у которых абсолютный риск является низким за счет возраста, но имеются важные факторы риска, необходимо использовать немедикаментозные, а при необходимости - и медикаментозные методы лечения с целью улучшения профиля риска и профилактики неблагоприятных исходов в более зрелом возрасте. Если не проводить лечение, то они могут развиться раньше, так как факторы риска с возрастом становятся более выраженными, а стойкое повышение АД на протяжении многих лет часто сопровождается поражением органов-мишеней.
3. Диагностическое обследование
Цели обследования включают:
2) исключение причин вторичной гипертензии;
3) оценку общего сердечно-сосудистого риска на основании анализа других факторов риска, поражения органов-мишеней и сопутствующих заболеваний.
Показаны следующие исследования:
- повторное измерение АД;
- медицинский анамнез;
- физическое обследование;
- лабораторные и инструментальные исследования.
Некоторые из них показаны всем больным с высоким АД, другие широко применяются только в развитых странах Европы, третьи обоснованны только при наличии клинических показаний.
3.1. Измерение АД
АД может спонтанно меняться вшироких пределах в течение дня, недели, месяцев или лет. В связи с этим артериальную гипертензию следует диагностировать на основании результатов повторного измерения АД. Если АД повышено незначительно, то повторные измерения необходимо продолжать в течение нескольких месяцев, чтобы как можно точнее установить «обычное» АД. С другой стороны, если имеются более значительное повышение АД, поражение органов-мишеней или высокий или очень высокий сердечно-сосудистый риск, то повторные измерения АД проводят в течение нескольких недель или дней. В целом, диагноз артериальной гипертензии может быть установлен на основании двукратного измерения АД при, по крайней мере, 2-х - 3-х визитах, хотя в особенно тяжелых случаях она может быть диагностирована уже при первом визите. АД может измеряться врачом или медсестрой в кабинете или в клинике (офисное АД), пациентом или его родственниками в домашних условиях или круглосуточно с помощью монитора. Ниже приводятся рекомендации Европейского общества гипертензии по измерению АД.
3.1.1. Офисное АД
АД можно измерять с помощью ртутного сфигмоманометра, части которого (резиновые трубки, клапаны, количество ртути и т.д.) должны находиться в рабочем состоянии. Могут использоваться также другие неинвазивные приборы (аускультативные или осциллометрические полуавтоматические), роль которых будет возрастать в результате запрещения применения ртути с медицинскими целями. Однако точность показаний подобных приборов должна быть проверена с помощью стандартных протоколов (www.dableducational.org), а точность измерений следует периодически сравнивать с показателями ртутного сфигмоманометра. Инструкции по правильному измерению офисного АД суммированы в рамке 2.
| Рамка 2. Измерение АД |
|---|
|
3.1.2. Амбулаторное мониторирование АД
Существует несколько приборов (в основном, осциллометрических) для автоматической регистрации АД в условиях нормальной жизнедеятельности.Они позволяют измерить среднесуточное АД, а также средние значения АД днем, ночью и утром. Эти показатели не заменяют стандартных значений АД. Однако они имеют важное вспомогательное значение, так как в клинических исследованиях было показано, что офисное АД слабо коррелирует со среднесуточными значениями АД и показателями АД в обычной жизни. Эти исследования свидетельствуют также о том, что
(1) результаты амбулаторного мониторирования АД более тесно коррелируют с поражением органов-мишеней и их динамикой нафоне лечения, чем офисное АД;
(2) средние значения АД позволяют предсказать более высокий сердечно-сосудистый риск как в общей популяции, так и у пациентов леченой и нелеченой гипертензией;
(3) результаты такого исследования позволяют точнее оценить снижение АД под влиянием лечения, учитывая их более высокую воспроизводимость и отсутствие эффектов «белого халата» и плацебо.
| Рамка 3. Амбулаторное мониторирование АД и измерение АД в домашних условиях |
Амбулаторное мониторирование АД• Хотя в качестве стандарта следует использовать офисное АД, амбулаторное мониторирование позволяет точнее оценивать сердечно-сосудистый риск у нелеченых и леченых пациентов.• Нормальные значения офисного и амбулаторного АД отличаются (табл. 5). • Проведение суточного мониторирования АД, в первую очередь, обоснованно в следующих случаях: - значительная вариабельность офисного АД при одном или разных визитах; - высокое офисное АД у пациентов группы низкого риска; - значительное несоответствие значений АД, измеренных дома и в кабинете врача; - предполагаемая резистентность к антигипертензивной терапии; - предполагаются эпизоды гипотонии, особенно у пожилых людей и больных диабетом; - повышение офисного АД у беременных женщин и подозрение на преэклампсию. Домашнее АД• Самостоятельное измерение АД в домашних условиях имеет клиническое и прогностическое значение. Оно позволяет:- получить дополнительные сведения о снижении АД в конце интервала дозирования антигипертензивных средств; - повысить приверженность пациента лечению; - существуют сомнения по поводу технической надежности результатов амбулаторного мониторирования АД. • Самостоятельное измерение рекомендовать не следует, если оно: - вызывает тревогу у пациентов; - является основанием для самостоятельной модификации схемы лечения; • Нормальные значения офисного и домашнего АД отличаются (табл. 5). |
Хотя тех же результатов можно частично достичь путем увеличения числа офисных измерений АД, суточное мониторирование АД может быть полезным на момент установления диагноза и во время лечения. АД желательно мониториро-вать в течение 24 ч, чтобы получить представление о среднедневном и средненочном АД, степени снижения АД в ночное время, утреннем подъеме АД и вариабельности АД. Среднедневные и средненочные значения АД и их изменения во время лечения связаны друг с другом, однако по прогностическому значению ночное АД превосходит дневное. Кроме того, у пациентов, у которых отсутствует ночное снижение АД, отмечены увеличение частоты поражения органов-мишеней и ухудшение прогноза; в некоторых исследованиях прогностическое значение этого феномена утрачивалось, когда в многофакторный анализ включали среднесуточное АД. Имеются также данные о том, что риск развития сердечных и цереброваскулярных исходов достигает пика в утренние часы, возможно, за счет резкого повышения АД после пробуждения, а также увеличения агрегации тромбоцитов,снижения фибринолитической активности и активации симпатической нервной системы. Прогрессирование поражения органов-мишеней и частота нежелательных исходов коррелировали также с вариабельностью АД (стандартным отклонением от средних значений). Хотя в этих исследованиях не всегда можно было исключить роль сопутствующих факторов, независимое прогностическое значение вариабельности АД было недавно подтверждено в длительном клиническом исследовании.
При проведении суточного мониторирования необходимо выполнять следующие условия:
- применять только приборы, валидированные с помощью стандартных протоколов;
- использовать манжеты адекватного размера и сравнивать начальные значения с показаниями сфигмоманометра (разница должна быть в пределах ±5 мм рт. ст.);
- регистрировать АД не реже, чем каждые 30 минут, чтобы зафиксировать адекватное число значений и обеспечить репрезентативность, если какие-либоз начения придется исключить из-за артефактов;
- cкорость автоматического снижения давления в манжете должна быть не более 2 мм рт. ст./с;
- пациент должен вести нормальный образ жизни, но избегать чрезмерной нагрузки; во время измерения АД рука должна быть вытянута и находиться в спокойном положении;
- предложите пациенту фиксировать в дневнике свою активность, а также длительность и качество ночного сна;
- следует провести повторное мониторирование АД, если из-за артефактов придется исключить более 30% измеренных значений АД. Процент адекватных показателей должен быть сопоставимым в течение дня и ночи;
- помните, что результаты амбулаторного мониторирования АД обычно на несколько мм рт. ст. ниже офисных значений. Как видно из табл.5, в различных популяционных исследованиях было показано, что офисное АД 140/90 мм рт. ст. соответствует среднесуточному АД 125-130/80 мм рт. ст. (130-135/85 мм рт. ст. днем и 120/70 мм рт. ст. ночью). Указанные величины могут расцениваться как пороговые значения для установления диагноза артериальной гипертензии при суточном мониторировании АД;
- клиническое значениеимеют, в основном, среднесуточные, дневные и/или ночные значения АД. Другие показатели(например, утренний подъем АД или вариабельность АД) представляются перспективными, однако они пока находятся на стадии изучения.
3.1.3. Домашнее АД
Самостоятельное измерение АД в домашних условиях не позволяет получить информацию, которую дает суточное мониторирование. Однако оно дает возможность оценить значения АД в повседневной жизни. Средний показатель за несколько дней обладает рядом достоинств результатов суточного мониторирования, в том числе отсутствием «эффекта белого халата», более высокой воспроизводимостью и прогностическим значением (вероятность наличия и прогрессирования поражения органов-мишеней, а также риск сердечно-сосудистых исходов). Следовательно, до и во время лечения рекомендуется самостоятельно измерять АД, так как эта достаточно дешевая процедура способствует увеличениюприверженности больного к антигипертензивной терапии.
При измерении АД в домашних условиях следует выполнять определенные условия:
- целесообразно использовать валидированные приборы. Немногие из существующих устройств, предполагающих измерение АД на запястье, прошли адекватную валидацию; если пациент использует подобные приборы, то он должен держать руку на уровне сердца;
- предпочтительно применение полуавтоматических устройств, а не ртутных сфигмоманометров, чтобы избежать проблем, связанных с необходимостью обучения пациента технике измерения АД, а также возможных ошибок при нарушении слуха у пожилых людей;
- пациент должен производить измерения в положении сидя после непродолжительного отдыха (несколько минут), предпочительно утром и вечером. Информируйте его, что измеренные значения могут отличаться в результате спонтанной вариабельности АД;
- не следует измерять АД слишком часто. Необходимо также измерить АД до приема препарата, чтобы оценить длительность его действия;
- значения АД в домашних условиях ниже офисных показателей (130-135/85 мм рт. ст. соответствует 140/90 мм рт. ст.) (см. табл. 5);
- больной должен информировать врача о результатах измерений и избегать самостоятельной модификации схемы антигипертензивной терапии.
| Систолическое АД | Диастолическое АД | |
|---|---|---|
| Офисное или клиническое | 140 | 90 |
| Суточное | 125-130 | 80 |
| Дневное | 130-135 | 85 |
| Ночное | 120 | 70 |
| Домашнее | 130-135 | 85 |
3.1.4. Изолированная офисная гипертензия или «гипертензия белого халата»
У некоторых больных отмечается стойкое повышение офисного АД, тогда как дневное или среднесуточное АД и домашнее АД находятся в пределах нормы. Это состояние обычно называют “гипертензией белого халата”, хотя лучше называть его “изолированной офисной гипертензией”, так как оно не коррелирует с подъемом офисного АД как ответной реакцией на контакт с врачом или медсестрой, т.е. истинным “эффектом белого халата”. Частота изолированной офисной гипертензии в общей популяции может достигать примерно 15%. Это состояние наблюдается у значительной части (трети или более) пациентов с диагнозом артериальная гипертензия.
Имеются данные о том, что у пациентов с изолированной офисной гипертензией сердечно-сосудистый риск ниже, чем у больных, у которых отмечается повышение как офисного, так и среднесуточного АД. Однако в нескольких (хотя и не во всех) исследованиях было показано, что у таких пациентов поражение органов-мишеней и метаболические нарушения встречаются чаще, чем у пациентов с нормальным АД. Эти данные свидетельствуют о том, что изолированная офисная гипертензия может иметь клиническое значение. Ее неблагоприятное прогностическое значение было менее очевидным в клинических исследованиях, предполагавших изучение отдаленных исходов с поправкой на возраст и пол. В тоже время, в одном исследовании прогностическое значение офисной гипертензии в отношении частоты сердечно-сосудистых исходов занимало промежуточное положение между нормальными значениями АД и артериальной гипертензией.
Изолированную офисную гипертензию выявляют чаще уженщин с гипертензией 1-й степени (легкой), пожилых людей, некурящих, пациентов с недавно развившейся артериальной гипертензией, а также у пациентов, у которых измерения офисного АД проводились редко. Изолированную офисную гипертензию следует диагностировать, если офисное АДсоставляет ≥140/90 мм рт. ст. при, по крайней мере, в трех измерениях, в то время как среднесуточное и дневное АД находятся в пределах нормы. Диагноз может основываться также на результатах самостоятельного измерения АД в домашних условиях (если среднее нескольких значений домашнего АД составляет <135/85 мм рт. ст., а офисное АД ≥140/90 мм рт. ст.), хотя следует учитывать, что эти пациенты могут отличаться от больных, у которых офисная гипертензия диагностирована на основании результатов амбулаторного мониторирования АД. У некоторых людей отмечаются высокое домашнее АД и нормальные результаты амбулаторного мониторирования и наоборот. Фармакотерапию следует начинать при наличии поражения органов-мишеней и высокого сердечно-сосудистого риска.Однако модификация образа жизни и регулярное наблюдение рекомендуются всем пациентам с изолированной офисной гипертензией, даже если принято решение не начинать медикаментозную терапию.
3.1.5. Изолированная амбулаторная или маскированная гипертензия
Описан также обратный феномен, когда у пациентов с нормальным офисным АД (менее 140/90 мм рт. ст.) отмечается повышение среднесуточного или домашнего АД. Это состояние называют “изолированной амбулаторной гипертензией” или “маскированной гипертензией”. Ее распространенность в общей популяции примерно соответствует таковой изолированной офисной гипертензии. Полагают, что примерно каждый седьмой или восьмой пациент с нормальным офисным АД попадает в эту категорию. Информация о возможной динамике этого состояния ограниченна, однако у таких пациентов наблюдали более высокую частоту поражения органов-мишеней и метаболических факторов риска по сравнению с таковой у пациентов с истинно нормальным АД. Имеются данные о том, что максированная гипертензия повышает сердечно-сосудистый риск, который сопоставим с таковым у пациентов, у которых повышения АД регистрируются как в офисе, так и дома.
Таким образом, исследования последних лет продемонстрировали важность измерения АД вне кабинета врача с целью более точной оценки тяжести артериальной гипертензии и идентификации более высокого риска у некоторых пациентов с нормальным АД. Недавно в длительном исследовании было выявлено прогрессирующее нарастание 12-летнего риска смерти у пациентов с повышенным офисным, домашним и/или среднесуточным АД по сравнению с таковым у пациентов с нормальными значениями этих показателей. Амбулаторное мониторирование и измерение домашнегоАД позволяют получить полезную информацию даже при отсутствии явного повышения офисного АД, особенно у пациентов с многочисленными факторами риска и признаками поражения органов-мишеней.
3.1.6. АД во время нагрузки и лабораторного стресса
В лабораторных условиях применяли физические и психические стрессорные факторы, чтобы изучить ответную реакцию АД и ее возможное клиническое значение.Физический стресс предполагает физическуюактивность (динамическую или статическую) или пассивное воздействие физических факторов, например, холода. Для имитации психического стресса пациентам предлагают решать математические или технические задачи или принимать определенные решения.
Все стрессорные факторы вызывают повышение АД. В клинических исследованиях изучали возможность использования различных вариантов гипертензивного ответа с целью оценки риска развития артериальной гипертензии, поражения органов-мишеней, сердечно-сосудистых заболеваний или смерти.
Данные о риске развития артериальной гипертензии противоречивы. В некоторых исследованиях непропорциональное повышение АД при физической нагрузке служило независимым фактором риска развития артериальной гипертензии, а у мужчин реакция АД на психический стресс позволяла предсказать динамику АД и риск гипертензии в течение 10 ближайших лет. Однако вариабельность АД в течение последующих лет только частично объяснялась различной реакцией на стресс, а результаты других исследований оказались отрицательными.
В большинстве исследований у пациентов с нормальным АД и артериальной гипертензией не выявлено достоверной связи между прессорным эффектом динамической нагрузки и гипертрофией левого желудочка при наличии поправки на АД в покое. Однако недавно в одном исследовании было показано, что изменения систолического АД при субмаксимальной физической нагрузке являются мощным предиктором развития гипертрофии левого желудочка у пациентов с предгипертонией. Значение реакции АД на статистическую нагрузку изучалось редко, однако в одном исследовании не было выявлено достоверной связи между реакцией АД на сжимание руки в кулак и массой левого желудочка, тогда как увеличение АД, вызванное холодом, позволяло предсказать массу миокарда в одном, но не в другом исследовании. Прессорный ответ на решение арифметических задач был тесно связан с концентрическим ремоделированием левого желудочка, но не с массой его в одном исследовании, в то время как в других исследованиях связь между структурой левого желудочка и типом реакции АД отсутствовала.
Данные о том, может ли повышенная прессорная реакция на велоэргометрическую нагрузку предсказать сердечно-сосудиствую заболеваемость и смертность независимо от АД в покое, противоречивы. Результаты 21-летнего наблюдения недавно показали, что систолическое АД в положении лежа и после 6-минутной нагрузки позволяет прогнозировать сердечно-сосудистую смертность, особенно у пациентов с небольшим повышением АД. Однако при более тяжелой гипертензии ситуация может отличаться. Возможное дополнительное прогностическое значение чрезмерного повышения АД во время нагрузки по сравнению с таковым АД в покое может зависеть от влияния нагрузки на сердечный выброс. Если нарушено индуцированное нагрузкой повышение сердечного выброса (что характерно для пациентов с тяжелой гипертензией), то АД при нагрузке утрачивает независимое прогностическое значение. Отсутствие снижения периферического сосудистого сопротивления при нагрузке может указывать на неблагоприятный прогноз.
В целом, результаты анализа связи между ответной реакций АД на физический и психический стресс и вероятностью развития артериальной гипертензии и поражения органов-мишеней неоднозначны. Как указано выше, в 21-летнем исследовании было показано, что проба с физической нагрузкой позволяет получить некоторую дополнительную информацию о риске сердечно-сосудистых исходов, по крайней мере, у пациентов с легким повышением АД, так как принять решение о лечении при отсутствии других факторов риска или поражения органов-мишеней бывает трудно.Наконец, не следует забывать, что при нагрузке измеряют систолическое АД, а точность измерений значительно ниже, чем в покое.
3.1.7. Центральное АД
За счет наложения приходящих и отраженных волн в артериальной системе систолическое и пульсовое АД в аорте (т.е. давление на уровне сердца, головного мозга и почек) может отличаться от давления на плечевой артерии. Высказываются предположения о том, что антигипертензивные средства могут оказывать разное действие на периферическое и центральное систолическое и пульсовое АД. Необходимость в инвазивном измерении центрального АД препятствовала проведению исследований в этой области. Однако недавно был предложен неинвазивный метод оценки аортального АД на основании расчета “индекса усиления” по кривой пульсовой волны, зарегистрированной на периферической артерии. С помощью этого метода было подтверждено, что эффекты антигипертензивных препаратов на центральное систолическое и пульсовое АД не всегда отражают их действие на уровне плечевой артерии. Кроме того, в крупном рандомизированном исследовании было установлено, что центральное пульсовое АД тесно коррелирует с риском сердечно-сосудистых исходов. Однако прогностическое значение центрального АД требует дополнительного подтверждения.
3.2. Семейный и медицинский анамнез
При обследовании пациента следует собрать подробный семейный анамнез. Особое внимание следует уделять артериальной гипертензии, сахарному диабету, дислипидемии, ИБС, инсульту, поражению периферических артерий и заболеваниям почек. Среди анамнестических данных необходимо оценить следующие:
2) симптомы, указывающие на возможность вторичной гипертензии и прием препаратов или веществ, которые повышают АД (капли для носа, кокаин, амфетамины, оральные контрацептивы, стероиды, нестероидные противовоспалительные препараты, эритропоэтин, циклоспорин);
3) факторы образа жизни (потребление большого количества животных жиров, соли и алкоголя, курение и физическая активность, прибавка массы тела);
4) симптомы ИБС, сердечной недостаточности, цереброваскулярных заболеваний, поражения периферических артерий, заболевание почек, сахарный диабет, подагра, дислипидемия, астма или другие серьезные заболевания, прием препаратов, использующихся для лечения этих болезней,
5) предыдущую антигипертензивную терапию, ее результаты и нежелательные эффекты,
6) личные и семейные факторы и факторы окружающей среды, которые могут повлиять на АД, сердечно-сосудистый риск, а также на результаты лечения.
Кроме того, следует выяснить наличие храпа, который может быть признаком синдрома апноэ во сне и фактором сердечно-сосудистого риска.
| Рамка 4. Сбор семейного и медицинского анамнеза |
|---|
| 1. Длительность артериальной гипертензии и значения АД. 2. Признаки вторичной гипертензии: а. семейный анамнез заболевания почек (поликистоз);
б. поражение почек, инфекция мочевых путей, гематурия, злоупотребление анальгетиками (паренхиматозные заболевания почек); в. прием лекарственных средств (оральные контрацептивы, карбеноксолон, капли для носа, кокаин, амфетамины, стероиды, нестероидные противовоспалительные препараты, эритропоэтин, циклоспорин); г. приступы потливости, головной боли, тревоги, сердцебиений (феохромоцитома); д. эпизоды мышечной слабости и тетании (альдостеронизм). 3. Факторы риска: а. семейный и личный анамнез гипертензии и сердечно-сосудистых заболеваний;
б. семейный и личный анамнез дислипидемии; в. семейный и личный анамнез сахарного диабета; г. курение; д. особенности питания; е. ожирение, уровень физической активности; ж. храп, апноэ во сне; з. особенности личности. 4. Симптомы поражения органов-мишеней: а. головной мозг и зрение: головная боль, головокружение, нарушение зрения, транзиторные ишемические атаки, чувствительные или двигательные нарушения;
б. сердце: сердцебиения, боль в груди, одышка, отеки; в. почки: жажда, полиурия, никтурия, гематурия; г. периферические артерии: холодные конечности, перемежающаяся хромота. 5. Предыдущая антигипертензивная терапия: лекарства, эффективность и побочные эффекты; 6. Факторы окружающей среды. |
3.3. Физикальное обследование
Помимо АД, необходимо измерять ЧСС (в течение 30 с или более при наличии аритмии), так как ее повышение указывает на более высокий риск, увеличение симпатической или снижение парасимпатической активности или наличие сердечной недостаточности. Следует выявлять дополнительные факторы риска, признаки вторичной гипертензии и поражения органов-мишеней. Измеряют окружность талии в положении стоя, а также массу тела и рост, чтобы рассчитать индекс массы тела по стандартной формуле.
| Рамка 5. Физикальное обследование с целью выявления признаков вторичной гипертензии, поражения органов-мишеней и висцерального ожирения. |
|---|
| Признаки вторичной гипертензии и поражения органов-мишеней: |
|
| Признаки поражения органов-мишеней: |
|
| Признаки висцерального ожирения: |
≥ 25 кг/м2 – избыточная масса тела
≥ 30 кг/м2 – ожирение |
3.4. Лабораторные исследования
Целью лабораторных исследований является поиск дополнительных факторов риска, признаков вторичной гипертензии и поражения органов-мишеней. Начинают с самых простых исследований и переходят к более сложным. Чем моложе пациент, чем выше АД и чем быстрее развивается артериальная гипертензия, тем более тщательно необходимо проводить исследования. Однако минимальный набор лабораторных тестов продолжает обсуждаться. В Европе, где сердечно-сосудистые болезни остаются главной причиной заболеваемости и смертности, стандартные лабораторные исследования должны включать следующие показатели: глюкоза натощак, общий холестерин, холестерин ЛПНП, холестерин ЛПВП, триглицериды (натощак), мочевая кислота, креатинин, калий, гемоглобин и гематокрит, анализ мочи с помощью тест-полоски (микроальбуминурия), микроскопия осадка мочи и ЭКГ. Уровень креатинина в сыворотке является неточным показателем функции почек. Однако даже небольшое его повышение может указывать на серьезное поражение почек и высокий сердечно-сосудистый риск. Уровень креатинина используют также для расчета клиренса креатинина по формулеКокрофта-Голта или скорости клубочковой фильтрации по формуле MDRD. Эти показатели позволяют идентифицировать пациентов с низкой клубочковой фильтрацией и повышенным сердечно-сосудистым риском, у которых уровни креатинина остаются в пределах нормы (см. также раздел 3.6.3). Если глюкоза плазмы натощак составляет ≥ 5,6 ммоль/л (100 мг%), рекомендуется провести пробу на толерантность к глюкозе. Повторное повышение гликемии плазмы натощак ≥ 7,0 ммоль/л (126 мг%) или нарушение толерантности к глюкозе указывают на наличие сахарного диабета. Хотя уровень С-реактивного белка, измеренный с помощью высокочувствительногометода (вчСРБ), позволяет предсказать развитие сердечно-сосудистых исходов в определенных ситуациях, его роль в оценке общего сердечно-сосудистого риска остается спорной. Исключение составляют больные метаболическим синдромом, у которых уровень вчСРБ ассоциируется со значительным дополнительным повышением риска. Значение других показателей воспаления (фибриноген, цитокины, гомоцистеин, мозговой натрийуретический пептид и др.) продолжает активно изучаться, однако в настоящее время их измерение не рекомендуется.
| Рамка 6. Лабораторные тесты |
|---|
| Стандартные тесты: |
| • Гликемия плазмы натощак; • Общий холестерин; • Холестерин ЛПНП; • Холестерин ЛПВП; • Триглицериды; • Калий; • Мочевая кислота; • Креатинин; • Расчетный клиренс креатинина (формула Кокрофта-Голта) или скорость клубочковой фильтрации (формула MDRD); • Гемоглобин и гематокрит; • Анализ мочи (с определением микроальбуминурии с помощью тест-полосок и микроскопией осадка); • ЭКГ. |
| Рекомендуемые тесты: |
| • Эхокардиография; • Ультразвуковое исследование сонных артерий; • Количественный анализ протеинурии (если результаты анализа с помощью тест-полоски оказываются положительными); • Лодыжечно-плечевой индекс; • Исследование глазного дна; • Проба на толерантность к глюкозе (если гликемия плазмы натощак более 5,6 ммоль/л, или 100 мг%); • Домашнее и суточное мониторирование АД; • Измерение скорости пульсовой волны (если возможно). |
| Специальные исследования: |
| • Дополнительные исследования для оценки поражения головного мозга, сердца, почек и сосудов. Обязательны при осложненной гипертензии! • Подтверждение диагноза вторичной гипертензии, заподозренной на основании анамнеза, физикального исследования или стандартных тестов: ренин, альдостерон, кортикостероиды, катехоламины в плазме и/или моче, ангиография, ультразвуковое исследование почек и надпочечников, компьютерная томография, магнитно-резонансная томография. |
3.5. Генетический анализ
У больных с повышенным АД часто отягощен анамнез по артериальной гипертензии, что указывает на роль генетических факторов в развитии этого заболевания. Эссенциальная гипертензия является очень неоднородным состоянием. Это свидетельствует о ее многофакторной этиологии и наличии полигенных нарушений. Полиморфизм некоторых генов повышает чувствительность людей к определенным факторам окружающей среды. Установлены различные мутации генов, которые кодируют гормоны основных систем, контролирующих АД, однако их точная роль в патогенезе эссенциальной гипертензии остается неясной. Полиморфизм генов может оказывать влияние на ферменты, метаболизирующие лекарственные препараты и, соответственно, на их эффективность и переносимость. В последние годы эти вопросы изучались в различных исследованиях. Описано несколько вариантов моногенной гипертензии, таких как синдром Лиддля. При этих состояниях мутации одного гена полностью объясняют развитие артериальной гипертензии и определяют выбор подходов к ее лечению.
3.6. Выявление признаков повреждения органов-мишеней
Субклиническое поражение органов-мишеней является промежуточным этапом сердечно-сосудистого континуума и определяет общий сердечно-сосудистый риск. Поэтому необходимо тщательно исследовать органы, которые страдают при артериальной гипертензии. В настоящее время доказано неблагоприятное прогностическое значение бессимптомного поражения органов-мишеней у пациентов, страдающих и не страдающих повышенным АД.
1. Микроальбуминурия ассоциируется с увеличением сердечно-сосудистого риска не только у больных сахарным диабетом, но и у пациентов, не страдающих этим заболеванием. Увеличение риска было продемонстрировано даже при менее значительной экскреции альбумина с мочой.
2. Подтверждено неблагоприятное прогностическое значение гипертрофии левого желудочка, а также утолщения комплекса интима-медиа сонной артерии. Эти изменения встречаются значительно чаще, чем можно было бы предположить на основании стандартных исследований. Если не проводить ультразвуковое исследование левого желудочка и сонных артерий, то до 50% больных могут быть
ошибочно отнесены к группе низкого или среднего дополнительного риска, в то время как наличие поражения сердца или сосудов указывает на более высокий риск.
3. При ретроспективном анализе клинических исследований было установлено, что уменьшение протеинурии и гипертрофии левого желудочка под влиянием антигипертензивной терапии приводит к снижению частоты сердечно-сосудистых исходов. Таким образом, диагностика поражения органов-мишеней имеет значение не только для количественного анализа сердечно-сосудистого риска, но и для мониторирования протективного эффекта антигипертензивных средств.
В настоящих рекомендациях, как и в 2003 г., выделен специальный раздел, в которомо бсуждается прогностическое значение поражения различных органов-мишеней и методы его диагностики. Скрининг на микроальбуминурию в настоящее время рекомендуют проводить всем больным артериальной гипертензией, а также пациентам с метаболическим синдромом, даже при наличии высокого нормального АД. Эхокардиография и ультразвуковое исследование являются рекомендуемым методами, особенно больным, у которых поражение органов-мишеней не удается выявить с помощью стандартного обследования, например ЭКГ, а также пожилым людям, у которых часто наблюдаются гипертрофия сердца и поражение сосудов. Информативным методом изучения состояния сосудов является измерение жесткости артерий по скорости пульсовой волны. Однако этот метод пока недостаточно распространен. Методы диагностики поражения органов-мишеней подробно описаны ниже.
| Рамка 7. Диагностика бессимптомного поражения органов-мишеней |
|---|
| Бессимптомное поражение органов-мишеней является промежуточным этапом сердечно-сосудистого континуума и определяет общий сердечно-сосудистый риск. |
| 1. Сердце |
| Всем больным с высоким АД следует проводить электрокардиографию с целью диагностики гипертрофии левогожелудочка, его перегрузки, ишемии миокарда и аритмий. Эхокардиография показана и в тех случаях, когда обоснованно применение более чувствительного метода. Она позволяет определить геометрические типы гипертрофии миокарда, среди которых худшее прогностическое значение имеет концентрическая гипертрофия. Для оценки диастолической дисфункции используют допплерографию кровотока через митральное отверстие. |
| 2. Сосуды |
| Ультразвуковое исследование сонных артерий проводят в тех случаях, когда целесообразно выявление гипертрофии стенки сосудов или бессимптомного атеросклероза. Увеличение жесткости крупных артерий (которое приводит к развитию изолированной систолической гипертензии у пожилых людей) может быть выявлено по изменению скорости пульсовой волны.Низкий лодыжечно-плечевой индекс указывает на тяжелое поражение периферических артерий. |
| 3. Почки |
| Поражение почек при артериальной гипертензии диагностируют на основании сниженной их функции или повышенной экскреции альбумина с мочой. Во всех случаях следует рассчитывать скорость клубочковой фильтрации (по формуле MDRD с учетом возраста, пола и расы) или клиренс креатинина (по формуле Кокрофта-Голта с учетом массы тела). Для выявления протеинурии у всех пациентов с артериальной гипертензией применяют тест-полоски. Если результат теста отрицательный, то определяют микроальбуминурию, которую соотносят с экскрецией креатинина с мочой. |
| 4. Исследование глазного дна |
| Исследование глазного дна рекомендуется только больным тяжелой гипертензией. Легкие изменения сетчатки обычно неспецифичны (исключение составляют люди молодого возраста). Геморрагии, экссудаты и отек соска зрительного нерва, наблюдающиеся при тяжелой гипертензии, сопровождаются высоким сердечно- сосудистым риском. |
| 5. Головной мозг |
| Скрытый мозговой инфаркт, лакунарный инфаркт, микрокровоизлияния и поражение белого вещества головного мозга нередко наблюдаются у больных артериальной гипертензией и могут быть выявлены с помощью МРТ или КТ, хотя высокая стоимость и недостаточная доступность этих методов ограничивают их применение. У пожилых людей тесты на когнитивную функциюпозволяют диагностировать начальное поражение головного мозга. |
| Сведения о доступности, прогностическом значении и стоимости различных методов диагностики бессимптомного поражения органов-мишеней приведены в табл. 4. |
3.6.1. Сердце
ЭКГ является обязательным исследованием у всех больных с высоким АД. Чувствительность метода в диагностике гипертрофии левого желудочка низкая, но тем не менее, гипертрофия левого желудочка, диагностированная на основании индекса Соколова-Лайона (SV1+RV5-6>38 мм) или индекса Корнелла (произведение амплитуды и длительности QRS > 2440 мм•мс), является независимым сердечно-сосудистым фактором риска и имеет важное значение для оценки наличия поражения сердца и кардиопротективного эффекта антигипертензивной терапии, по крайней мере, у больных старше 55 лет. ЭКГ позволяет также выявить перегрузку левогожелудочка (указывающую на более высокий риск), ишемию миокарда, нарушения проводимости и аритмии, включая фибрилляцию предсердий, которая нередко развивается у пожилых больных артериальной гипертензией. Холтеровское мониторирование проводят с целью диагностики аритмий или выявления эпизодов ишемии миокарда, а также сниженной вариабельности сердечного ритма, которая отмечается при тяжелой гипертензии. Однако прогностическое значение этого признака не доказано, хотя оно было продемонстрировано при сердечной недостаточности и после инфаркта миокарда.
Эхокардиография, несмотря на определенные технические ограничения (вариабельность результатов, низкое качество изображения у больных ожирением и обструктивными заболеваниями легких и т.д.), является более чувствительным методом диагностики гипертрофии левого желудочка и оценки сердечно-сосудистого риска. Она позволяет точнее стратифицировать общий риск и выбрать схему лечения. Адекватное исследование предполагает измерение толщины задней стенки левого желудочка и межжелудочковой перегородки, конечного диастолического размера левого желудочка и расчет его массы по стандартной формуле. Хотя связь между индексом массы миокарда левогожелудочка и сердечно-сосудистым риском непрерывна, общепринятыми критериями диагностики гипертрофии левогожелудочка являются значения индекса массы более 125 г/м2 у мужчин и 110 г/м2 у женщин. Повышенную частоту сердечно-сосудистых исходов позволяют предсказать концентрическая гипертрофия левого желудочка (отношение толщины стенки к радиусу левогожелудочка ≥ 0,42 при наличии увеличенной массыжелудочка), эксцентрическая гипертрофия (увеличение массы миокарда при отношении толщины стенки к радиусу < 0,42) и концентрическое ремоделирование (отношение толщины стенки к радиусу ≥ 0,42 при нормальной массе левого желудочка). Однако наиболее неблагоприятным прогнозом характеризуется концентрическая гипертрофия миокарда.
Кроме того, эхокардиография позволяет оценить систолическую функцию левого желудочка. Дополнительными факторами риска сердечно-сосудистых осложнений считают изменение фракции выброса, а также утолщение эндокарда и стенки. Заполнение левого желудочка в диастолу (диастолическая функция) может быть изучено с помощью допплерографии на основании измерения коэффициента Е/А трансмитрального кровотока, времени раннего диастолического расслабления и кровотока из легочной вены в левое предсердие. Полезная информация может быть получена также с помощью тканевой допплерографии латеральной части митрального отверстия. Эти методы представляют большой интерес, так как у значительной части больных (около 50%) сердечной недостаточностью наблюдается диастолическая дисфункция при отсутствии существенных изменений систолической функции левогожелудочка (так называемая диастолическая сердечная недостаточность). Нарушения диастолической функции часто наблюдаются у больных артериальной гипертензией (у каждого четвертого пожилого пациента). Эти изменения могут возникнуть при отсутствии систолической дисфункции, и даже гипертрофии левого желудочка. Имеются данные о том, что диастолическая дисфункция повышает риск развития фибрилляции предсердий. Более того, в двух исследованиях было показано, что она позволяет предсказать развитие сердечной недостаточности и ассоциируется с увеличением общей смертности, хотя в другом исследовании последняя ассоциация зависела от наличия ряда кофакторов. Наконец, эхокардиография дает возможность оценить наличие и степень дилатации левого желудочка, которая ассоциируется с риском развития фибрилляции предсердий, сердечно-сосудистых исходов и смерти. Кроме того,могут быть получены данные о сегментарных дефектах сократимости левого желудочка, связанных с ишемией или перенесенным инфарктом.
Другие методы диагностики, такие как МРТ, сцинтиграфию сердца, пробу с нагрузкой и коронарную ангиографию, применяют по соответствующим показаниям. Рентгенография грудной клетки может оказаться полезной, если имеется одышка или необходимо исследование крупных внутригрудных артерий, однако в целом этот метод не имеет большого значения в диагностике гипертонического поражения сердца.
В последние годы вызывает интерес возможность изучения степени фиброза сердца с помощью ультразвуковых методов. Показано, что состав ткани миокарда при гипертрофии левого желудочка может меняться, а препараты, вызывающие регресс гипертрофии, оказывают разное влияние на фиброз. В настоящее время самым точным методом изучения состава ткани сердца является МРТ, однако высокая стоимость исследования препятствует его широкому применению. Изучают циркулирующие маркеры отложения коллагена в тканях, однако они только частично образуются в сердце.
3.6.2. Сосуды
Существует несколько неинвазивных методов изучения структуры и функции крупных артерий при артериальной гипертензии. Измерение толщины комплекса интима-медиа (ТИМ) сонных артерий с помощью ультразвукового метода позволяет предсказать развитие как инсульта, так и инфаркта миокарда. Связь между ТИМ сонных артерий и сердечно-сосудистыми исходами непрерывна, однако общепринятым критерием ее утолщения является значение более 0,9 мм. Ультразвуковое исследование общих сонных артерий, в которых атеросклероз развивается редко, позволяет оценить только гипертрофию сосудов, в то время как для выявления атеросклероза необходимо исследовать также бифуркации и/или внутренние сонные артерии, где бляшки определяются чаще. О наличии бляшки свидетельствует увеличение ТИМ более 1,3 или 1,5 мм или локальное увеличение толщины на 0,5 мм или на 50% по сравнению с соседними участками. Подобные изменения часто встречаются у нелеченых больных артериальной гипертензией, у которых не удается выявить поражение органов-мишеней с помощью стандартных методов. Соответственно, ультразвуковой метод часто позволяет диагностировать скрытое поражение сосудов и точнее стратифицировать сердечно-сосудистый риск. Признаком поражения артерий может быть лодыжечно-плечевой индекс менее 0,9 (его измеряют с помощью допплеровского метода и обычного тонометра). Низкий лодыжечно-плечевой индекс указывает на поражение периферических артерий и далеко зашедший атеросклероз, тогда как при исследовании сонных артерий можно выявить более ранние изменения. Снижение лодыжечно-плечевого индекса ассоциируется с развитием стенокардии, инфаркта миокарда, инсульта и повышенной вероятностью вмешательств на сонных и периферических сосудах. У больных с многососудистым коронарным атеросклерозом изменения этого показателя считают дополнительным фактором риска.
В последние 10 лет накоплено много данных об увеличении жесткости стенок крупных артерий и феномене отраженной волны, которые считают основными факторами, определяющими развитие изолированной систолической гипертензии и повышение пульсового давления. Измерение жесткости стенок артерий на основании изменений диаметра сосудов в зависимости от изменений АД представляет собой сложную задачу, которую трудно решить в обычной практике. С другой стороны, измерение скорости пульсовой волныв сонной или бедренной артериях позволяет неинвазивно оценить жесткость артерий и является достаточно простым и точным методом. Этот показатель считают независимым фактором риска общей смертности и сердечно-сосудистой заболеваемости, коронарных осложнений и инсульта у больных неосложненной эссенциальной гипертензией. Хотя связь междужесткостью аорты и риском осложнений является непрерывной, критерием существенного изменения функции аорты у пациентов среднего возраста считают увеличение скорости пульсовой волны более 12 м/с. В настоящее время подобные методы, в основном, применяют с научными целями.
Как видно из табл. 4, некоторые методы диагностики поражения сосудов не могут быть использованы в клинической практике по различных причинам. Увеличение отношения толщины стенки к диаметру просвета мелких артерий может быть выявлено в подкожной ткани, взятой при биопсии. Этот метод позволяет диагностировать ранние изменения сосудов при сахарном диабете и артериальной гипертензии, а результаты исследования коррелируют с сердечно-сосудистой заболеваемостью и смертностью. Однако инвазивность метода делает его непригодным для широкого применения. Увеличение содержания кальция в коронарных артериях, которое оценивают с помощью компьютерной томографии высокого разрешения, также является сердечно-сосудистым фактором риска, однако препятствиями к использованию метода служат ограниченная доступность и высокая стоимость. Эндотелиальная дисфункция имеет прогностическое значение при некоторых сердечно-сосудистых заболеваниях, но ее информативность при артериальной гипертензии изучена недостаточно .
Кроме того, методы анализа эндотелиального ответа на различные факторы остаются инвазивными, трудоемкими и нестандартизированными. При этом неясно, отражает ли эндотелиальная функция сосудов одного органа состояние других сосудов. В связи с этим, изучение эндотелиальной функции в настоящее время не может быть рекомендовано больным артериальной гипертензией. Тем не менее, результаты исследований циркулирующих маркеров активности эндотелия, а также предшественников эндотелиальных клеток оказались обнадеживающими. В ближайшем будущем можно ожидать появления более простых маркеров повреждения эндотелия. Их информативность необходимо будет изучить в крупных исследованиях.
3.6.3. Почки
Критериями диагностики поражения почек при артериальной гипертензии являются снижение их функции и/или экскреция альбуминов с мочой. Почечную недостаточность в настоящее время классифицируют в соответствии со скоростью клубочковой фильтрации, рассчитанной по формуле MDRD с учетом возраста, пола, расы и сывороточного уровня креатинина. Расчетная скорость клубочковой фильтрации менее 60 мл/мин/1,73м2 указывает на наличие хронической болезни почек 3-й стадии; менее 30 и 15 мл/мин/1,73 м2 – 4-й и 5-й стадий, соответственно. По формуле Кокрофта-Голта рассчитывают клиренс креатинина с учетом возраста, пола, масса тела и сывороточного уровня креатинина. Эта формула информативна в диапазоне более 60 мл/мин, однако она завышает клиренс креатинина при хронической болезни почек 3-й-5-й стадии. Обе формулы позволяют выявить легкие нарушения функции почек при нормальных значениях уровня креатинина. Снижение клубочковой фильтрации и увеличение сердечно-сосудистого риска отражаются также в повышении сывороточных уровней цистатина С.
Небольшое увеличение сывороточного креатинина (до 20%) иногда наблюдается после назначения или изменения антигипертензивной терапии, однако это не следует рассматривать как признак ухудшения функции почек. У нелеченых больных артериальной гипертензией часто наблюдается гиперурикемия (особенно при преэклампсии), которая коррелирует со снижением почечного кровотока и наличием нефросклероза. Если повышение сывороточной концентрации креатинина или снижение расчетной скорости клубочковой фильтрации (или клиренса креатинина) указывают на ухудшение клубочковой фильтрации, то увеличение экскреции альбуминов или белка с мочой отражает повреждение клубочков.Микроальбуминурия (см. табл. 2) позволяет предсказать развитие явной диабетической нефропатии у больных сахарным диабетом 1-го и 2-го типа, тогда как протеинурия свидетельствует о более тяжелом поражении паренхимы почек. У больных артериальной гипертензией, страдающих и нестрадающих сахарным диабетом, микроальбуминурия (даже ниже пороговых значений) является фактором риска сердечно-сосудистых осложнений. Выявлена непрерывная связь между сердечно-сосудистой и общей смертностью и значением коэффициента белок/креатинин мочи у мужчин (≥3,9 мг/г) и женщин (≥7,5 мг/г). Следовательно, термин «микроальбуминурия»может вводить в заблуждение (кроме того, он неправильно ориентирует на небольшое повреждение) и теоретически должен быть заменен термином «низкая альбуминурия». Микроальбуминурию можно измерять в разовой порции мочи (использование суточной или ночной мочи не рекомендуется) по отношению концентрации альбумина и креатинина. Стандартные тест-полоски позволяют выявить альбуминурию выше 300 мг/г креатинина, а «микроальбуминурические» тест-полоски – более 30 мг/г креатинина. В настоящее время изучаются более чувствительные тест-полоски, с помощью которых можно выявить более низкую альбуминурию.
Таким образом, нарушенияфункции почек, которые диагностируют с помощью перечисленных выше параметров, часто встречаются у больных артериальной гипертензией и являются мощным фактором риска сердечно-сосудистых осложнений и смерти, даже у леченых пациентов. В связи с этим у всех больных артериальной гипертензией рекомендуется рассчитывать клубочковую фильтрацию и оценивать наличие белка в моче (с помощью тест-полосок). Если результаты последнего теста оказываются отрицательными, то целесообразно измерять низкую альбуминурию с помощью валидированных коммерческих методов, по крайней мере, дважды. При этом следует рассчитывать отношение альбуминурии к экскреции креатинина с мочой с поправкой на пол.
3.6.4. Исследование глазного дна
В 30-х гг. XX века Keith, Wagener и Barker выделили четыре степени гипертонической ретинопатии, однако сегодня большинство больных артериальной гипертензией обращаются к врачу на раннем этапе заболевания, поэтому геморрагии и экссудаты (3-я степень) и отек соска зрительного нерва (4-я степень) встречаются очень редко. В то же время ретинопатию 1-й степени (очаговое или генерализованное сужение артериол) и 2-й степени (перекрест артериол и венул) выявляют значительно чаще, чем другие маркеры поражения органов-мишеней, имеющие клиническое значение (гипертрофия левого желудочка, бляшки в сонных артериях и микроальбуминурия). Прогностическое значение начальных степеней ретинопатии подвергается сомнению. Эти изменения малоспецифичны, хотя у молодых людей изменения сетчатки должны обратить на себя внимание врача. Напротив, ретинопатия 3-й и 4-й степени ассоциируется с увеличением сердечно-сосудистого риска. Разработаны более «селективные» методы изучения повреждения органов зрения при артериальной гипертензии. Например, для оценки состояния артериол и венул используют полуавтоматический анализ фотографий глазного дна. С помощью этого метода были изучены топологические изменения сосудов сетчатки, связанные с артериальной гипертензией. Сужение артериол и венул может предшествовать развитиюартериальной гипертензии. Однако этот метод по-прежнему применяют только с научными целями.
3.6.5. Головной мозг
У больных, перенесших инсульт, наличие, характер и локализация очаговых изменений могут быть оценены с помощью томографии. Компьютерная томография (КТ) – стандартный метод диагностики инсульта, хотя он постепенно вытесняется магнитно-резонансной томографией (МРТ). Исключением является необходимость быстрой диагоностики внутричерепного кровотечения. МРТ позволяет выявить ишемическое повреждение головного мозга в течение нескольких минут после окклюзии артерии. Кроме того, этот метод имеет преимущества перед КТ в диагностике скрытых мозговых инфарктов, большинство которых являются небольшими и глубокими (лакунарный инфаркт). В нескольких исследованиях было показано, что небольшие инфаркты мозга, микрокровоизлияния и поражения белого вещества нередко наблюдаются в общей популяции, а их частота увеличивается с возрастом и при наличии артериальной гипертензии. Эти изменения ассоциируются с высоким риском инсульта, ухудшения когнитивной функции и развития деменции. Недостаточная доступность и стоимость препятствуют широкому применению МРТ для обследования пожилых больных артериальной гипертензией, однако скрытый мозговой инфаркт следует исключать у всех больных с неврологическими нарушениям, особенно со сниженной памятью. Когнитивные расстройства у пожилых людей, по крайней мере, частично связаны с артериальной гипертензией, поэтому при обследовании пожилых пациентов следует использовать адекватные тесты на когнитивную функцию.
4. Необходимость лечения артериальной гипертензии
4.1. Введение
Ниже обсуждаются доказательства пользы антигипертензивной терапии, а также сравниваются благоприятные эффекты препаратов разных классов. Самыми надежными доказательствами считают результаты крупных рандомизированных исследований, в которых изучаются фатальные и нефатальные исходы, хотя они также имеют определенные ограничения.
В рандомизированные исследования приходится включать пожилых людей или других пациентов, относящихся к группе высокого риска, чтобы зарегистрировать максимально возможное число исходов и обеспечить высокую статистическую значимость результатов. Как следствие, в подобных исследованиях плохо представлены молодые пациенты с неосложненной гипертензией, относящиеся к группе низкого риска. Соответственно, прямая информация о пользе антигипертензивной терапии у значительной части больных артериальной гипертензией отсутствует. Кроме того, протоколы клинических исследований часто отличаются от реальной практики лечения артериальной гипертензии, так как прием антигипертензивных средств, назначенных после рандомизации в начале исследования, обычно продолжают даже при отсутствии существенного снижения АД, тогда как врач в этой ситуации заменяет их другими средствами. В связи с этим, в клинических исследованиях благоприятный эффект лечения может быть занижен за счет отсутствия пользы терапии у пациентов, не реагирующих на антигипертензивные средства.
Пожалуй, главным недостатком исследований является их небольшая продолжительность (в большинстве случаев 4-5 лет), в то время как ожидаемая продолжительность жизни у пациентов среднего возраста составляет 20-30 лет. Отдаленные результаты антигипертензивной терапии, а также особенности эффектов препаратов разных классов недавно были изучены путем продолжения наблюдения за пациентами после завершения клинических исследований. Однако подобные исследования являются неконтролируемыми, что снижает ценность полученных результатов.
Дополнительным подходом к изучению целесообразности лечения является использование промежуточных конечных точек, таких как бессимптомное поражение органов-мишеней. Подобные показатели менее надежны, чем «твердые» конечные точки (фатальный или нефатальный инфаркт миокарда или инсульт, смерть от сердечно-сосудистых или любых причин). Однако убедительно доказано, что некоторые признаки поражения органов-мишеней позволяют с высокой точностью предсказать последующее развитие фатальных и нефатальных исходов, т.е. «твердых» конечных точек. К подобным показателям относят изменения протеинурии и эхокардиографических или электрокардиографических признаков гипертрофии левого желудочка (разделы 3.6 и 4.5). Понятно, что неблагоприятные клинические исходы не развиваются при здоровой сердечно-сосудистой системе; им всегда предшествуют изменения структуры или функции органа. Поэтому ниже рассматриваются результаты исследований, в которых изучалось поражение органов-мишеней. Информативными критериями пользы антигипертензивной терапии могут служить изменения сопутствующих состояний, в частности сахарного диабета, метаболических нарушений и терминальной почечной недостаточности. Терминальная болезнь почек ассоциируется с резким возрастанием сердечно-сосудистого риска.Она использовалась в качестве конечной точки в нескольких клинических исследованиях. Промежуточной конечной точкой считают также развитие сахарного диабета, прогностическое значение которого более подробно обсуждается в разделе 4.5.5.
Ниже приводятся также результаты мета-анализов клинических исследований, хотя они не всегда являются самым надежным доказательством. Мета-анализ обладает более высокой статистической значимостью, чем конкретное исследование, и позволяет оценить средний эффект лечения, однако он имеет определенные ограничения. Мета-анализ проводят ретроспективно, выбор исследований часто субъективен, а исследования неоднородны, причем разницу между ними не всегда можно определить с помощью статистических тестов. В связи с этим результаты мета-анализа, как и другие источники информации, следует оценивать критически.
4.2. Плацебоконтролируемые исследования
Результаты рандомизированных плацебоконтролируемых исследований, в которых изучалась польза снижения АД, оказались однозначными. Они были включены в несколько мета-анализов и базировались на большом числе пациентов. Результаты можно суммировать следующим образом:
2) ее польза проявляется у пожилых людей, в том числе больных изолированной систолической гипертензией;
3) степень снижения сердечно-сосудистого риска сходна у мужчин и женщин и у представителей европеоидной, монголоидной и негроидной рас, что указывает на эффективность терапии в различных этнических группах;
4) антигипертензивная терапия сопровождается значительным снижением риска фатального и нефатального инсульта (примерно на 30-40%) и менее существенным снижением риска коронарных осложнений (на 20%).
Наконец, антигипертензивная терапия значительно снижает частоту развития сердечной недостаточности.
При мета-анализах плацебоконтролируемых исследований специально изучалась эффективность препаратов разных классов, хотя сравнивать полученные данные сложно, учитывая разницу степени снижения АД на фоне приема активных препаратов и плацебо в различных исследованиях. Тем не менее, продемонстрировано снижение сердечно-сосудистой заболеваемости и смертности, а также риска отдельных исходов в тех случаях, когда лечение начинали с тиазидного диуретика или бета-блокатора. Улучшение прогноза было отмечено и при лечении антагонистом кальция или ингибитором АПФ.
Подтвержденная эффективность антигипертензивной терапии не позволяет проводить плацебоконтролируемые исследования, т.е. сравнивать результаты лечения активным препаратом и только плацебо. По этой причине в последние годы новые препараты сравнивали с плацебо у больных, получающих другие антигипертензивные средства. Подобные исследования подтвердили пользу препаратов различных классов даже в тех случаях, когда степень снижения АД была небольшой, а исходные его значения не соответствовали традиционным критериям диагностики артериальной гипертензии. В исследовании HOPE у больных группы высокого сердечно-сосудистого риска (в основном, инфаркт миокарда в анамнезе), получавших различные сердечно-сосудистые средства, применение рамиприла привело к умеренному снижению АД (систолическое АД снизилось примерно на 3 мм рт. ст.) и четкому снижению(на 22%) частоты сердечно-сосудистых исходов по сравнению с плацебо. В исследовании FEVER антагонист кальция фелодипин сравнивали с плацебо у больных артериальной гипертензией среднего риска, у которых АД находилось в пределах 160/90 мм рт. ст. на фоне проводимой антигипертензивной терапии. В группе фелодипина АД снизилось в большей степени, чем в группе плацебо (на 3,5/1,5 мм рт. ст.). При этом риск любых сердечно-сосудистых исходов достоверно снизился примерно на 28%. В исследовании EUROPA у больных с ИБС, которые получали различные сердечно-сосудистые средства, снижение АД (на 5/2 мм рт. ст.) на фоне лечения ингибитором АПФ периндоприлом (± индапамидом) привело к уменьшению риска сердечно-сосудистых исходов по сравнению с плацебо независимо от исходного АД. В исследовании ACTION у больных стенокардией небольшое снижение АД при лечении нифедипином с замедленным высвобождением действующего вещества в сочетании с другими средствами также сопровождалось снижением частоты сердечно-сосудистых осложнений по сравнению с плацебо (только в подгруппе больных артериальной гипертензией). Снижение риска сердечно-сосудистых исходов было отмечено и в исследовании CAMELOT у больных с ИБС, у которых назначение амлодипина привело к большему (на несколько мм рт. ст.) снижению АД по сравнению с плацебо. Однако в похожем исследовании не была подтверждена польза активной терапии.
Сходный подход был использован при изучении новых препаратов, таких как антагонисты ангиотензиновых рецепторов. В исследовании SCOPE у больных старше 70 лет с артериальной гипертензией лечение кандесартаном (часто в сочетании с диуретиком) привело к небольшому дополнительному снижениюАД по сравнению с плацебо, которое также часто сочетали с диуретиком (разница между группами составила 3,2/1,6ммрт. ст.).При этом выявлено достоверное снижение риска развития нефатального инсульта. В исследованиях RENAAL и IDNT у больных артериальной гипертензией, сочетавшейся с сахарным диабетом 2-го типа и нефропатией, присоединение лозартана или ирбесартана к комбинированной антигипертензивной терапии замедлило прогрессирование нефропатии (первичная конечная точка), но не оказало существенного влияния на большинство вторичных сердечно-сосудистых конечных точек (хотя оба исследования не обладали достаточной статистической силой). Тем не менее, при объединении результатов этих двух исследований было выявлено значительное снижение сердечно-сосудистой заболеваемости при лечении антагонистом ангиотензиновых рецепторов. Таким образом, можно сделать вывод о том, что эти препараты также дают благоприятный эффект при артериальной гипертензии.
4.3. Сравнение более и менее агрессивной антигипертензивной терапии
Информация по этому вопросу была, в основном, получена в крупномисследовании HOT, хотя были проведены и менее крупные исследования, в основном, у больных сахарным диабетом. Результаты 5-ти исследований, охватывающих примерно 22 000 больных, были включены в мета-анализ Blood Pressure Lowering Treatment Trialists' (BPLTT). Полученные данные продемонстрировали пользу более жесткого контроля АД для снижения риска инсульта и основных сердечно-сосудистых исходов, особенно при сахарном диабете. Дополнительную информацию можно получить на основании результатов последних плацебоконтролируемых исследований (см. выше), в которых пациенты группы плацебо получали несколько менее интенсивную антигипертензивную терапию. Наконец, косвенными доказательствами могут служить результаты таких исследований, как HDFP, в которых сравнивали различные схемы антигипертензивной терапии, обеспечивавшие разную степень снижения АД. Практически во всех случаях более низкие значения АД сопровождались, по крайней мере, тенденцией к снижению частоты инсульта (см. раздел 4.4).
4.4. Сравнение препаратов разных классов в исследованиях с твердыми конечными точками
После публикации рекомендаций ESH/ESC 2003 года был проведен мета-анализ клинических исследований, в которых сравнивали различные схемы антигипертензивной терапии. Он послужил основой для обсуждения эффектов препаратов разных классов.Однако мы также приводим результаты последних исследований, которые не были включены в мета-анализ BPLTT, и критически оцениваем проблемы, возникавшие в этих исследованиях.
Указанные исследования позволили получить важную информацию о сравнительной эффективности антигипертензивных препаратов различных классов, однако интерпретировать полученные данные сложно, так как степень снижения АД в группах сравнения часто отличалась. Эти различия были обычно небольшими, однако даже небольшая разница АД может сопровождаться значительной разницей клинических исходов, а статистический анализ не позволяет адекватно решить эту проблему. Мета-регрессионный анализ дает возможность учесть разницу антигипертензивных эффектов, однако исследования, включаемые в такой анализ, еще менее однородны, чем при классическом мета-анализе. Наконец, в сравнительных исследованиях пациенты получали изучаемые препараты только в начале лечения, тогда как к концу исследований большинство рандомизированных больных получали комбинированную терапию разными препаратами, которые имели сходное распределение в группах сравнения.
4.4.1. Антагонисты кальция по сравнению с тиазидными диуретиками и бета-блокаторами
Недавно были обобщены результаты 9-ти исследований, в которых антагонисты кальция сравнивали с другими препаратами более чем у 68 000 больных. Степень снижения АД в группах сравнения была сопоставимой.Отношения шансов указывали на возможное преимущество антагонистов кальция перед стандартными препаратами, однако достоверная разница в общей смертности, сердечно-сосудистой смертности, риске любых сердечно-сосудистых исходов и инфаркта миокарда между группами отсутствовала. Антагонисты кальция вызывали несколько большее снижение риска инсульта, но уступали препаратам сравнения по эффективности в профилактике сердечной недостаточности. Результаты оказались сходными у больных, страдавших и не страдавших сахарным диабетом. В исследовании ASCOT изучалась сравнительная эффективность антигипертензивной терапии, которую начинали с антагониста кальция (амлодипина) или стандартного препарата. Исследование INVEST, не включенное в мета-анализ, также продемонстрировало сопоставимую частоту сердечно-сосудистых исходов у больных ИБС, которые начинали лечение с антагониста кальция (верапамила, часто в комбинации с ингибитором АПФ) или бета-блокатора (атенолола, часто в комбинации с диуретиком). Терапия на основе амлодипина привела к несколько более значительному снижению АД, что сопровождалось выраженным снижением риска инсульта, сердечно-сосудистой и общей смертности. Как и в большинстве других исследований, в ASCOT большинство пациентов получали комбинированную терапию (антагонист кальция/ингибитор АПФ или бета-блокатор/тиазидный диуретик).
4.4.2. Ингибиторы АПФ по сравнению с тиазидными диуретиками и бета-блокаторами
В мета-анализ BPLTT были включены 6 рандомизированных исследований, в которых примерно у 47 000 больных сравнивали ингибиторы АПФ с диуретиками и бета-блокаторами. В целом, отношения шансов указывали на возможные преимущества ингибиторов АПФ, однако достоверная разница в общей смертности, риске любых сердечно-сосудистых исходов, сердечно-сосудистой смерти и ИБС отсутствовала. Ингибиторы АПФ несколько уступали препаратам сравнения по эффективности в профилактике инсульта и застойной сердечной недостаточности. Незначительная разница отношения шансов любых сердечно-сосудистых исходов была выявлена при анализе результатов лечения у больных, страдавших и не страдавших сахарным диабетом.
Следует отметить неоднозначность результатов исследований, в которых ингибиторы АПФ сравнивали с диуретиками. Во втором австралийском исследовании у больных артериальной гипертензией, получавших ингибитор АПФ, выявили снижение частоты сердечно-сосудистых исходов по сравнению с пациентами, которым был назначен тиазидный диуретик.Однако разница была небольшой, проявлялась только у мужчин и достигла статистической значимости только после включения повторных исходов. В исследовании ALLHAT, напротив, частота ИБС (первичная конечная точка) была сходной в группах хлорталидона и лизиноприла, однако частота сердечной недостаточности и инсульта была значительно ниже при лечении диуретиком (в этой группе выявили также большее снижение АД).
4.4.3. Ингибиторы АПФ по сравнению с антагонистами кальция
Препараты двух классов сравнивали в 6-ти исследованиях почти у 26 000 больных. Разницы коронарной, сердечно-сосудистой и общей смертности, а также частоты ИБС не выявили. Антагонисты кальция превосходили ингибиторы АПФ по эффективности в профилактике инсульта, а ингибиторы АПФ более эффективно снижали риск развития сердечной недостаточности.
4.4.4. Антагонисты ангиотензиновых рецепторов по сравнению с другими препаратами
В 5-ти исследованиях сравнивали антагонисты ангиотензиновых рецепторов с другими препаратами. Разница препаратов сравнения затрудняет проведение мета-анализа этих исследований. В исследовании LIFE более чем у 9 000 больных артериальной гипертензией с ЭКГ-признаками гипертрофии левого желудочка среднее АД снизилось в сходной степени в группах пациентов, которые начинали лечение с лозартана или бета-блокатора атенолола. В течение примерно 5-ти лет у больных группы лозартана выявлено достоверное снижение риска основных сердечно-сосудистых исходов (первичная конечная точка) на 13%. Частота инфаркта миокарда не различалась, в то время как разница в частоте инсульта составила 25%. Достоверное снижение риска нефатального инсульта (хотя он не был первичной конечной точкой) было отмечено также у пожилых пациентов в исследовании SCOPE, в котором кандесартан вызвал несколько более значительное снижение АД, чем плацебо и обычная терапия. В исследовании MOSES примерно у 1 500 больных артериальной гипертензией, перенесших нарушения мозгового кровообращения, сравнивали результаты лечения, которое начинали с эпросартана или антагониста кальция нитрендипина. В среднем за 2,5 г. АД снизилось в двух группах в сходной степени. Частота сердечно-сосудистых исходов была значительно ниже в группе эпросартана, однако снижение частоты инсульта выявили только при анализе повторных нарушений мозгового кровообращения. В исследовании JIKEY HEART более чем у 3 000 японцев с артериальной гипертензией высокого риска (ИБС, сердечная недостаточность, сахарный диабет или множественные факторы риска) применение валсартана привело к снижению АД со 139/81 до 132/78 мм рт. ст. В течение 3 лет выявили значительное снижение риска развития инсульта (на 40%) по сравнению с группой больных, у которых были достигнуты несколько более высокие значения АД при применении других антигипертензивных препаратов (исключая антагонисты ангиотензиновых рецепторов). И, наконец, в исследовании VALUE были рандомизированы более 15 000 больных артериальной гипертензией высокого риска, которым назначали валсартан или амлодипин. В течение 5 лет у больных группы амлодипина АД снизилось в несколько большей степени, чем в группе валсартана. Частота сердечных исходов и смерти (первичная конечная точка) достоверно не отличалась между двумя группами, однако при применении амлодипина отмечено значительное снижение риска инфаркта миокарда и слабое снижение частоты инсульта. С другой стороны, валсартан имел некоторое преимущество по эффективности в профилактике сердечной недостаточности. Объединенные данные продемонстрировали более высокую эффективность антагонистов ангиотензиновых рецепторов в профилактике сердечной недостаточности у больных сахарным диабетом, хотя число наблюдений было небольшим.
Недавно была высказана гипотеза о том, что антагонисты ангиотензиновых рецепторов уступают другим антигипертензивным препаратам по эффективности в профилактике инфаркта миокарда. Однако она не была подтверждена при мета-анализе различных исследований, который продемонстрировал сходное снижение риска инфаркта миокарда при применении этих препаратов. Эффективность антагонистов ангиотензиновых рецепторов и ингибиторов АПФ (т.е. двух классов препаратов, подавляющих активность ренин-ангиотензиновой системы) в профилактике исходов прямо не сравнивалась. В настоящее время продолжается крупное исследование ONTARGET, в котором у пациентов с артериальной гипертензией и нормальным АД, относящихся к группе высокого риска, сравниваются рамиприл и телмисартан. В сравнительных рандомизированных исследованиях у больных сердечной недостаточностьюи пациентов с дисфункцией левогожелудочка после инфаркта миокарда разницы в частоте инсульта, основных коронарных исходов и сердечной недостаточности при лечении ингибиторами АПФ и антагонистами ангиотензивновых рецепторов не выявили. При мета-регрессионном анализе BPLTT недавно было показано, что антагонисты ангиотензиновых рецепторов по профилактической эффективности, опосредованной гипотензивным действием, сопоставимы с ингибиторами АПФ, хотя последние могут давать несколько более выраженный эффект, независимый от изменений АД.
4.4.5. Исследования бета-блокаторов
Польза бета-блокаторов по сравнениюс другими антигипертензивными средствами была недавно подвергнута сомнению на основании результатов двух крупных рандомизированных исследований LIFE и ASCOT, которые продемонстрировали преимущества, соответственно, антагониста ангиотензиновых рецепторов и антагониста кальция перед бета-блокатором по эффективности в профилактике инсульта (LIFE) или инсульта и смертности (ASCOT). Эти два крупных исследования оказали существенное влияние на результаты недавно выполненного мета-анализа, авторы которого пришли к заключению о том, что терапия, начатая с бета-блокатора, менее эффективна в профилактике инсульта, но не инфаркта миокарда или смерти. На основании сходного мета-анализа NICE в Великобритании было рекомендовано применять бета-блокаторы для лечения артериальной гипертензии только в качестве препаратов четвертой линии. К этим выводам следует отнестись серьезно, однако интерпретировать их необходимо критически. Дизайн исследований LIFE и ASCOT предполагал возможность ранней комбинированной терапии, поэтому подавляющее большинство больных, рандомизированных в группу бета-блокатора, фактически получали комбинацию бета-блокатора и тиазидного диуретика. Сходная комбинация часто использовалась в группе хлорталидона в исследовании ALLHAT, которое не подтвердило более низкую ее эффективность в профилактике инсульта. В исследовании INVEST лечение бета-блокатором, к которому в большинстве случаев добавляли тиазидный диуретик, привело к сопоставимому снижению риска любых и определенных сердечно-сосудистых исходов по сравнению с группой пациентов, которым назначали верапамил, а при необходимости присоединяли трандолаприл. И, наконец, недавно выполненный мета-анализ показал, что по сравнению с плацебо терапия бета-блокаторами значительно снижает риск развития инсульта. Это свидетельствует о том, что меньшая эффективность бета-блокатора/тиазидного диуретика в исследовании ASCOT, по крайней мере, частично объясняется менее значительным снижением АД (особенно центрального) в этой группе.
Комбинированная терапия бета-блокатором и тиазидным диуретиком сопровождается метаболическими нарушениями и развитием сахарного диабета (раздел 4.5.5) и может быть противопоказанной больным, склонным к его развитию. В любом случае, результаты мета-анализов клинических исследований бета-блокаторов иллюстрируют сложности, которые возникают при изучении возможных благоприятных или необлагоприятных эффектов антигипертензивных препаратов у пациентов, получающих комбинированную терапию.
4.4.6. Заключение
Результаты сравнительных рандомизированных исследований показали, что при сопоставимом снижении АД разница в сердечно-сосудистой заболеваемости и смертности у больных, получающих антигипертензивные препараты разных классов, невелика. Это свидетельствует о том, что польза лечения в значительной степени определяется снижением АД как таковым. В некоторых исследованиях степень снижения АД отличалась в группах сравнения, что послужило основанием для проведения мета-регрессионного анализа, который позволяет учесть разницу достигнутого АД.
Несмотря на некоторые ограничения подобного подхода, полученные данные подтвердили важность снижения АД для профилактики неблагоприятных исходов, за исключением сердечной недостаточности: при снижении систолического АД на 10 мм рт. ст. независимо от выбранной терапии отмечалось значительное снижение риска развития как инсульта, так и коронарных осложнений. Результаты мета-регрессионных анализов также показали, что некоторые антигипертензивные препараты могут оказывать благоприятное влияние на риск определенных исходов независимо от снижения АД (т.е. разница в частоте осложнений отмечалась при сопоставимых значениях АД). Этот эффект определенно меньше (5-10%) основного профилактического эффекта, опосредованного снижением АД. С другой стороны, результаты отдельных исследований и их мета-анализов показали, что антагонисты кальция уступают диуретикам/ бета-блокаторам, ингибиторам АПФ и антагонистам ангиотензиновых рецепторов по эффективности в профилактике развития сердечной недостаточности (независимо от возможной разницы гипотензивного действия). Высказывалось мнение о том, что диагностировать сердечную недостаточность трудно, а при лечении антагонистами кальция возникают дополнительные сложности, связанные с появлением отеков на фоне вазодилатации. Кроме того, диуретики, возможно, не предупреждают развитие сердечной недостаточности, а просто маскируют ее симптомы. В связи с этим, в некоторых последних исследованиях, таких как VALUE, в качестве конечной точки анализировали только случаи госпитализации по поводу сердечной недостаточности. Полученные данные убедительно подтвердили ограниченную эффективность антагонистов кальция в профилактике этого состояния по сравнению с антагонистом ангиотензиновых рецепторов. Можно предположить, что для профилактики сердечной недостаточности большое значение имеют гуморальные эффекты, которые существенно отличаются у препаратов разных классов.Однако даже в этом случае сам факт снижения АД играет ключевую роль, так как в исследовании ACTION у больных ИБС, страдавших артериальной гипертензией, снижение АД на 14,6/7,6 мм рт. ст. при применении нифедипина пролонгированное действие сопровождалось снижением частоты госпитализаций по поводу сердечной недостаточности на 38% по сравнению с плацебо.
4.5. Рандомизированные исследования с промежуточными конечными точками
Возможные различия в благоприятных эффектах антигипертензивных препаратов разных классов следует изучать не только в отношении основных сердечно-сосудистых исходов. Бессимптомное поражение органов-мишеней наблюдается на более раннем этапе сердечно-сосудистого континуума и может оказаться более чувствительным к действию определенных антигипертензивных средств. В связи с этим ниже обсуждаются результаты исследований, в которых конечными точками служило бессимптомное поражение органов-мишеней.
4.5.1. Сердце
Во многих исследованиях изучали влияние различных антигипертензивных препаратов на гипертрофию левого желудочка, ассоциирующуюся с артериальной гипертензией. В большинстве случаев ее оценивали с помощью эхокардиографии, хотя только в некоторых исследованиях использовались достаточно надежные критерии. У пациентов с артериальной гипертензией и гипертрофией левого желудочка невозможно применение плацебо. Необходимыми условиями сравнительных исследований являются следующие:
2) длительность лечения должна составлять, по крайнеймере, 9-12мес.;
3) снижение АД должно быть сопоставимым в группах сравнения;
4) необходимо принять меры, чтобы избежать регрессии к среднему и систематической ошибки при интерпретации эхокардиограмм, если они не анализируются в слепой последовательности.
Учитывая ограничения многих исследований, мета-анализ не позволяет однозначно судить о преимуществах препаратов определенных классов.
Более надежная информация была получена в ряде крупных исследований, имевших адекватный дизайн. Три из них показали сопоставимый регресс гипертрофии при лечении ингибиторами АПФ (лизиноприлом, эналаприлом и фозиноприлом, соответственно) и антагонистами кальция (амлодипином, нифедипином и амлодипином, соответственно). В одном исследовании масса левого желудочка уменьшилась в равной степени при лечении антагонистом ангиотензиновых рецепторов кандесартаном и ингибитором АПФ эналаприлом, а в другом исследовании были получены сходные результаты при лечении антагонистом кальция лацидипином и бета-блокатором атенололом. В нескольких исследованиях наблюдалось более выраженное уменьшение массы миокарда при лечении несколькими антагонистами ангиотензиновых рецепторов (валсартаном, ирбесартаном, лозартаном) по сравнениюс бета-блокатором (во всех случаях атенолол). В исследовании LIFE у 960 больных лозартан превосходил атенолол по степени регресса гипертрофии левого желудочка. В двух крупных исследованиях сравнивали фиксированную комбинацию ингибитора АПФ и диуретика (периндоприла/ индапамида) с бета-блокатором атенололом или ингибитором АПФ эналаприлом, однако более значительное снижение массы миокарда на фоне комбинированной терапии ассоциировалось с более выраженным снижением АД и коррелировало с более значительным уменьшением центрального АД. Дополнительная информация была получена в двух исследованиях, в которых массу миокарда измеряли с помощью магнитно-резонансной томографии. В достаточно крупном исследовании блокатор альдостероновых рецепторов эплеренон и ингибитор АПФ эналаприл характеризовались сходной эффективностью, а их комбинация давала более выраженный эффект, чем оба препарата по отдельности (однако на фоне более значительного снижения АД). В меньшем по объему исследовании при сравнении антагониста ангиотензиновых рецепторов телмисартана с бета-блокатором карведилолом, обладающим альфа-блокирующими свойствами, первый давал более выраженный эффект при сходном снижении среднесуточного АД.
В целом, результаты клинических исследований свидетельствуют о том, что снижение АД, независимо от препарата конкретного класса или схемы комбинированной терапии, сопровождается регрессом гипертрофии левогожелудочка. Продемонстрирована сопоставимая эффективность ингибиторов АПФ, антагонистов ангиотензиновых рецепторов, антагонистов кальция и, возможно, антагонистов альдостерона, в то время как антагонисты рецепторов ангиотензина пре-восходили бета-блокаторы. В исследовании установлена эффективность диуретика индапамида, который имел преимущества перед ингибитором АПФ эналаприлом. Однако эта работа оказалась единственным исследованием, в котором ингибитор АПФ не вызывал уменьшения массы левогожелудочка, что не позволяет судить о сравнительной эффективности диуретиков и ингибиторов АПФ.
В двух длительных исследованиях недавно было показано, что регресс гипертрофии левогожелудочка является стойким, но достигает максимума через 2-3 г. В крупном исследовании LIFE было установлено, что снижение массы миокарда под влиянием антигипертензивной терапии сопровождается снижением риска основных сердечно-сосудистых исходов, инсульта, сердечно-сосудистой и общей смертности, что подтверждает результаты других длительных наблюдений.
Благодаря появлению неинвазивных методов оценки фиброза миокарда повысился интерес к изучению фиброзного компонента гипертрофии левогожелудочка. При ретроспективном анализе двух рандомизированных контролируемых исследований, в которых изучался регресс гипертрофии левогожелудочка, было показано, что лозартан по влиянию на эхогенность миокарда (показатель фиброза) значительно превосходит атенолол, а кандесартан по эффективности сопоставим с ингибитором АПФ эналаприлом. При изучении биохимических показателей фиброза (пропептид или проколлагены I и III типов) было отмечено уменьшение содержания коллагена при лечении лозартаном, но не атенололом, хотя этот результат не был подтвержден в другом исследовании. В двух сравнительных исследованиях уровни натрийуретических пептидов снизились при лечении лозартаном и увеличились при применении атенолола, что указывало на противоположное влияние двух препаратов на податливость левого желудочка.
Подтверждением разницы эффектов антигипертензивных препаратов на гипертрофию левогожелудочка могут также служить электрокардиографические исследования. В исследовании LIFE лозартан достоверно превосходил атенолол по влиянию на ЭКГ-признаки гипертрофии левого желудочка. Сходный результат был получен при анализе результатов эхокардиографии в том же исследовании. Уменьшение ЭКГ-признаков гипертрофии левого желудочка ассоциировалось с достоверным снижением сердечно-сосудистой заболеваемости и смертности. В двух небольших исследованиях другой антагонист ангиотензиновых рецепторов ирбесартан по эффективности превосходил атенолол, а эналаприл имел преимущества перед антагонистом кальция нисольдипином.
Значительно меньше исследованы сравнительные эффекты разных антигипертензивных препаратов на диастолические нарушения, которые часто встречаются у больных артериальной гипертензией и обычно (но не всегда) сочетаются с гипертрофией левого желудочка. В двух исследованиях было выявлено большее уменьшение массы левогожелудочка при лечении антагонистами ангиотензиновых рецепторов (лозартаном, ирбесартаном) по сравнению с атенололом, однако в обоих случаях не отмечено существенной разницы в ЭхоКГ-показателях диастолической функции между двумя группами. Следует отметить, что диастолическая дисфункция не служила критерием включения в эти исследования. В настоящее время проводятся крупные исследования, в которых первичной конечной точкой является диастолическая дисфункция левого желудочка.
В последние годы внимание исследователей было привлечено к дилатации левого предсердия, которая коррелирует с гипертрофией левого желудочка и является фактором риска сердечно-сосудистых исходов. Накапливаются также данные о том, что антигипертензивные препараты могут оказывать разное влияние на риск развития фибрилляции предсердий. В двух крупных исследованиях было показано, что лечение антагонистами ангиотензиновых рецепторов лозартаном и валсартаном сопровождалось снижением частоты впервые выявленной фибрилляции предсердий по сравнениюс терапией бета-блокатором атенололом и антагонистом кальция амлодипином. Снижение частоты фибрилляции предсердий было также отмечено в трех исследованиях у больных с сердечной недостаточностью, в которых сравнивали эналаприл или антагонисты ангиотензиновых рецепторов кандесартан и валсартан с плацебо. В исследовании LIFE снижение частоты фибрилляции предсердий коррелировало с регрессом гипертрофии левого желудочка. В небольших по объему исследованиях изучалось влияние антагонистов ангиотензиновых рецепторов на частоту рецидивов фибрилляции предсердий. Эти исследования продемонстрировали благоприятные эффекты ирбесартана по сравнению с плацебо и лозартана по сравнению с амлодипином; препараты в обоих случаях добавляли к амиодарону. Таким образом, эффективность антагонистов ангиотензиновых рецепторов убедительно доказана по отношению к профилактике первых пароксизмов фибрилляции предсердий и менее убедительно – к профилактике повторных приступов (по сравнению с бета-блокаторами, антагонистами кальция или плацебо). Антагонисты ангиотензиновых рецепторов и ингибиторы АПФ прямо не сравнивались. Дополнительная информация может быть получена в продолжающихся специальных исследованиях.
4.5.2. Стенка артерий и атеросклероз
Мета-анализ рандомизированных исследований, в которых конечной точкой была толщина комплекса интима-медиа сонных артерий, представляет трудную задачу, учитывая значительные различия между исследованиями. Некоторые из них не обладали статистической силой, необходимой для выявления небольших различий, в других отсутствовал внутренний контроль, который позволяет избежать системной ошибки при интерпретации данных и регрессии к среднему. И, наконец, исследования, в которых изучали состояние общей сонной артерии (показатель гипертрофии стенки сосудов), трудно объединять с исследованиями, в которых использовали комбинированную конечную точку, отражающую также состояние бифуркации и/или внутренней сонной артерии (более надежный показатель атеросклероза).
При изучении толщины комплекса интима-медиа общей сонной артерии в трех плацебоконтролируемых исследованиях не удалось подтвердить преимущества ингибиторов АПФ или бета-блокатора. В сравнительных исследованиях ингибитор АПФ не отличался от тиазидного диуретика, тогда как антагонисты кальция превосходили тиазиды, бета-блокатор и ингибитор АПФ. Таким образом, имеющиеся данные свидетельствуют о том, что антагонисты кальция оказывают более выраженное влияние на утолщение (предположительно гипертрофию) стенки сонных артерий, связанное с артериальной гипертензией, чем другие антигипертензивные средства.
При оценке толщины комплекса интима-медиа бифуркации и/или внутренней сонной артерии (более информативный показатель атеросклероза) в плацебоконтролируемых исследованиях продемонстрирована эффективность антагониста кальция, ингибитора АПФ и бета-блокатора, что, возможно, отражает антиатеросклеротический эффект снижения АД. При сравнении различных схем антигипертензивной терапии, обеспечивавших сопоставимое снижение АД, установлена более высокая эффективность антагонистов кальция по сравнениюс гидрохлортиазидом, хлорталидоном и атенололом. В последнем исследовании была также показана более высокая эффективность ингибитора АПФ по сравнению с тиазидным диуретиком. В исследовании ELSA было также обнаружено, что замедленное утолщение стенки сонных артерий при лечении лацидипином по сравнению с атенололом сопровождается меньшим увеличением и более значительным снижением числа бляшек. Однако при изучении состава стенки сонной артерии по ее эхогенности не было выявлено разницы между лацидипином и атенололом. В целом, полученные данные свидетельствуют о том, что снижение АД позволяет задержать прогрессирование каротидного атеросклероза. При этом антагонисты кальция по эффективности превосходят диуретики и бета-блокаторы, а ингибиторы АПФ более эффективны, чем диуретики.
Хотя скорость пульсовой волны признана информативным методом оценки растяжимости стенок крупных артерий, однако влияние антигипертензивной терапии как таковой и различных антигипертензивных препаратов на этот параметр практически не изучено. Многие исследования были небольшими и нерандомизированными, поэтому трудно судить о том, были ли изменения скорости пульсовой волны(т.е.жесткости) следствием снижения АД, особых свойств использованных препаратов или регрессии к средней.
Результаты ряда небольших плацебоконтролируемых и сравнительно непродолжительных (несколько недель) исследований свидетельствуют о том, что некоторые антигипертензивные агенты на самом деле снижают скорость пульсовой волны, однако ее снижение могло быть также следствием гипотензивного действия препаратов. В пользу этого вывода говорят результаты исследования, в котором сравнивали эффективность более и менее агрессивной антигипертензивной терапии. Значительное снижение скорости пульсовой волны выявили только у пациентов, получавших более интенсивное лечение. Вопрос о том, отличаются ли препараты разных классов по этому эффекту, остается открытым. Результаты 4-х сравнительных исследований оказались противоречивыми, что, возможно, отражает недостаточную статистическую силу каждого из них.
4.5.3. Головной мозг и когнитивная функция
В некоторых рандомизированных исследованиях в качестве конечных точек изучали поражение головного мозга и когнитивную дисфункцию. В рамках исследования PROGRESS оценивали влияние снижения АД на прогрессирование поражения белого вещества головного мозга (с помощью МРТ). Общий объем новых очаговых изменений значительно снизился в группе больных, у которых лечение периндоприлом и индапамидом привело к снижению АД на 11/4 мм рт. ст. по сравнению с плацебо.
Недавно был выполнен мета-анализ исследований, в которых изучалось влияние антигипертензивной терапии на когнитивную функцию. В трех исследованиях у 13 143 больных ее оценивали с помощью шкалы Mini Mental State Evaluation. Авторы выявили небольшое, но значительное улучшение когнитивной функции при разнице АД по сравнениюс группой плацебо в 4,8/2,6 мм рт. ст. В 5-ти исследованиях у 717 больных снижение АД в среднем на 3,2/1,5 мм рт. ст. по сравнению с плацебо сопровождалось улучшением результата теста на логическую память. С другой стороны, в 4-х рандомизированных исследованиях у 2 396 пациентов снижение АД в среднем на 17,1/7,0 мм рт. ст. ассоциировалось с небольшим, но достоверным ухудшением теста на образное восприятие и логическое мышление. Таким образом, создается впечатление, что лечение артериальной гипертензии приводит к улучшению результатов скрининговых тестов на деменцию и память, что дополнительно подтверждает благоприятное влияние антигипертензивной терапии на цереброваскулярную заболеваемость. Однако результаты других тестов не улучшились при снижении АД. Можно предположить, что антигипертензивная терапия по-разному влияет на различные когнитивные функции. Следует отметить, что в исследованиях, которые не подтвердили благоприятный эффект лечения на обучение, отмечалось значительно более выраженное снижение АД, что не позволяет исключить J-образный эффект.
Наконец, во многих исследованиях сравнивали эффекты активных антигипертензивных эффектов и плацебо, в то время как число сравнительных исследований было небольшим. Следовательно, более выраженное влияние того или иного класса антигипертензивных средств на когнитивную функцию убедительно не доказано. Однако необходимо отметить, что в единственном плацебоконтролируемом исследовании, в котором наблюдалось значительное снижение частоты развития деменции, применялся антагонист кальция нитрендипин.
4.5.4. Функция и поражение почек
В многочисленных рандомизированных исследованиях изучались эффекты антигипертензивной терапии на различные показатели функции почек (микроальбуминурию и протеинурию, скорость клубочковой фильтрации и частоту терминальной болезни почек) при различных состояниях – в том числе сахарном диабете, диабетической нефропатии, недиабетической нефропатии или эссенциальной гипертензии. Учитывая неоднородность перечисленных состояний, конечных точек, а также разницу в размерах выборок и статистической силе исследований, возможность объединения их результатов вызывает сомнения. Более адекватным представляется критический обзор имеющихся данных.
Основной вопрос заключается в том, позволяет ли более выраженное снижение АД (до 130/80 мм рт. ст., а не 140/90 мм рт. ст.) лучше сохранить функцию почек у больных с нефропатией. Хотя более низкие целевые значения АД рекомендуются во всех руководствах, необходимо признать, что этот вопрос недостаточно изучен в рандомизированных клинических исследованиях. Доказательством, в основном, служат результаты исследования MDRD, которое продемонстрировало значительное уменьшение частоты развития терминальной болезни почек у больных, страдавших, в основном, недиабетической нефропатией, при снижении среднего АД до менее 92 мм рт. ст. (т.е. ниже 120/80 мм рт. ст.) против 107 мм рт. ст. в группе сравнения (т.е. ниже 140/90 мм рт. ст.).Однако в других исследованиях у больных недиабетической или диабетической нефропатией снижение АД до более низких целевых значений не позволило добиться более выраженного нефропротективного эффекта. В одном исследовании у больных сахарным диабетом и нормотонией снижение АД до менее 120/80 мм рт. ст. под действием валсартана не привело к более значительному улучшению клиренса креатинина по сравнению с таковым при менее интенсивной антигипертензивной терапии (АД несколько выше 120/80 мм рт. ст.). Тем не менее, агрессивная терапия оказывала благоприятное влияние на экскрецию белка с мочой. В другом исследовании у больных недиабетической нефропатией более значительное снижение АД при присоединении антагониста кальция к ингибитору АПФ не привело к дополнительному снижению частоты терминальной болезни почек и протеинурии. Тем не менее, положительные результаты MDRD подтверждаются данными, полученными в исследовании IDNT и 11-ти исследованиях у больных недиабетической нефропатией, показавшими возможнуюпользу снижения систолического АД, по крайней мере, до 120 мм рт. ст. Наконец, споры по поводу целевых значений АД, необходимых для сохранения функции почек у больных сахарным диабетом, могут быть неоправданными, учитывая доказанную пользу более интенсивной антигипертензивной терапии у таких пациентов (целевое АД менее 130/80 мм рт. ст.) в отношении профилактики сердечно-сосудистых осложнений.
В большом числе рандомизированных исследований изучались нефропротективные свойства антигипертензивных препаратов, в основном ингибиторов АПФ и антагонистов ангиотензивноых рецепторов. В нескольких плацебоконтролируемых исследованиях было показано, что антагонисты ангиотензиновых рецепторов, ингибиторы АПФ или комбинация низкой дозы ингибитора АПФ с диуретиком задерживают развитие терминальной болезни почек и повышение уровня креатинина в сыворотке и уменьшают или предупреждают микроальбуминурию или протеинурию у больных с диабетической и недиабетической нефропатиями. Продемонстрирован антипротеинурический эффект спиронолактона по сравнению с плацебо. Во всех других плацебоконтролируемых исследованиях (за исключением одного) нефропротективные эффекты препаратов ассоциировались с несколько более выраженным снижением АД, которое могло, по крайней мере частично, объяснять улучшение функции почек. В исследовании SYST-EUR лечение антагонистом кальция нитрендипином также оказывало нефропротективное действие по сравнению с плацебо.
Результаты сравнительных исследований различных схем антигипертензивной терапии оказались менее однозначными. В двух исследованиях (в одно включали больных с диабетической протеинурией, в другое – с недиабетической нефропатией) было продемонстрировано преимущество антагониста ангиотензиновых рецепторов или ингибитора АПФ перед антагонистом кальция в профилактике развития терминальной болезни почек или удвоения уровня креатинина в сыворотке. Тем не менее, при ретроспективном анализе результатов исследования ALLHAT у больных артериальной гипертензией и сниженной функцией почек (сведения о наличии протеинурии отсутствовали) частота этих конечных точек оказалась сходной при лечении диуретиком, антагонистом кальция или ингибитором АПФ. Результаты исследований, в которых изучалась скорость клубочковой фильтрации, также были неоднозначными: только в одном исследовании степень ее снижения при лечении ингибитором АПФ была меньшей, чем при применении бета-блокатора или антагониста кальция; другие исследования не позволили выявить разницу между ингибиторами АПФ и антагонистом кальция, бета-блокатором, антагонистом ангиотензиновых рецепторов, антагонистом кальция/диуретиком. В одном исследовании продемонстрированы сходные эффекты антагониста кальция и диуретика.
Более четкие результаты были получены при изучении влияния различных антигипертензивных средств на микроальбуминурию и протеинурию. Антагонисты ангиотензиновых рецепторов снижали экскрецию белка с мочой более эффективно, чем бета-блокатор, антагонист кальция или тиазидный диуретик. Антагонист альдостерона и ингибитор АПФ по эффективности превосходили антагонисты кальция. Тем не менее, в трех исследованиях ингибиторы АПФ по антипротеинурическому действия были сопоставимы с антагонистами кальция, а в одном исследовании не отличались от диуретика.
Представляют интерес несколько исследований, в которых изучалась комбинированная терапия антагонистом ангиотензиновых рецепторов и ингибитором АПФ(по сравнению с монотерапией). В исследовании COOPERATE было отмечено замедление прогрессирования недиабетической нефропатии на фоне комбинированной терапии по сравнению с монотерапией, несмотря на отсутствие разницы АД между группами. Однако в других исследованиях более выраженный антипротеинурический эффект комбинированной терапии ассоциировался с более значительным снижением АД. Если титрование дозы ингибитора АПФ обеспечивало сопоставимое с комбинированной терапией снижение АД, то антипротеинурический эффект двух схем терапии не различался. При мета-анализе клинических исследований было подтверждено более выраженное антипротеинурическое действие комбинированной терапии, которое сочеталось с более значительным снижением АД. С другой стороны, два небольших исследования свидетельствуют о том, что антагонисты ангиотензиновых рецепторов в очень больших дозах могут давать более значительный антипротеинурический эффект по сравнению со стандартными дозами, несмотря на отсутствие дополнительного снижения АД. Полученные данные необходимо подтвердить в более крупных исследованиях.
4.5.5. Развитие сахарного диабета
Сахарный диабет и артериальная гипертензия часто сочетаются друг с другом. Подобное сочетание приводит к тяжелым последствиям. Некоторые антигипертензивные средства оказывают нежелательное влияние на метаболизм, поэтому в ряде клинических исследований изучалась (часто ретроспективно) частота развития сахарного диабета. Практически во всех исследованиях у больных, получавших диуретики и/или бета-блокаторы, она была выше, чем при лечении ингибиторами АПФ, антагонистами ангиотензиновых рецепторов или антагонистами кальциями. Недавно было показано, что терапия антагонистами ангиотензиновых рецепторов и ингибиторами АПФ ассоциируется с меньшей частотой развития сахарного диабета, чем лечение антагонистами кальция. Остается неясным, обладают ли блокаторы ренин-ангиотензиновой системы истинным антидиабетогенным эффектом или просто лишены диабетогенной активности, характерной для бета-блокаторов и диуретиков и – в меньшей степени – для антагонистов кальция. В единственном плацебоконтролируемом исследовании, в котором оценивалась частота развития сахарного диабета (SHEP), она была выше у больных, получавших активную терапию (диуретиком и часто бета-блокатором). Сходные данные были получены в исследовании MRC у пожилых людей. По данным мета-анализа, сахарный диабет в группе плацебо развивался реже, чем при лечении диуретиком или бета-блокатором. В других плацебоконтролируемых исследованиях у пациентов группы высокого сердечно-сосудистого риска или с сердечной недостаточностью также было продемонстрировано снижение частоты развития сахарного диабета при лечении ингибиторами АПФ или антагонистами ангиотензиновых рецепторов по сравнению с плацебо, однако во всех этих исследованиях плацебо (а также активный препарат) присоединяли к многокомпонентной терапии различными препаратами, среди которых преобладали диуретики и бета-блокаторы. Тоже самое затрудняет интерпретацию отрицательного результата исследования DREAM, в котором терапия рамиприлом у пациентов с нарушенной толерантностьюк глюкозе не привела к снижению частоты развития сахарного диабета по сравнению с плацебо. Почти половина больных в этом исследовании страдала артериальной гипертензией, а одна треть – дислипидемией. Многие из них получали различные антигипертензивные средства и гиполипидемические препараты. При мета-анализе 22-х исследований, включавших более 160 000 больных, было показано, что ассоциация между антигипертензивной терапией и развитием сахарного диабета самая низкая при лечении антагонистами ангиотензиновых рецепторов и ингибиторами АПФ. За ними следовали антагонисты кальция, бета-блокаторы и диуретики.
Высказано предположение, что лекарственный сахарный диабет по прогнозу отличается от «спонтанного». Так, в контролируемых исследованиях развитие сахарного диабета не сопровождалось увеличением риска сердечно-сосудистых исходов по сравнениюс пациентами, у которых диабет отсутствовал. Однако известно, что сердечно-сосудистые осложнения развиваются более чем через 10 лет после установления диагноза сахарного диабета; указанный срок превышает возможную длительность контролируемых рандомизированных исследований. Более длительные (16-30 лет) наблюдения продемонстрировали значительное увеличение частоты сердечно-сосудистых осложнений у больных, у которых развивался сахарный диабет при лечении антигипертензивными средствами (преимущественно диуретиками и/или бета-блокаторами). Заметным исключением являются результаты14-летнего исследования SHEP. У пациентов с вновь развившимся сахарным диабетом (на фоне приема хлорталидона±атенолола) не было отмечено увеличения смертности. Ограничение указанных длительных исследований заключается в том, что в них не оценивали микрососудистые осложнения, которые тесно связаны с гипергликемией. Кроме того, они были неконтролируемыми, что не позволяло исключить роль дополнительных факторов. В связи с этим сегодня нельзя подтвердить или опровергнуть гипотезу о том, что лекарственные и «спонтанный» сахарный диабет отличаются по прогнозу. При отсутствии убедительных данных увеличение частоты сахарного диабета при лечении некоторыми антигипертензивными препаратами вызывает определенные опасения, которые нельзя игнорировать.
5. Подходы к лечению артериальной гипертензии
5.1. Когда начинать антигипертензивную терапию
Решение о назначении антигипертензивной терапии принимают на основании двух критериев:
2) уровня сердечно-сосудистого риска (рис. 2).
Все больные, у которых при повторном измеренииАД диагностируют АГ 2-й или 3-й степени, нуждаются в антигипертензивной терапии, так как (на это указывается в рекомендациях ESH/ESC 2003 г) в большом числе плацебоконтролируемых исследований было убедительно доказано, что она значительно снижает частоту сердечно-сосудистых осложнений, в том числе смертельных, независимо от уровня общего риска (средний, высокий или очень высокий). Польза лечения АГ 1-й степени убедительно не доказана, так как этот вопрос специально не изучался. Однако в исследовании FEVER было показано, что снижение систолического АД до менее 140 мм рт.ст. дает протективный эффект даже у пациентов группы среднего риска. Эти данные позволяют рекомендовать антигипертензивную терапию больным с систолическим АД ≥140 мм рт.ст.
Сразу после установления диагноза АГ любой степени целесообразно рекомендовать модификацию образа жизни, тогда как решение о сроках назначения медикаментозной терапии принимают с учетом общего сердечно-сосудистого риска. В исследовании VALUE у больных АГ высокого риска несколько более поздний контроль АД ассоциировался с тенденцией к увеличению риска сердечно-сосудистых исходов. В исследовании ASCOT у больных АГ (в сочетании с дополнительными факторами риска общий сердечно-сосудистый риск был ниже, чем в VALUE) благоприятный эффект улучшенного контроля АД проявлялся в течение первых нескольких месяцев. В связи с этим оценивать результаты модификации образа жизни следует быстрее, чем рекомендовалось ранее (рис. 2). Медикаментозную терапию следует начинать немедленно у больных АГ 3-й степени, а также пациентов с АГ 1-й и 2-й степени при наличии высокого или очень высокого сердечно-сосудистого риска. У больных АГ 1-й и 2-й степени, относящихся к группе среднего риска, медикаментозная терапия может быть отложена на несколько недель, а у больных АГ 1-й степени при отсутствии других факторов риска (низкий добавочный риск) – на несколько месяцев. Однако если не удается добиться контроля АД, то даже в этих случаях необходимо начинать фармакотерапию.
Если АД является высоким нормальным (130-139/89 мм рт. ст.), то решение о назначении антигипертензивной терапии в значительной степени зависит от уровня сердечно-сосудистого риска. В рандомизированных исследованиях было показано, что у больных сахарным диабетом, цереброваскулярной болезнью, ИБС и атеросклерозом периферических артерий она вызывает снижение риска фатальных и нефатальных сердечно-сосудистых осложнений, хотя в двух других исследованиях у пациентов с ИБС польза снижения АД не была подтверждена или снижение сердечно-сосудистого риска отмечалось только при наличии повышенного АД. У больных сахарным диабетом и альбуминурией снижение АД до очень низких значений (<125/75 мм рт. ст.) сопровождалось уменьшением микроальбуминурии или протеинурии (которые являются предикторами ухудшения функции почек и сердечно-сосудистых осложнений), а также уменьшением скорости нарастания протеинурии. Сходные результаты были также получены у больных с исходным АД менее 140/90 мм рт. ст., которые получали препараты, оказывающие прямое антипротеинурическое действие, – такие как блокаторы ренин-ангиотензиновой системы. Это позволяет рекомендовать антигипертензивную терапию (в сочетании с интенсивной модификацией образа жизни) даже пациентам с высоким нормальным (а иногда и нормальным) АД, если у них имеются сердечно-сосудистые заболевания или сахарный диабет.
| Артериальное давление, мм рт. ст. | |||||
| Другие факторы риска, органы-мишени или заболевания | Нормальное САД 120-129 или ДАД 80-84 | Высокое нормальное САД 130-39 или ДАД 85-89 | АГ 1-й степени САД 140-159 или ДАД 90-99 | АГ 2-й степени САД 160-179 или ДАД 100-109 | АГ 3-й степени САД≥180 или ДАД≥110 |
| Нет других факторов риска | Снижение АД не требуется | Модификация образа жизни; если через несколько месяцев АД не контролируется, медикаментозная терапия | Модификация образа жизни + немедленная медикаментозная терапия | ||
| 1-2 фактора риска | Модификация образа жизни | ||||
| ≥3 факторов риска, метаболический синдром или поражение органов-мишеней | Модификация образа жизни | Модификация образа жизни; обсудить медикаментозную терапию | Модификация образа жизни + медикаментозная терапия |
||
| Сахарный диабет | Модификация образа жизни + медикаментозная терапия |
||||
| Сердечно-сосудистые заболевания или нефропатия | Модификация образа жизни + немедленная медикаментозная терапия | ||||
Рисунок 2. Назначение антигипертензивной терапии
Польза интенсивной модификации образа жизни в сочетании с применением антигипертензивных средств у пациентов с высоким нормальным АД, относящихся к группе высокого риска (наличие, по крайней мере, трех дополнительных факторов риска, метаболического синдрома или поражения органов-мишеней), не доказана. Следует подчеркнуть, что в проспективных исследованиях у пациентов с высоким нормальным АД частота сердечно-сосудистых заболеваний была выше, чем у людей с нормальным или оптимальным АД. Кроме того, у первых была выше вероятность развития АГ, которая часто ассоциируется с другими факторами риска и метаболическим синдромом. Наконец, применение антигипертензивных средств позволяет на некоторое время задержать формирование АГ. В то же время в исследовании DREAM лечение рамиприлом у пациентов с метаболическими нарушениями (и высоким нормальным АД или АГ 1-й и 2-й степени) не позволило задержать развитие сахарного диабета или снизить частоту сердечно-сосудистых исходов, несмотря на снижение АД. К сожалению, исследование DREAM не обладало статистической силой, необходимой для изучения сердечно-сосудистых исходов, поэтому этот важный вопрос нуждается в дополнительных исследованиях. В настоящее время пациентам с высоким сердечно-сосудистым риском (не страдающим сахарным диабетом) и высоким нормальным АД необходимо рекомендовать интенсивную модификацию образа жизни (включая прекращение курения) и регулярное измерение АД, учитывая высокую вероятность развития АГ. Однако врачи и пациенты иногда предпочитают применение антигипертензивных средств, особенно более эффективно предупреждающих поражение органов-мишеней и развитие АГ и сахарного диабета. Модификация образажизни и контроль АД показаны пациентам с нормальным АД, относящимся к группам низкого и среднего добавочного риска.
5.2. Цели лечения
Первичной цельюлечения АГ является максимальное снижение суммарного риска сердечно-сосудистых осложнений и смерти. Для этого необходимо контролировать все модифицируемые факторы риска, включая курение, дислипидемию, абдоминальное ожирение и сахарный диабет, а также проводить лечение сопутствующих заболеваний и самой АГ.
| Рамка 8. Цели лечения |
|---|
|
5.2.1. Целевое АД в общей популяции больных АГ
В рекомендациях ESH/ESC 2003 г. было предложено снижать АД до 140/90 мм рт. ст. у всех больных АГ; при этом было отмечено, что польза снижения АД до таких значений была доказана только у больных сахарным диабетом или сердечно-сосудистыми заболеваниями, а также при ретроспективном анализе результатов исследования HOT. В последнем частота неблагоприятных исходов была самой низкой при уровнях АД около 138/83 мм рт. ст. Дополнительные данные, подтверждающие пользу снижения АД до <140 мм рт. ст., были получены при ретроспективном анализе результатов исследований VALUE и INVEST. В исследовании VALUE «контроль» АД у больных АГ (< 140/90ммрт.ст.) сопровождался значительным снижением частоты инсульта, инфаркта миокарда, сердечной недостаточности, а также сердечно-сосудистой заболеваемости и смертности по сравнению с таковой у больных с неконтролируемой АГ, несмотря на антигипертензивную терапию. В исследовании INVEST также было отмечено снижение риска нефатальных ифатальных сердечно-сосудистых исходов у пациентов с контролируемой АГ. Эти результаты согласуются с данными клинической практики. Снижение АД до <140/90 мм рт.ст. ассоциировалось со значительным снижением сердечно-сосудистой заболеваемости и смертности по сравнению с таковыми у пациентов с неконтролируемой гипертензией. Очевидно, что интерпретировать результаты, которые были получены в нерандомизированных исследованиях, следует осторожно. Однако следует отметить, что целесообразность снижения АД до <140/90 мм рт. ст. была недавно прямо подтверждена в исследовании FEVER, в котором снижение АД до 138,1/82,3 мм рт. ст. на фоне активной антигипертензивной терапии привело к снижению риска инсульта, коронарных исходов и сердечно-сосудистой смертности на 28% по сравнению с таковым у пациентов группы плацебо, у которых АД оставалось на уровне 141,6/83,9 мм рт.ст.
Существуют также аргументы в пользу снижения АД до более низких значений (менее 140/90 ммрт.ст.), близких к нормальным, если они хорошо переносятся больными.
2) Исследования продемонстрировали прямую линейную связь между сердечно-сосудистым риском и систолическим и диастолическим АД, достигавшими 115-110 и 75-70 мм рт. ст., соответственно, без признаков J-образногофеномена.
3) Более значительное снижение АД в результате антигипертензивной терапии может способствовать улучшению протективного эффекта у пациентов с более высоким риском (см. ниже).
5.2.2. Целевые значения АД у больных сахарным диабетом и пациентов очень высокого и высокого риска
Чтобы обеспечить максимальный протективный эффект в отношении сердечно-сосудистой системы, больным сахарным диабетом рекомендуется проводить более интенсивную антигипертензивную терапию и снижать АД до целевого значения <130/80 мм рт. ст. В исследованиях HOT и UKPDS было убедительно доказано, что у больных сахарным диабетом 2-го типа более значительное снижение АД ассоциируется с дополнительным уменьшением риска развития макро- и микрососудистых осложнений. Это было подтверждено в исследованиях ABCD. Недавно при мета-анализе клинических исследований у больных сахарным диабетом было продемонстрировано снижение риска сердечно-сосудистых исходов (особенно инсульта) при более интенсивном лечении по сравнению с менее интенсивным (разница систолического и диастолического АД между группами составила в среднем 6,0 и 4,6 мм рт. ст., соответственно). Тем не менее, польза более жесткого контроля АД (<130/80ммрт. ст.) доказана менее убедительно. В нескольких рандомизированных исследованиях показана польза снижения диастолического АД до примерно 80 мм рт. ст. и даже ниже, однако имеется очень мало данных, подтверждающих благоприятный эффект снижения систолического АД до менее 130 мм рт. ст. Однако в исследованиях ABCD у пациентов с сахарным диабетом и высоким или нормальным АД снижение систолического АД до 132 и 128 мм рт. ст. сопровождалось уменьшением частоты неблагоприятных исходов (общей смертности и инсульта, соответственно) по сравнению с таковой в группах больных, у которых контроль АД был менее жестким (систолическое АД 138 и 137 мм рт. ст., соответственно). Кроме того, в рамках исследования UKPDS была выявлена тесная связь между динамикой систолического АД и частотой макро- и микрососудистых осложнений у больных сахарным диабетом; увеличение риска осложнений наблюдалось при значениях систолического АД более 120 мм рт. ст.
Данные в пользу более низких целевых уровней АДу больных с высоким сердечно-сосудистым риском в отсутствие сахарного диабета менее постоянны. Наиболее четко установлена польза интенсивной антигипертензивной терапии у больных, перенесших инсульт или транзиторную ишемическую атаку, так как в исследовании PROGRESS у пациентов с цереброваскулярными заболеваниями снижение АД со 147/86 до 138/82 мм рт. ст. привело к снижению риска повторного инсульта и основных сердечно-сосудистых исходов, соответственно, на 28% и 26% по сравнению с пациентами группы плацебо, у которых АД изменилось незначительно. Снижение сердечно-сосудистого риска было также отмечено у пациентов с нормальным АД, у которых во время лечения оно снизилось до 127/75 мм рт.ст. Недавно при ретроспективном анализе результатов исследования PROGRESS было выявлено снижение частоты повторного инсульта (особенно геморрагического) при уменьшении систолического АД примерно до 120ммрт. ст. Польза более жесткого контроля АД в других группах высокого риска доказана менее убедительно. По данным ретроспективного анализа результатов исследования HOT, более значительное снижение диастолического и систолического АД (82 против 85 мм рт. ст. и 142-145 против 145-148 мм рт.ст.) ассоциировалось с более выраженным профилактическим эффектом у пациентов высокого и очень высокого сердечно-сосудистого риска (50% выборки HOT), но не у пациентов более низкого риска. В плацебоконтролируемых исследованиях у больных, перенесших инфаркт миокарда, лечение бета-блокаторами или ингибиторами АПФ привело к снижению частоты повторного инфаркта миокарда и смерти, даже при нормальном АД. Считалось, что эти препараты сами по себе обладают протективной активностью, поэтому снижение АД редко расценивалось как причина улучшения прогноза. В тех случаях, когда авторы указывали значения АД, в основной группе оно было ниже, чем в группе плацебо. Как указано в разделе 5.1, большинство плацебоконтролируемых исследований у больных стенокардией илиИБС подтвердило снижение риска сердечно-сосудистых исходов при более низких значениях АД (EUROPA: 128/78 против 133/80 мм рт.ст.; ACTION у больных АГ: 137/77 против 144/81 мм рт.ст.; CAMELOT: 124/76 против 130/77 мм рт.ст.), хотя в другом исследовании у больных стенокардией сходные целевые значения АД (129/74 против 132/76 мм рт. ст.) не позволили добиться дополнительного эффекта.
Польза снижения АД до более низких целевых значений у пациентов с недиабетической нефропатией (с точки зрения профилактики сердечно-сосудистых исходов) убедительно не доказана, однако установлено, что снижение АД до менее 130/80 мм рт. ст. помогает сохранить функцию почек, особенно при наличии протеинурии (раздел 4.5.4).
5.2.3. Целевые значения домашнего и амбулаторного АД
Накапливаются данные, подтверждающие прогностическое значение результатов измерения АД в домашних условиях и при суточном мониторировании, поэтому эти методы все чаще используются для оценки эффективности лечения. При сходных офисных показателях АД более низкие значения среднесуточного АД ассоциируются со снижением частоты сердечно-сосудистых исходов.Однако оптимальные целевые показатели АД, измеренного в домашних условиях и при суточном мониторировании, пока не установлены. При использовании этих двух методов значения АД оцениваются на несколько мм рт. ст. ниже офисных показателей (табл. 5), однако разница пропорциональна значениям последних, т.е. домашнее и среднесуточное АД обычно выше при высоком офисном АД и ниже при более низких значениях офисногоАД. Этот факт, а также более выраженное влияние антигипертензивной терапии на уровни АД, измеренного в клинике, по сравнению со среднесуточным АД, позволяют сделать вывод о том, что оптимальные целевые показатели АД, измеренного в клинике и амбулаторно, существенно не различаются.
5.2.4. Заключение
На основании имеющихся данных, всем больным АГ можно рекомендовать снижение АД, по крайней мере, до 140/90 мм рт. ст. или ниже. Антигипертензивная терапия должна быть более агрессивной у больных сахарным диабетом, у которых целевое АД составляет <130/80 мм рт. ст. Сходными целевые значения АД являются у пациентов с цереброваскулярной болезнью, а также ИБС. При этом риск недостаточной перфузии жизненно важных органов очень низкий, исключая эпизоды ортостатической гипотонии, развития которых следует избегать, особенно у пожилых людей и больных сахарным диабетом. Существование J-образной зависимости между риском неблагоприятных исходов и достигнутым АД подозревали на основании результатов анализа post-hoc, которые демонстрировали увеличение частоты осложнений при достаточно низком диастолическом АД. Полагают, что изгиб кривой происходит при значениях АД, которые значительно ниже целевых показателей при интенсивной антигипертензивной терапии, что было подтверждено в рандомизированных исследованиях у больных инфарктом миокарда в анамнезе и хронической сердечной недостаточностью. У этих пациентов бета-блокаторы и ингибиторы АПФ снижали частоту сердечно-сосудистых исходов, несмотря на дополнительное снижение достаточно низких исходных показателей систолического и диастолического АД.
Следует подчеркнуть, что, несмотря на широкое использование многокомпонентных схем антигипертензивной терапии, в большинстве исследований достигнутое систолическое АД оставалось выше 140 мм рт.ст. Даже если среднее АД было ниже этого значения, оно было достигнуто максимум у 60-70% больных. У больных сахарным диабетом лечение АГ никогда не приводило к снижению среднего систолического АД менее 130 мм рт.ст, за исключением исследования ABCD, в которое включали пациентов с нормальным или высоким нормальным АД. Таким образом, добиться снижения АД до указанных целевых значений бывает трудно, особенно при более высоком исходном АД, а также у пожилых людей, так как с возрастом систолическое АД в значительной степени зависит от фиброза и ригидности аорты. Исследования свидетельствуют о том, что на фоне комбинированной терапии у больных сахарным диабетом систолическое АД обычно остается несколько выше, чему пациентов без диабета.
5.3. Эффективность затрат на антигипертензивную терапию
В нескольких исследованиях было показано, что у больных высокого или очень высокого риска антигипертензивная терапия характеризуется эффективностью затрат, а снижение сердечно-сосудистой заболеваемости и смертности в значительной степени нивелирует затраты на пожизненную терапию. Польза лечения, вероятно, даже больше, чем можно предсказать на основании числа неблагоприятных исходов, которых удается избежать (число пациентов, которых необходимо пролечить, или NNT).
1) В нескольких плацебоконтролируемых исследованиях значительное число пациентов группы плацебо получали антигипертензивные препараты, а часть больных основной группы фактически прекращали их прием, хотя анализ по группам проводился у всех рандомизированных пациентов (intention-to-treat).
2) В нескольких исследованиях разница между основной группой и группой плацебо продолжала нарастать в течение нескольких лет, что может указывать на более выраженный протективный эффект длительного снижения АД.
3) У молодых людей с АГ низкого риска относительно небольшой эффект, достигнутый в течение 5 лет,может трансформироваться в более значительное увеличение продолжительности жизни по сравнению с пожилыми пациентами группы высокого риска. Это означает, что у молодых людей эпидемиологические исследования позволяют лучше оценить пользу лечения, чем результаты клинических исследований. У молодых пациентов целью лечения является не профилактика маловероятных тяжелых или смертельных исходов в ближайшие несколько лет, а предупреждение развития и/или прогрессирования поражения органов-мишеней, которое, в конечном итоге, приводит к переходу от группы низкого риска в группу высокого риска. В нескольких исследованиях, прежде всего HDFP и HOT, было показано, что, несмотря на
интенсивное лечение, частота сердечно-сосудистых исходов у больных АГ высокого риска или осложненной АГ остается значительно выше, чем у пациентов группы низкого или среднего риска.Можно предположить, что добиться модификации высокого сердечно-сосудистого риска бывает трудно, а использование антигипертензивных средств только у пациентов высокого или очень высокого риска не является оптимальной стратегией. Наконец, лечение АГ часто сравнивают с модификацией образа жизни, которая не требует затрат. Однако, чтобы добиться реального изменения образа жизни, необходима помощь специалистов, затраты на которую могут оказаться достаточно значительными.
6. Стратегии лечения
6.1. Модификация образа жизни
Модификация образажизни показана всем больным, в том числе пациентам с высоким нормальным АД и пациентам, нуждающимся в медикаментозной антигипертензивной терапии. Цели улучшения образа жизни включают в себя снижение АД, контроль других факторов риска и сопутствующих заболеваний, снижение числа и доз антигипертензивных препаратов. К мерам, которые снижают АД и сердечно-сосудистый риск, относят следующие:
1) прекращение курения,
2) снижение массы тела, если она является избыточной;
3) ограничение потребления алкоголя;
4) физическую активность;
5) ограничение потребления соли;
6) увеличение потребления фруктов и овощей и снижение потребления насыщенных жиров и общего потребления жиров.
Необходимо всегда пропагандировать здоровую диету. Однако польза немедикаментозных методов в профилактике сердечно-сосудистых исходов у больных АГ не доказана, а приверженность к ним низкая. Они не должны быть поводом для необоснованной отсрочки медикаментозной терапии, особенно у пациентов более высокого риска.
| Рамка 9. Модификация образа жизни |
|---|
– прекращение курения;
– снижение и стабилизация массы тела; – ограничение потребления алкоголя; – физические нагрузки; – ограничение потребления соли; – увеличение количества фруктов и овощей в диете и снижение потребления насыщенных жиров и общего количества жиров.
|
6.1.1. Прекращение курения
Курение вызывает острое повышение АД и ЧСС, которое сохраняется в течение более 15 мин после одной выкуренной сигареты. Возможным механизмом считают стимуляцию симпатической нервной системы, что сопровождается выбросом катехоламинов в плазму. Как это ни парадоксально, в нескольких эпидемиологических исследованиях АД у курильщиков было сходным с таковым у некурящих или даже ниже. Однако с помощью амбулаторного мониторирования АД было показано, что у нелеченых курильщиков с АГ и нормальным АД среднесуточные значения его выше, чему некурящих; разница была особенно значительной у пациентов, выкуривавших большое число сигарет за день. Курение позволяло также предсказать повышение систолического АД в будущем, хотя его независимое влияние на АД не было подтверждено, а прекращение курения не приводит к снижению АД.
Курение является мощным сердечно-сосудистым фактором риска, а прекращение курения, по-видимому, считают самым эффективным методом профилактики большого числа сердечно-сосудистых заболеваний, включая инсульт и инфаркт миокарда. В пользу этого свидетельствует тот факт, что у людей, бросивших курить в молодом возрасте, продолжительность жизни сходна с таковой у людей, которые никогда не курили. В связи с этим курящим больным АГ необходимо рекомендовать бросить курить.
При необходимости могут быть назначены никотинсодержащие средства или бупропион. Варенициклин – новый селективный частичный агонист никотиновых ацетилхолиновых рецепторов, эффективность которого была подтверждена в плацебоконтролируемых исследованиях. Пассивное курение также увеличивает риск ИБС и заболеваний. Благодаря принятым мерам в последние годы воздействие пассивного курения снизилось. Желательно, чтобы эти меры были приняты во всех странах Европы.
6.1.2. Умеренное употребление алкоголя
Во многих исследованиях продемонстрирована U- или J-образная связь между смертностью и употреблением алкоголя. Небольшое или умеренное употребление алкоголя сопровождается снижением смертности, тогда как злоупотребление алкоголем увеличивает смертность. Однако такая зависимость недавно было подвергнута сомнению на основании мета-анализа имеющихся данных. Связь между употреблением алкоголя, уровнями АД и распространенностью АГ в популяции является линейной. Кроме того, злоупотребление алкоголем сопровождается высоким риском инсульта, особенно при так называемом «кутежном» пьянстве. Алкоголь ухудшает эффективность антигипертензивной терапии, однако при сокращении его употребления этот эффект нивелируется в течение 1-2 нед примерно на 80%. У людей, злоупотребляющих алкоголем, возможно повышение АД после резкого прекращения приема алкоголя. У них чаще диагностируют АГ в начале недели, если они употребляют алкоголь, в основном, в выходные дни. Ограничение потребления алкоголя в клинических исследованиях приводило к значительному снижению систолического и диастолического АД. Мужчинам с АГ следует рекомендовать ограничить употребление алкоголя до 20-30 г этанола в день, а женщинам – до не более 10-20 г этанола в день. Их следует предупредить о повышении риска инсульта при «кутежном» пьянстве.
6.1.3. Ограничение потребления соли
Эпидемиологические исследования свидетельствуют о том, что потребление поваренной соли с пищей способствует повышению АД и увеличению распространенности АГ. В рандомизированных контролируемых исследованиях у больных АГ ограничение потребления натрия на 80-100 ммоль (4,7-5,8 г натрия хлорида) в день от исходного потребления 180 ммоль (10,5 г) приводило к снижению АД в среднем на 4-6 мм рт.ст., хотя этот эффект очень варьировал. Антигипертензивный эффект ограничения потребления натрия позволяет уменьшить дозы и число антигипертензивных препаратов, необходимых для контроля АД. Влияние низкосолевой диеты на АД сильнее выражено у афроамериканцев, людей среднего и пожилого возраста, а также больных АГ, сахарным диабетом и хроническими заболеваниями почек, т.е. в группах пациентов, у которых понижен ответ ренин-ангиотензин-альдостероновой системы. Активация последней в сочетании с усилением активности симпатической нервной системы нивелирует гипотензивное действие ограничения потребления соли.
Пациентам следует рекомендовать избегать подсаливания пищи и потребления соленых продуктов. Целесообразно также увеличение потребления натуральных продуктов, содержащих больше калия. Чрезмерное потребление соли может быть причиной резистентной АГ. Рекомендуемое потребление натрия было недавно снижено со 100 до 65 ммоль/сут, что соответствует 3,8 г натрия хлорида. Добиться этой цели бывает трудно. Более реально снижение потребления натрия хлорида до 5 г/сут (85 ммоль/сут).
6.1.4. Другие изменения диеты
В последнее десятилетие было показано, что увеличение потребления калия, а также фруктов, овощей и нежирных молочных продуктов в сочетании с ограничением потребления холестерина, насыщенных жиров и общего количества жиров также вызывают снижение АД. В нескольких небольших клинических исследованиях и при их мета-анализе было установлено, что омега-3 полиненасыщенные жирные кислоты в высоких дозах (рыбий жир) могут снизить АД у больных АГ, хотя их гипотензивное действие обычно проявляется только при назначении достаточно высоких доз (≥3 г/сут). У пациентов с АГ АД снижалось в среднем на 4,0/2,5 мм рт. ст. Имеющиеся данные не позволяют рекомендовать увеличение потребления клетчатки с целью снижения АД. Высказано предположение, что потребление кальция и магния также способствует снижению АД, однако эта гипотеза нуждается в дополнительной проверке, как и роль других специальных диет, предполагающих модификациюсодержания углеводов. Больным АГ следует рекомендовать есть больше фруктов и овощей (4-5 порций или 300 г овощей в день), больше рыбы и ограничить потребление насыщенных жиров и холестерина. Может быть полезной консультация квалифицированного диетолога.
6.1.5. Снижение массы тела
Установлена прямая связь между массой тела и АД. Ожирение предрасполагает к повышению АД и развитию АГ. Доказано также, что похудание приводит к снижению АД у больных ожирением и благоприятно влияет на другие факторы риска (инсулинорезистентность, сахарный диабет, гиперлипидемия, гипертрофия левогожелудочка и обструктивное апноэ во сне).По данным мета-анализа, снижение массы тела в среднем на 5,1 кг ассоциировалось со снижением АД на 4,4/3,6 мм рт. ст. Степень снижения АД была сходной у пациентов с нормальным АД и АГ, но оказалась более значительной при более выраженном похудании. В клинических исследованиях подтверждено более значительное снижение АД при большем снижении массы тела. Умеренное похудание в сочетании с ограничением потребления натрия или без него позволяет предупредить развитие АГ у пациентов с избыточной массой тела и высоким нормальным АД, а также дает возможность уменьшить число антигипертензивных препаратов и облегчает их отмену. У людей среднего возраста масса тела постепенно увеличивается (на 0,5-1,5 кг/год); поэтому полезной целью может быть стабилизация массы тела.
6.1.6. Физические нагрузки
Недостаточная физическая активность – мощный предиктор сердечно-сосудистой смертности, который не зависит от АДи других факторов риска. Недавно при мета-анализе рандомизированных контролируемых исследований было установлено, что динамические аэробные физические нагрузки снижают АД на 3,0/2,4 мм рт. ст., а среднедневное АД – на 3,3/3,5 мм рт. ст. Снижение АД в покое у больных АГ было более выраженным (на 6,9/4,9 мм рт. ст.), чем у пациентов с нормальным АД (на 1,9/1,6 мм рт. ст.). Даже умеренные нагрузки снижали АД, а также массу тела, количество жировой ткани и окружность талии, и увеличивали чувствительность к инсулину и уровни холестерина ЛПВП. Таким образом, людям, ведущим малоподвижный образ жизни, рекомендуются регулярные умеренные физические нагрузки, например, по 30-45мин в день (ходьба, бег трусцой, плавание). Объем исследований до начала программы тренировок зависит от уровня предполагаемой физической нагрузки, наличия симптомов, общего сердечно-сосудистого риска, сопутствующих заболеваний. Интенсивные изометрические нагрузки, например подъем тяжестей, могут вызвать значительное повышение АД, поэтому их следует избегать. Если АГ плохо контролируется, то лучше избегать тяжелых физических нагрузок,а также выполнений пробы с максимальной нагрузкой. Они могут быть отложены до тех пор, пока антигипертензивная терапия позволит снизить АД.
6.2. Фармакотерапия
| Рамка 10. Выбор антигипертензивных препаратов |
|---|
1. предыдущий позитивный или негативный опыт применения препаратов соответствующего класса;
2. влияние антигипертензивных средств на сердечно-сосудистые факторы риска у конкретного больного; 3. наличие бессимптомного поражения органов-мишеней, сердечно-сосудистых заболеваний, нефропатии или сахарного диабета может быть основанием для выбора определенных антигипертензивных средств (рамка 11 и табл. 6); 4. наличие других состояний может препятствовать назначению ряда антигипертензивных препаратов (табл. 7); 5. возможность взаимодействия с другими лекарственными средствами, которые используются для лечения сопутствующих заболеваний; 6. затраты на лечение как для пациента, так и организации здравоохранения, хотя стоимость не может иметь преимущества перед эффективностью и переносимостью.
|
| Рамка 11. Предпочтительные антигипертензивные средства | |
|---|---|
| Бессимптомное поражение органов-мишеней | |
| Гипертрофия левого желудочка | Ингибиторы АПФ, антагонисты кальция, АРА |
| Бессимптомный атеросклероз | Антагонисты кальция, ингибиторы АПФ |
| Микроальбуминурия | Ингибиторы АПФ, АРА |
| Нарушение функции почек | Ингибиторы АПФ, АРА |
| Сердечно-сосудистые заболевания | |
| Перенесенный инсульт | Любой антигипертензивный препарат |
| Перенесенный инфаркт миокарда | Бета-блокаторы, ингибиторы АПФ, АРА |
| Стенокардия | Бета-блокаторы, антагонисты кальция |
| Сердечная недостаточность | Диуретики, бета-блокаторы, ингибиторы АПФ, АРА, антагонисты альдостерона |
| Фибрилляция предсердий | |
| Пароксизмальная | АРА, ингибиторы АПФ |
| Постоянная | Бета-блокаторы, недигидропиридиновые антагонисты кальция |
| Терминальная нефропатия/ протеинурия | Ингибиторы АПФ, АРА, петлевые диуретики |
| Атеросклероз периферических артерий | Антагонисты кальция |
| Другие состояния | |
| Изолированная систолическая гипертензия (пожилые) | Диуретики, антагонисты кальция |
| Метаболический синдром | Ингибиторы АПФ, АРА, антагонисты кальция |
| Сахарный диабет | Ингибиторы АПФ, АРА |
| Беременность | Антагонисты кальция, метилдопа, бета-блокаторы |
| Афроамериканцы | Диуретики, антагонисты кальция |
| АРА – антагонисты рецепторов ангиотензина II | |
6.2.1. Выбор антигипертензивного препарата
Большое число рандомизированных исследований, в которых антигипертензивные препараты сравнивали с плацебо или друг с другом, подтверждают выводы, сделанные в рекомендациях ESH/ESC 2003 г.:
1) основные благоприятные эффекты антигипертензивной терапии, в основном, являются следствием снижения АД как такового и мало зависят от выбора препаратов;
2) тиазидные диуретики (а также хлорталидон и индапамид), бета-блокаторы, антагонисты кальция, ингибиторы АПФ и антагонисты ангиотензиновых рецепторов вызывают адекватное снижение АД и значительное снижение риска неблагоприятных сердечно-сосудистых исходов. Соответственно, все эти препараты подходят для стартовой и поддерживающей антигипертензивной терапии и могут применяться как по отдельности, так и в комбинации друг с другом.Препараты перечисленных классов имеют определенные особенности, преимущества и недостатки, которые обсуждаются ниже и позволяют врачу подобрать наиболее адекватную схему антигипертензивной терапии в каждом конкретном случае.
В двух крупных исследованиях и недавно выполненном мета-анализе было показано, что бета-блокаторы уступают другим препаратам по эффективности в отношение профилактики инсульта, но не в отношение профилактики коронарных осложнений и смерти. Польза бета-блокаторов доказана у больных стенокардией, сердечной недостаточностью и перенесенным инфарктом миокарда, которые часто сочетаются с АГ. В связи с этим бета-блокаторы по-прежнему могут рассматриваться как средства первой и второй линии в лечении АГ. Бета-блокаторы способствуют увеличению массы тела, оказывают нежелательное влияние на обмен липидов и повышают (по сравнению с другими препаратами) частоту развития сахарного диабета, поэтому с них не следует начинать лечение больных АГ с множественными метаболическими факторами риска, включая метаболический синдром и его основные компоненты (абдоминальное ожирение, высокая нормальная или нарушенная гликемия натощак, нарушенная толератность к глюкозе), которые повышают риск диабета. Это касается также тиазидных диуретиков, которые в высоких дозах ухудшают липидный обмен и оказывают диабетогенное действие. В исследованиях, продемонстрировавших увеличение частоты развития сахарного диабета, тиазиды часто применяли с бета-блокаторами, что затрудняет оценку вклада препаратов двух групп. Указанные недостатки могут не распространяться на бета-блокаторы, обладающие вазодилатирующими свойствами (карведилол и небиволол), которые в меньшей степени влияют на метаболизм или не оказывают на него действия, а также реже вызывают диабет, чем классические бета-блокаторы. Бета-блокаторы, ингибиторы АПФ и антагонисты ангиотензиновых рецепторов менее эффективны у афроамериканцев, которым в первую очередь следует назначать диуретики и антагонисты кальция.
| Тиазидные диуретики | Изолированная систолическая гипертензия (пожилые) Сердечная недостаточность Афроамериканцы |
| Бета-блокаторы | Стенокардия Перенесенный инфаркт Сердечная недостаточность Тахиаритмии Глаукома Беременность |
| Антагонисты кальция (дигидропиридины) |
Изолированная систолическая гипертензия (пожилые) Стенокардия Гипертрофия левого желудочка Каротидный/ коронарный атеросклероз Беременность Афроамериканцы |
| Антагонисты кальция (верапамил/дилтиазем) |
Стенокардия Каротидный атеросклероз Суправентрикулярная тахикардия |
| Ингибиторы АПФ | Сердечная недостаточность Дисфункция ЛЖ Перенесенный инфаркт Диабетическая нефропатия Недиабетическая нефропатия Гипертрофия ЛЖ Каротидный атеросклероз Протеинурия/ микроальбуминурия Фибрилляция предсердий Метаболический синдром |
Антагонисты ангиотензиновых рецепторов |
Сердечная недостаточность Перенесенный инфаркт Диабетическая нефропатия Протеинурия/ микроальбуминурия Гипертрофия ЛЖ Фибрилляция предсердий Метаболический синдром Кашель, вызванный ингибиторами АПФ |
| Диуретики (антагонисты альдостерона) |
Сердечная недостаточность Перенесенный инфаркт |
| Петлевые диуретики | Терминальная нефропатия Сердечная недостаточность |
Исследования, в которых изучалось влияние антигипертензивной терапии на бессимптомное поражение органов-мишеней, продемонстрировали различия определенных препаратов: ингибиторы АПФ и антагонисты кальция более эффективно снижали гипертрофию левого желудочка, включая фиброзный ее компонент; кроме того, они достаточно эффективно уменьшали микроальбуминурию и протеинурию, сохраняли функцию почек и задерживали прогрессирование нефропатии; антагонисты кальция не только вызывают регресс гипертрофии левого желудочка, но и замедляют прогрессирование гипертрофии стенки и атеросклероза сонных артерий.
Данные о благоприятных эффектах антигипертензивных препаратов других классов более ограниченны. Альфа1-адреноблокаторы, препараты центрального действия (агонисты альфа2-адренорецепторов и модуляторы имидазолиновых рецепторов) адекватно снижали АД и оказывали благоприятное влияние на обмен веществ. Продемонстрировано также антигипертензивное действие антагонистов альдостерона. Единственное крупное исследование, в котором изучался альфа1-адреноблокатор (доксазозин в ALLHAT), было прекращено раньше срока, поэтому благоприятные или неблагоприятные эффекты препаратов этой группы в лечении АГ остаются недоказанными. То же касается препаратов центрального действия и антагонистов альдостерона. Однако все эти средства часто использовали в комбинации с другими антигипертензивными препаратами в клинических исследованиях, которые подтвердили их протективное влияние на сердечно-сосудистую систему. Соответственно, они могут использоваться в качестве компонента комбинированной терапии. Альфа1-адреноблокаторы показаны при наличии доброкачественной гиперплазии предстательной железы. Алискирен – новый препарат, препятствующий активации рениновой системы. Он зарегистрирован в США и вскоре должен появиться в Европе. Этот препарат эффективно снижал АД у больных АГ как в виде монотерапии, так и в комбинации с тиазидным диуретиком. В доклинических исследованиях он оказывал также антипротеинурическое действие. Высказано предположение, что ренин может обладать эффектами, не связанными с классическим ренин-ангиотензиновым каскадом, а его прогностическое значение может не зависеть от продукции ангиотензина II, хотя это пока не доказано. Сведений об эффективности препарата в профилактике неблагоприятных сердечно-сосудистых исходов также нет.
На протяжении многих лет дискутируется вопрос о том, какие антигипертензивные препараты следует считать средствами первой линии.Однако в клинических исследованиях было доказано, что для контроля АД большинству больных требуется комбинированная терапия. Если пациенты должны на протяжении всей жизни принимать, по крайней мере, два антигипертензивных препарата, то вопрос о том, какой из них предпочтительно применять в первые несколько недель терапии, имеет второстепенное значение.Однако препараты разных классов (и даже в рамках одного класса) отличаются по типам и частоте побочных эффектов; некоторые пациенты могут быть склонными к развитию определенных нежелательных реакций. Кроме того, антигипертензивные средства могут оказывать разное влияние на факторы риска, поражение органов-мишеней, риск определенных неблагоприятных исходов или различаются по эффективности в определенных группах пациентов. В связи с этим подбирать антигипертензивные препараты и их комбинации следует индивидуально. При их выборе необходимо учитывать следующие факторы:
1) предыдущий позитивный или негативный опыт применения препаратов соответствующего класса;
2) влияние антигипертензивных средств на сердечно-сосудистые факторы риска, имеющиеся у конкретного больного;
3) наличие бессимптомного поражения органов-мишеней, сердечно-сосудистых заболеваний, нефропатии или сахарного диабета;
4) наличие других состояний;
5) возможность взаимодействия с другими лекарственными средствами, которые используются для лечения сопутствующих заболеваний;
6) затраты на лечение как для пациента, так и организации здравоохранения, хотя стоимость не должна иметь преимущества перед эффективностью и переносимостью. Врачи должны отдавать предпочтение антигипертензивным препаратам, которые оказывают длительное действие и могут быть использованы один раз в день. Упрощение схемы антигипертензивной терапии способствует повышению приверженности лечению, в то время как круглосуточный контроль АД имеет важное дополнительное прогностическое значение. Длительно действующие средства дают более постоянный антигипертензивный эффект в течение суток, что позволяет свести к минимуму вариабельность АД.
Критерии, перечисленные в этом разделе, позволяют во многих случаях подобрать определенные препараты или комбинации. Состояния, которые могут служить доводом в пользу назначения различных агентов или противопоказаниями к их применению, перечислены в табл. 6 и 7 и в рамке 11, а подходы к лечению пациентов с различными состояниями подробнее обсуждаются в разделе 7.
| Абсолютные | Возможные | |
|---|---|---|
| Тиазидные диуретики | Подагра | Метаболический синдром Нарушение толерантности к глюкозе Беременность |
| Бета-блокаторы | Астма Атрио-вентрикулярная блокада II-III степени Поражение периферических артерий |
Метаболический синдром Нарушение толерантности к глюкозе Спортсмены и физически активные люди Хроническая обструктивная болезнь легких |
| Антагонисты кальция (дигидропиридины) |
Тахиаритмии Сердечная недостаточность |
|
| Антагонисты кальция (верапамил и дилтиазем) |
Атрио-вентрикулярная блокада II-III степени Сердечная недостаточность |
|
| Ингибиторы АПФ | Беременность Ангионевротический отек Гиперкалиемия Двусторонний стеноз почечных артерий |
|
| Антагонисты рецепторов ангиотензина | Беременность Гиперкалиемия Двусторонний стеноз почечных артерий |
|
| Диуретики (антагонисты альдостерона) | Почечная недостаточность Гиперкалиемия |
При выборе стартовой и последующей антигипертензивной терапии следует уделять особое внимание нежелательным эффектам, даже субъективным, так как они являются главной причиной низкой приверженности лечению. Полностью избежать нежелательных реакций невозможно, так как они частично имеют психологическую природу и отмечаются даже при приеме плацебо. Однако необходимо стараться ограничить лекарственные побочные эффекты и сохранить качество жизни путем замены антигипертензивных препаратов или отказа от необоснованного увеличения их доз. Побочные эффекты тиазидных диуретиков, бета-блокаторов и антагонистов кальция зависят от дозы (в отличие от антагонистов ангиотензиновых рецепторов и ингибиторов АПФ).
6.2.2. Монотерапия
| Рамка 12. Монотерапия или комбинированная терапия |
|---|
|
Лечение можно начать с одного препарата, который назначают в низкой дозе. Если АД не контролируется, то можно использовать первый препарат в полной дозе или заменить его на препарат другого класса (который также назначают в низкой, а затем в полной дозе). Замена препарата является обязательной, если он не снижает АД или вызывает серьезные побочные эффекты. Такая последовательная монотерапия позволяет подобрать антигипертензивную терапию, которая характеризуется оптимальными эффективностью и безопасностью у конкретного больного. Однако, хотя частота ответа на монотерапию (снижение систолического и диастолического АД, по крайней мере, на 20 и 10 мм рт.ст., соответственно) любым антигипертензивным препаратом составляет примерно 50%, тем не менее, вероятность достижения целевого значения АД (менее 140/90 мм рт. ст.) не превышает 20-30% (за исключением пациентов с АГ 1-й степени). Кроме того, подбор оптимальной монотерапии является трудоемким как для врачей, так и пациентов, что приводит к снижению приверженности лечению и задерживает достижение контроля АД, который имеет особенно большое значение для пациентов высокого риска. Определенные надежды возлагаются на фармакогеномику, которая в будущем, возможно, позволит идентифицировать препараты, способные обеспечить максимальный эффект у конкретных пациентов. Целесообразно продолжение исследований в этой области.
6.2.3. Комбинированная терапия
В большинстве клинических исследований для снижения АД до целевых значений использовали комбинацию, по крайней мере, двух антигипертензивных препаратов. Комбинированная терапия еще чаще требуется больным сахарным диабетом, заболеванием почек, пациентам группы высокого риска, а также в любых ситуациях, когда врач старается снизить АД до более низких значений. Например, недавно в крупном исследовании около 90% больных АГ высокого риска получали, по крайней мере, два антигипертензивных препарата, чтобы добиться снижения АД до <140/90 мм рт. ст.
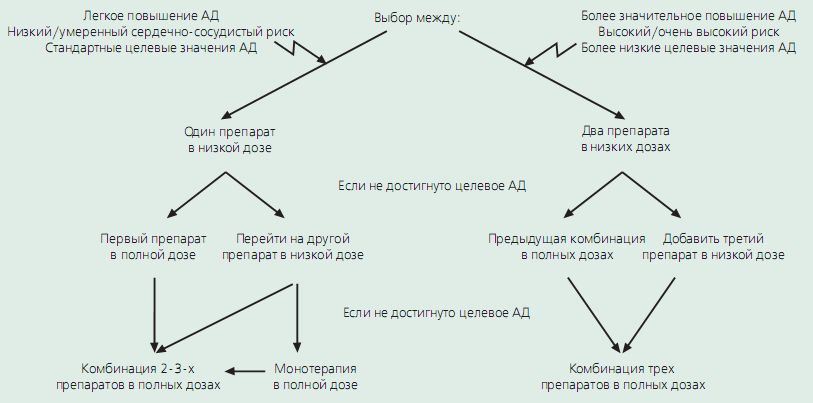
В рекомендациях ESH/ESC 2003 г. было указано, что комбинация двух антигипертензивных препаратов может служить не только необходимым этапом после попытки монотерапии, но и альтернативой последней уже на первом этапе лечения (рис. 3). Очевидный недостаток стартовой комбинированной терапии двумя препаратами заключается в том, что один из них может оказаться ненужным. Однако комбинированная терапия имеет следующие преимущества:
1) два препарата могут быть использованы в низких дозах, что снижает риск побочных эффектов по сравнению с лечением одним препаратом в полной дозе;
2) комбинированная терапия позволяет избежать безуспешных попыток выбора эффективной монотерапии у пациентов с очень высоким АД или поражением органов-мишеней;
3) существуют фиксированные комбинированные препараты, применение которых дает возможность упростить терапию и повысить приверженность;
4) комбинированная терапия позволяет быстрее достичь целевых значений АД, чем монотерапия. Это может иметь очень важное значение для пациентов высокого риска, так как в исследовании VALUE более выраженное снижение АД в группе амлодипина по сравнениюс валсартаном (на 3,8/2,2 мм рт. ст.) уже в течение первых 6 мес сопровождалось более низкой частотой сердечно-сосудистых исходов. Начинать лечение с комбинации антигипертензивных средств следует, в первую очередь, у пациентов высокого сердечно-сосудистого риска, т.е. при наличии значительного повышения АД (более 20/10 мм рт. ст. по сравнению с пороговым значением) или более легкой гипертензии, сочетающейся с множественными факторами риска, бессимптомным поражением органов мишеней, сахарным диабетом, нефропатией или ассоциированными сердечно-сосудистыми заболеваниями. Во всех этих случаях необходимо добиться более значительного снижения АД, которого трудно достичь при монотерапии.
Антигипертензивные препараты разных классов можно сочетать друг с другом, если
1) они имеют разные и взаимодополняющие механизмы действия;
2) доказано, что комбинация по эффективности превосходит оба компонента по отдельности;
3) комбинация способствует улучшению переносимости лечения.
Ниже перечислены схемы комбинированной терапии, которые оказались эффективными и хорошо переносимыми и с успехом использовались в рандомзированных клинических исследованиях. Они выделены жирной линией на рис. 4:
- тиазидный диуретик и ингибитор АПФ;
- тиазидный диуретик и антагонист ангиотензиновых рецепторов;
- антагонист кальция и ингибитор АПФ;
- антагонист кальция и антагонист ангиотензиновых рецепторов;
- антагонист кальция и тиазидный диуретик;
- бета-блокатор и антагонист кальция (дигидропиридиновый).
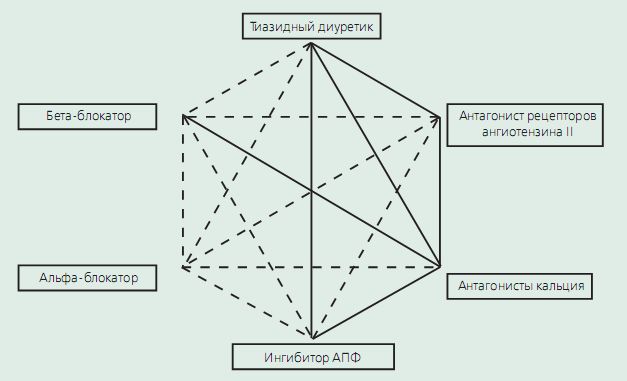
Комбинация тиазидного диуретика и бета-блокатора с успехом использовалась во многих плацебоконтролируемых и сравнительных клинических исследованиях, однако эти препараты оказывают неблагоприятное влияние на метаболизм, которое может оказаться еще более выраженным при их сочетанном применении (разделы 4.4.5 и 4.5.5). Хотя эта схема комбинированной терапии по-прежнему используется, ее следует избегать у пациентов с метаболическим синдромом, а также при наличии высокого риска развития сахарного диабета. Комбинация тиазидного и калийсберегающих диуретиков (амилорида, триамтерена или спиронолактона) широко использовалась для профилактики потери калия при лечении тиазидами, что может способствовать снижению частоты внезапной смерти, предотвращению нарушения толерантности к глюкозе и сахарного диабета, ассоциирующихся с гипокалиемией, вызванной тиазидами. В последние годы изучалась комбинация ингибитора АПФ и антагониста ангиотензиновых рецепторов. Хотя препараты этих двух групп влияют на разные уровни одной и той же системы, их сочетание позволяло добиться более выраженного антипротеинурического эффекта, чем назначение обоих компонентов по отдельности, как при диабетической, так и при недиабетической нефропатии. Кроме того, эта комбинация улучшала выживаемость при сердечной недостаточности. Остается неясным, можно ли воспроизвести преимущества комбинированной терапии путем простого увеличения дозы любого из ее компонентов в случаемонотерапии. Дополнительные сведения о пользе комбинированной терапии антагонистом ангиотензиновых рецепторов и ингибитором АПФ будут получены в исследовании ON-TARGET. Возможны и другие схемы комбинированной терапии, однако они применяются реже, а сведения об их эффективности ограничены.Некоторые из этих комбинаций обозначены пунктирной линией на рис. 4.
Наконец, сегодня выпускаются фиксированные комбинации двух препаратов в одной таблетке, обычно в низких дозах, например, антагонист ангиотензиновых рецепторов с тиазидным диуретиком или антагонистом кальция, ингибитор АПФ с тиазидным диуретиком или антагонистом кальция, бета-блокатор с диуретиком или тиазидный диуретик с калий-сберегающим диуретиком. Хотя фиксированные дозы компонентов ограничивают возможность их титрования, уменьшение числа таблеток, которые вынужден принимать пациент, способствует улучшениюприверженности лечению. Фиксированные комбинированные препараты в низких дозах могут быть использованы на начальном этапе лечения, если врач считает целесообразным назначение двух, а не одного антигипертензивного препарата. Следует подчеркнуть, что комбинированная терапия двумя препаратами не всегда приводит к контролю АД, поэтому некоторым пациентам, особенно страдающим заболеваниями почек и другими формами осложненной гипертензии, могут потребоваться три или четыре препарата. Дополнительная информация о преимуществах такого подхода будет получена после завершения исследования ACCOMPLISH, в котором сравнивается эффективность фиксированных комбинированных препаратов, содержащих ингибитор АПФ с антагонистом кальция или диуретиком, в отношении профилактики сердечно-сосудистой заболеваемости и смертности.
7. Подходы к лечению в особых ситуациях
7.1. Пожилые
У пожилых людей антигипертензивная терапия приводит к снижению сердечно-сосудистой заболеваемости и смертности независимо от типа АГ – систоло-диастолической или изолированной систолической. Это было подтверждено в большом числе рандомизированных исследований, в которые включали пациентов в возрасте 60 – 70 лет и более. При мета-анализе было выявлено снижение риска фатальных и нефатальных сердечно-сосудистых исходов, а также инсульта у пациентов в возрасте старше 80 лет, несмотря на отсутствие снижения общей смертности. Благоприятные эффекты антигипертензивной терапии на заболеваемость, но не смертность больных старческого возраста недавно были подтверждены в пилотном исследовании HYVET.
| Рамка 13. Антигипертензивная терапия у пожилых людей |
|---|
|
В рандомизированных контролируемых исследованиях, продемонстрировавших пользу антигипертензивной терапии по сравнению с плацебо у пожилых больных систоло-диастолической гипертензией, в качестве препаратов первой линии применяли диуретики или бета-блокаторы. Недавно при мета-анализе клинических исследований было высказано предположение, что у пожилых людей бета-блокаторы по эффективности в профилактике сердечно-сосудистых исходов уступают диуретикам, однако многие из этих пациентов получали диуретики в сочетании с бета-блокаторами. У больных изолированной систолической гипертензией в качестве препаратов первой линии применяли диуретики или дигидропиридиновые антагонисты кальция. С антагонистов кальция лечение начинали в двух китайских исследованиях у больных систоло-диастолической или изолированной систолической гипертензией. Во всех этих исследованиях активные препараты превосходили плацебо или контроль (отсутствие лечения). В ряде исследований сравнивали «новые» препараты со «старыми». В исследовании STOP-2 частота сердечно-сосудистых исходов была сходной у пожилых больных АГ, получавших антагонист кальция, ингибитор АПФ или стандартную терапию диуретиком и бета-блокатором, а в исследовании ALLHAT терапия диуретиком, антагонистом кальция или ингибитором АПФ оказывала сопоставимое влияние на риск сердечно-сосудистых осложнений у больных старше 65 лет. В исследовании LIFE у больных 55-80 лет с АГ и гипертрофией левого желудочка антагонист ангиотензиновых рецепторов лозартан снижал риск сердечно-сосудистых исходов, особенно инсульта, более эффективно, чем бета-блокатор атенолол; сходные данные были получены у больных изолированной систолической гипертензией. Исследование SCOPE продемонстрировало снижение риска инсульта у больных АГ в возрасте 70 лет и старше, получавших антагонист ангиотензиновых рецепторов кандесартан (по сравнению с группой пациентов, у которых антигипертензивная терапия не предполагала применение последнего). У больных изолированной систолической гипертензией риск инсульта при лечении кандесартаном снизился на 42%. Таким образом, у пожилых больных АГ продемонстрирована польза применения, по крайней мере, одного представителя нескольких классов – диуретиков, бета-блокаторов, антагонистов кальция, ингибиторов АПФ и антагонистов ангиотензиновых рецепторов. В связи с этим нет достаточных оснований для выбора антигипертензивных препаратов с учетом возраста.
Начинать антигипертензивнуютерапиюу пожилых людей следует в соответствии с общими рекомендациями. До и во время лечения АД целесообразно измерять в положениях сидя и стоя, так как и без того высокий риск ортостатической гипотонии у пожилых может еще более повыситься под влиянием антигипертензивных препаратов. У пожилых людей факторы риска, поражение органов-мишеней, сердечно-сосудистые и другие сопутствующие состояния встречаются чаще, чем у молодых людей. В связи с этим подбирать антигипертензивные препараты следует индивидуально. Многим больным для контроля АД требуется применение двух или более препаратов, так как у пожилых людей бывает особенно трудно добиться снижения систолического АД до 140 мм рт. ст. и менее.
Оптимальное диастолическое АД, которого следует добиваться при проведении лечения, остается неясным. При анализе результатов исследования SHEP изучалась роль диастолического АД на фоне лечения больных изолированной систолической гипертензией. Авторы сделали вывод о том, что снижение диастолического АД до менее 70 мм рт. ст., и особенно менее 60 мм рт. ст., указывает на высокий риск неблагоприятных исходов. Это может быть следствием слишком активной терапии.Однако в исследовании Syst-Eur не было выявлено неблагоприятных последствий снижения диастолического АД до 55 мм рт.ст. (данных о более низких значениях было недостаточно), за исключением пациентов с ИБС в анамнезе. В том же исследовании низкое диастолическое АД ассоциировалось с повышенной несердечно-сосудистой смертностью и в группе плацебо, т.е. последнее не было связано с избыточным лечением. При мета-анализе результатов лечения нескольких тысяч больных были отмечены более высокая сердечно-сосудистая и несердечно-сосудистая смертность при снижении диастолического и систолического АД до менее 60 и 120 мм рт.ст., соответственно. Таким образом, исходный высокий риск может быть причиной чрезмерного снижения АД во время лечения, а не наоборот. Необходимы дополнительные исследования для изучения безопасных значений АД у пожилых людей, прежде всего – диастолического, что позволит обеспечить оптимальный контроль изолированной систолической гипертензии.
7.2. Сахарный диабет
Выделяют два типа сахарного диабета. Диабет 1-го типа развивается в молодом возрасте и характеризуется деструкцией бета-клеток и абсолютной недостаточностью инсулина, тогда как диабет 2-го типа чаще встречается у людей среднего и пожилого возраста и обусловлен ухудшением транспорта глюкозы через мембраны клеток поперечно-полосатых мышц под действием инсулина, хотя может наблюдаться и снижение секреции инсулина. Сахарный диабет 2-го типа встречается в 10-20 раз чаще инсулинозависимого диабета 1-го типа. Частота АГ у таких больных достигает 70-80%.
Сочетание сахарного диабета любого типа иА Г значительно увеличивает риск поражения почек и других органов-мишеней и сопровождается значительно более высокой частотой инсульта, ИБС, сердечной недостаточности, поражения периферических артерий и сердечно-сосудистой смертности. Как указано в разделе 3.6.3, микроальбуминурия является ранним маркером нефропатии и сердечно-сосудистым фактором риска. Сведения об эффективности антигипертензивной терапии в отношении профилактики сердечно-сосудистых исходов у больных сахарным диабетом 1-го типа ограниченны, однако имеются данные о том, что стандартная терапия и лечение ингибиторамиАПФ задерживают прогрессирование нефропатии.
| Рамка 14. Антигипертензивная терапия у больных диабетом |
|---|
|
Данные, представленные в разделе 4.4, не оставляют сомнения в том, что снижение АД у больных сахарным диабетом 2-го типа оказывает выраженное протективное действие на сердечно-сосудистую систему независимо от выбора антигипертензивного(-ых) препарата(-ов). В плацебоконтролируемых исследованиях применяли диуретики (часто в комбинации с бета-блокаторами), антагонисты кальция и ингибиторы АПФ. Это позволяет сделать вывод о том, что даже у больных сахарным диабетом польза антигипертензивной терапии в профилактике сердечно-сосудистых исходов в значительной степени связана со снижением АД как такового. Недавно при мета-анализе исследований было показано, что более низкие целевые значения АД у больных диабетом 2-го типа дают более выраженный профилактический эффект, чем у пациентов без диабета. Данные, представленные в разделах 5.1 и 5.2, подтверждают целесообразность назначения антигипертензивной терапии при высоких нормальных значениях АД и снижения его до 130/80 ммрт.ст. и менее. Влияние более низких значений АД на течение диабетической нефропатии менее изучено (раздел 4.5.4).
| Рамка 15. Антигипертензивная терапия у больных с нарушенной функцией почек |
|---|
|
В нескольких контролируемых рандомизированных исследованиях у больных сахарным диабетом 2-го типа изучались нефропротективные свойства ряда антигипертензивных препаратов, не связанные с их гипотензивной активностью. Как указано в разделе 4.5.4, доказаны преимущества антагонистов ангиотензиновых рецепторов и ингибиторов АПФ, которые предупреждают появление микроальбуминурии и протеинурии и снижают экскрецию белка с мочой. Таким образом, по возможности, больным сахарным диабетом 2-го типа следует снижать АД до <130/80 мм рт.ст. Показаны интенсивные немедикаментозные мероприятия. Особое внимание следует уделять вмешательствам (ограничение калорийности пищи и повышение физической активности), которые позволяют снизить массу тела, так как избыточная масса тела и ожирение часто встречаются у больных сахарным диабетом 2-го типа, а похудание ассоциируется с некоторым снижением АД и улучшением толерантности к глюкозе. Антигипертензивные препараты могут быть назначены при высоком нормальном АД и наличии микроальбуминурии. В принципе, могут быть использованы любые антигипертензивные средства. Следует учитывать, что у больных сахарным диабетом труднее добиться адекватного контроля АД, поэтому им часто требуется комбинированная терапия, по крайней мере, двумя препаратами. Бета-блокаторы и тиазидные диуретики не следует применять на первом этапе лечения, так как они могут ухудшить инсулинорезистентность и вызвать необходимость в увеличении доз или числа сахароснижающих препаратов. При наличии микроальбуминурии или диабетической нефропатии лечение следует начинать с блокаторов ренин-ангиотензиновой системы или включать их в схемы комбинированной терапии. У больных сахарным диабетом 2-го типа ингибиторы АПФ предупреждали появление микроальбуминурии, поэтому они могут быть также использованы с целью профилактики нефропатии. Целесообразно также применение гиполипидемических средств, так как в исследовании CARDS была подтверждена польза адекватного контроля уровней липидов у больных сахарным диабетом.
7.3. Цереброваскулярная болезнь
7.3.1. Инсульт и транзиторные ишемические атаки
В рекомендациях ESH/ESC 2003 г. уже были представлены доказательства пользы антигипертензивной терапии у больных, перенесших инсульт или транзиторные ишемические атаки. Они были получены в двух плацебоконтролируемых исследованиях, проведенных двойным слепым методом (PATS при лечении диуретиком и PROGRESS при применении ингибитора АПФ периндоприла, часто в комбинации с индапамидом). В обоих исследованиях частота повторного инсульта снизилась примерно на 30%. В этих исследованиях установлена эффективность лечения как у больных АГ, так и у пациентов с нормальным АД. Тенденция к улучшению при лечении ингибитором АПФ по сравнению с плацебо наблюдалась также в исследовании HOPE в подгруппе больных, перенесших инсульт. Таким образом, снижение АД является эффективной стратегией вторичной профилактики у больных с цереброваскулярной болезнью, даже если исходное АД составляет менее 140/90 ммрт. ст. (см. раздел 5.1).
| Рамка 16. Антигипертензивная терапия у больных с цереброваскулярной патологией |
|---|
|
После публикации рекомендаций 2003 г. были получены дополнительные данные, позволяющие уточнить роль антигипертензивной терапии у больных с цереброваскулярной патологией. Анализ результатов исследования PROGRESS продемонстрировал снижение риска как ишемического, так и геморрагического инсульта, которое было пропорциональным степени снижения АД. В этом исследовании комбинированная терапия периндоприлом и индапамидом привела к снижению систолического АД на 12,3 мм рт. ст. и риска инсульта на 43% (ишемического – на 36% и геморрагического – на 76%), в то время как монотерапия периндоприлом вызывала меньшее снижение систолического АД и недостоверно снижала риск инсульта (5%). Целевой уровень АД, который обеспечивает максимальную пользу лечения у больных, перенесших инсульт или транзиторные ишемические атаки, не установлен, хотя ретроспективный анализ PROGRESS свидетельствует о том, что он составляет менее 130 мм рт. ст.
Накапливаются также данные о применении антагонистов ангиотензиновых рецепторов. При анализе результатов исследования SCOPE у больных, перенесших инсульт, рандомизированных в группу кандесартана, было выявлено значительное снижение частоты инсульта и основных сердечно-сосудистых исходов по сравнению с контрольной терапией в сочетании с плацебо. Как указано в разделе 4.4.4, в исследовании MOSES у больных АГ, перенесших нарушения мозгового кровообращения, лечение антагонистом ангиотензиновых рецепторов эпросартаном привело к снижению частоты сердечно-сосудистых исходов на 31% по сравнению с нитрендипином, однако снижение риска повторного инсульта (12%) не достигало статистической значимости. В целом, положительная роль снижения АД убедительно доказана, однако сравнительная эффективность различных антигипертензивных препаратов в отношении профилактики повторного инсульта нуждается в дополнительном изучении.
Информация о необходимой степени и оптимальных методах снижения АД у больных острым инсультом ограниченна. Результаты отдельных исследований и патофизиологические данные свидетельствуют о том, что при остром инсульте происходит нарушение ауторегуляции головного мозга (особенно в области инфаркта или кровоизлияния), а быстрое снижение АД может привести к гипоперфузии пораженных участков головного мозга и распространению некроза. Однако в клиническом исследовании у 339 больных АГ применение кандесартана с первого дня инсульта привело к значительному снижению смертности и числа сердечно-сосудистых исходов в течение последующих 12 мес. В этом исследовании кандесартан применяли в обеих группах (исключая первые дни после инсульта, когда его назначали только пациентам основной группы), поэтому его благоприятный эффект мог не зависеть от снижения АД или быть следствием более быстрого контроля АД. В настоящее время проводятся дополнительные исследования, в которых изучается эффективность антигипертензивных средств у больных острым инсультом. Пока же снижать повышенное АД в первые часы после инсульта следует осторожно, тем более что оно часто спонтанно нормализуется в течение последующих нескольких дней. С другой стороны, резкое повышение АД может создавать угрозу для жизни, а его неотложное снижение необходимо при наличии отека легких, расслоения стенки аорты и перенесенного инфаркта миокарда. Во всех этих случаях АД следует снижать постепенно под тщательным контролем врача.
7.3.2. Когнитивная дисфункция и деменция
В нескольких исследованиях было показано, что высокое АД ассоциируется с когнитивной дисфункцией, а у больных АГ различные виды деменции встречаются чаще, чем у людей с нормальным АД. Высокое АД приводит к поражению мелких сосудов, которое является причиной развития лакунарных инфарктов и поражения белого вещества головного мозга, которые часто наблюдаются у больных АГ и ассоциируются с ухудшением когнитивной функции.
Хотя польза антигипертензивной терапии для профилактики инсульта убедительно доказана, ее благоприятное влияние на течение других форм цереброваскулярной болезни (таких как поражение белого вещества головного мозга, нарушение когнитивной функции и деменция) четко не установлено. В разделе 4.5.3 приведены результаты исследований и мета-анализа, в которых изучались эффекты антигипертензивной терапии, в основном, по сравнению с плацебо, на различные когнитивные функции. В целом, снижение АД несколько улучшало когнитивную функцию и память, но не влияло на способность к обучению. В настоящее время снижение когнитивной функции у больных АГ может рассматриваться как показание к снижению АД, однако необходимы дополнительные исследования в этой области, так как когнитивная дисфункция наблюдается примерно у 15% людей в возрасте ≥ 65 лет, а частота деменции увеличивается с 5% в указанном возрасте до 25% после 85 лет.
7.4. Коронарная болезнь сердца и сердечная недостаточность
У больных ИБС часто наблюдается повышение АД или АГ в анамнезе. После инфаркта миокарда риск фатальных и нефатальных коронарных осложнений более высок, если повышено АД. В плацебоконтролируемых или сравнительных рандомизированных исследованиях применение нескольких бета-блокаторов, ингибиторов АПФ или антагонистов ангиотензиновых рецепторов сразу или спустя некоторый срок после инфаркта миокарда обычно приводило к значительному снижению сердечно-сосудистой заболеваемости и смертности. Во многих случаях дизайн исследований предполагал изучение органопротективных свойств определенных препаратов, а не эффекта снижения АД; в связи с этим в некоторых случаях отсутствовала полная информация о его изменениях. В тех случаях, когда они были известны, АД практически всегда было ниже в группах больных, получавших активное лечение, что не позволяло четко дифференцировать прямые эффекты изученных агентов и благоприятные последствия снижения АД. Тем не менее, четко доказана польза применения антигипертензивных препаратов, таких как бета-блокаторы, ингибиторы АПФ и антагонисты ангиотензиновых рецепторов, у больных, недавно перенесших инфаркт миокарда, особенно при наличии систолической дисфункции.
| Рамка 17. Антигипертензивная терапия у больных ИБС и сердечной недостаточностью |
|---|
|
Результаты 4-х плацебоконтролируемых исследований у больных хронической ИБС обобщены в разделе 4.2. В трех из них, но не в четвертом, было выявлено снижение риска сердечно-сосудистых исходов при снижении АД. Важная роль его подтверждается результатами ретроспективного анализа исследования INVEST. Было показано, что независимо от выбранной антигипертензивной терапии у больных АГ и ИБС частота сердечно-сосудистых исходов снижалась пропорционально достигнутому АД и была значительно ниже у пациентов, у которых удалось достичь контроля АД.
В исследовании INVEST была отмечена сопоставимая частота коронарных и сердечно-сосудистых исходов у больных АГ и ИБС при лечении верапамилом (± трандолаприлом) или атенололом (± гидрохлортиазидом). В исследовании ALLHAT в большой подгруппе больных АГ и ИБС также продемонстрирована сопоставимая частота коронарных и сердечно-сосудистых осложнений при лечении хлорталидоном, лизиноприлом или амлодипином.
Таким образом, создается впечатление, что для больных ИБС большое значение имеет снижение АД как таковое, а не выбор конкретного гипотензивного препарата. В частности, опровергнуты заявления о том, что антагонисты кальция могут представлять опасность для коронарных больных. Очевидно, что у больных коронарной болезнью сердца АД следует снижать постепенно и избегать тахикардии.
У больных застойной сердечной недостаточностью повышение АД наблюдается редко, так как у них снижена насосная функция сердца и сердечный выброс. В ряде рандомизированных исследований было продемонстрировано увеличение выживаемости и снижение частоты госпитализаций при применении антигипертензивных препаратов. С лечебной целью могут применяться тиазиды или петлевые диуретики, а также бета-блокаторы, антагонисты альдостерона, ингибиторы АПФ или антагонисты ангиотензиновых рецепторов (на фоне диуретической терапии; см. раздел 4). Если у больного сердечной недостаточностью сохраняется АГ при лечении указанными препаратами, то могут быть добавлены дигидропиридиновые антагонисты кальция, особенно при наличии стенокардии. У значительной части больных хронической сердечной недостаточностью, особенно страдающих АГ, и пожилых людей отсутствует систолическая дисфункция и определяется нарушение диастолической функции левого желудочка (см. раздел 3.6.1). Недавно было показано, что антагонисты ангиотензиновых рецепторов дают определенный положительный эффект у больных сердечной недостаточностью и сохранной систолической функцией; однако имеющиеся данные пока ограниченны, а польза применения антигипертензивных препаратов при этой распространенной форме сердечной недостаточности должна быть подтверждена в клинических исследованиях.
7.5. Фибрилляция предсердий
АГ – самый важный популяционный фактор риска фибрилляции предсердий. Фибрилляция предсердий повышает риск сердечно-сосудистой заболеваемости и смертности примерно в 2-5 раз и ассоциируется со значительным увеличением риска эмболического инсульта. Независимыми факторами риска фибрилляции предсердий считают увеличение массы миокарда левого желудочка и диаметра левого предсердия. При наличии указанных изменений больные АГ нуждаются в интенсивной антигипертензивной терапии. Жесткий контроль АД необходим, если начато лечение антикоагулянтами, учитывая увеличение частоты инсульта и геморрагических осложнений при систолическом АД ≥140 мм рт. ст. При ретроспективном анализе результатов двух исследований было выявлено снижение частоты фибрилляции предсердий при лечении антагонистами ангиотензиновых рецепторов (см. раздел 4.5.1), поэтому эти препараты могут быть предпочтительными, хотя их эффективность требует подтверждения.
В двух исследованиях у больных с фибрилляцией предсердий было выявлено снижение частоты пароксизмов при добавлении антагонистов рецепторов ангиотензина к амиодарону (см. раздел 4.5.1). Указанные исследования были относительно небольшими, поэтому их результаты желательно подтвердить в более крупных исследованиях. В
настоящее время применение антагонистов ангиотензиновых рецепторов можно считать предпочтительным у больных с пароксизмальной фибрилляцией предсердий, которые нуждаются в лечении АГ. По данным мета-анализа, ингибиторы АПФ и антагонисты ангиотензиновых рецепторов снижали частоту пароксизмов в сопоставимой степени у больных пароксизмальной фибрилляцией предсердий и застойной сердечной недостаточностью. Это свидетельствует о благоприятном эффекте блокады ренин-ангиотензиновой системы под влиянием препаратов обоих классов.При постоянной форме фибрилляции предсердий сохраняют большое значение бета-блокаторы и недигидропиридиновые антагонисты кальция (верапамил и дилтиазем), которые снижают частоту желудочкового ритма.
7.6. Недиабетическая нефропатия
До появления антигипертензивных средств поражение почек часто наблюдалось у больных первичной гипертензией. В 1955 г. G.A. Perera при обследовании 500 больных выявил протеинурию в 42% случаев и хроническую почечную недостаточность в 18%. В этой серии ожидаемая продолжительность жизни после появления признаков поражения почек не превышала 5-7 лет.
На фоне антигипертензивной терапии почечные осложнения АГ развиваются относительно нечасто, однако при анализе скорости клубочковой фильтрации и клиренса креатинина оказалось, что у достаточно большого процента пациентов наблюдается нарушение функции почек, которое является важным фактором риска сердечно-сосудистых заболеваний.
Как указано в разделе 4.5.4, имеется достаточно данных для того, чтобы рекомендовать таким больным снижение АД, по крайней мере, до 120/80 мм рт. ст., особенно при наличии протеинурии. В нескольких исследованиях блокада ренин-ангиотензиновой системы более эффективно задерживала развитие терминальной нефропатии и повышение уровня креатинина в сыворотке и снижала протеинурию и микроальбуминурию. Это не было подтверждено в других исследованиях, например, в ALLHAT, однако для снижения АД до низких целевых значений обычно требуется комбинированная терапия. Соответственно, в состав использованной схемы целесообразно включать ингибитор АПФ или антагонист ангиотензиновых рецепторов. В тех редких случаях, когда возможна монотерапия, целесообразно использовать один из препаратов этих групп. Если достигнуто целевое АД, но протеинурия остается выше 1 г/сут (или более 1 г/г креатинина), то необходима дальнейшая интенсификация терапии. Имеются обнадеживающие результаты применения ингибиторов АПФ в сочетании с антагонистами ангиотензиновых рецепторов или высоких доз последних при условии тщательного контроля уровней креатинина и калия в сыворотке. Однако этот вопрос нуждается в дополнительном изучении.
7.7. Артериальная гипертензия у женщин
В возрасте 30-44 лет у женщин систолическое АД обычно ниже, чем у мужчин. Однако систолическое АД у женщин растет быстрее, чем у мужчин, поэтому после 60 лет у них чаще встречается АГ. Связь между АД и сердечно-сосудистыми заболеваниями является сходной у женщин и мужчин, за исключением более низкой абсолютной частоты ИБС у женщин молодого возраста. По данным мета-анализа, благоприятный эффект антигипертензивной терапии по сравнени юс плацебо был сходным у мужчин и женщин. Мета-анализ зависимости результатов применения препаратов различных классов от пола не проводился. Однако в большинстве исследований было выявлено сходное снижение риска при использовании различных схем антигипертензивной терапии у мужчин и женщин. Исключением являются исследование ANBP 2, в котором преимущество эналаприла перед гидрохлортиазидом отмечалось только у мужчин, и исследования VALUE, в котором амлодипин по сравнению с валсартаном более эффективно снижал АД и риск сердечных осложнений у женщин, но не у мужчин.
| Рамка 18. Гипертензия у женщин |
|---|
| 1. Лечение АГ у женщин |
| Ответ на антигипертензивную терапию и благоприятные эффекты снижения АД сходны у женщин и мужчин. Однако ингибиторы АПФ и антагонисты ангиотензиновых рецепторов не следует назначать беременным женщинам и женщинам, планирующим беременность, учитывая тератогенное действие этих средств. |
| 2. Пероральные контрацептивы |
| Пероральные контрацептивы, содержащие низкие дозы эстрогенов, повышают риск АГ, инсульта и инфаркта миокарда. Контрацептивы, содержащие только прогестогены, могут быть использованы у женщин с высоким АД, однако их влияние на риск сердечно-сосудистых исходов изучено недостаточно. |
| 3. Гормонозаместительная терапия |
| Гормонозаместительная терапия снижает частоту переломов костей и рака толстой кишки, но увеличивает риск коронарных осложнений, инсульта, тромбоэмболий, рака молочной железы, заболеваний желчного пузыря и деменции. Ее не следует назначать с целью кардиопротекции женщинам постменопаузального возраста. |
| 4. Гипертензия во время беременности |
|
У женщин детородного возраста следует избегать применения потенциально тератогенных средств. Им нецелесообразно назначать ингибиторы АПФ и антагонисты ангиотензиновых рецепторов. В случае беременности эти препараты следует немедленно отменить.
7.7.1. Пероральные контрацептивы
Пероральные контрацептивы вызывают небольшое увеличение АД у большинства женщин и стойкую гипертензию примерно у 5%. Риск сердечно-сосудистых осложнений, в основном, повышается у женщин старше 35 лет, а также курящих. АГ, вызванная пероральными контрацептивами, обычно протекает легко, а АД возвращается к норме в течение 6 мес после прекращения их приема. Имеются противоречивые данные о возможном влиянии пероральных контрацептивов на прогрессирование АГ, в то время как в некоторых исследованиях отмечена связь между их применением и поражением почек, подтвержденным при биопсии, при отсутствии первичной нефропатии. Основной причиной повышения АД считают эстрогены, однако механизмы их гипертензивного действия неизвестны. Хотя эстрогены улучшали эндотелиальную функцию, они могут стимулировать синтез ангиотензиногена в печени. Во время менструального цикла растяжимость артерий меняется в зависимости от изменений концентраций эстрогенов, а применение пероральных контрацептивов ассоциировалось с увеличением альбуминурии.
Препараты, содержащие 30 мкг эстрогенов и 1 мг прогестогена и менее, считают относительно безопасными. Однако в эпидемиологическом исследовании было показано, что, хотя в 1994 г. чаще всего применяли комбинированные контрацептивы, содержавшие низкую дозу эстрогенов, у англичанок, принимавших подобные препараты, АД было выше (на 2,3/1,6 мм рт. ст.). В крупном проспективном когортном исследовании у американских медсестер применение пероральных контрацептивов сопровождалось удвоением относительного риска развития АГ.
В нескольких исследованиях случай-контроль, проведенных в конце 60-х годов, была подтверждена связь между пероральными контрацептивами и инсультом. Хотя клиническое значение этой связи при использовании низких доз контрацептивов было недавно подвергнуто сомнению, тем не менее, при систематизированном обзоре литературы было выявлено увеличение риска инсульта и острого инфаркта миокарда у женщин, пользовавшихся контрацептивами. Кроме того, пероральные контрацептивы в 2-6 раз повышают относительный риск венозных тромбозов и эмболий, а их применение ассоциируется с увеличением частоты тромботического инсульта.
При наличии АГ, вызванной комбинированными пероральными контрацептивами или обусловленной другими причинами, с целью контрацепции можно применять препараты, содержащие только прогестогены. Пока достоверной ассоциации между их применением и развитием АГ не выявлено (при длительности наблюдения 2-4 года), однако этот вопрос не изучался в рандомизированных исследованиях, так как их проведение является сложным и спорным с этической точки зрения.
7.7.2. Гормонозаместительная терапия
В западных странах у женщин после наступления менопаузы отмечается более быстрое увеличение систолического АД, чем у мужчин. Вопрос о том, является ли это следствием возраста или менопаузы, продолжается обсуждаться, так как результаты исследований, в которых изучалась эта связь, оказались противоречивыми. Исследование, охватывающее 18 326 женщин, свидетельствует о том, что менопауза сопровождается некоторым повышением АД, однако оно невелико (около 3/3 мм рт. ст.) и в значительной степени маскируется прессорным эффектом старения.
Однако нет сомнения в том, что после менопаузы у женщин повышается сердечно-сосудистый риск и отмечаются неблагоприятные изменения многих сердечно-сосудистых факторов риска. Это привлекло интерес к изучению влияния гормоно-заместительной терапии на риск сердечно-сосудистых заболеваний. В ряде клинических исследований было показано, что такая терапия сопровождается улучшением профиля сердечно-сосудистыхфакторов риска и снижением частоты ИБС и инсульта. Кроме того, у женщин постменопаузального возраста, которые получали гормонозаместительную терапию, было отмечено менее значительное повышение систолического АД по сравнению с контролем. Однако последние крупные исследования не подтвердили эффективность гормонозаместительной терапии в отношении профилактики сердечно-сосудистых исходов и продемонстрировали увеличение риска рака и сердечно-сосудистых заболеваний. Всистематизированном обзоре группы Cochrane было показано, что единственным благоприятным эффектом гормонозаместительной терапии было снижение частоты переломов костей и рака толстой кишки, которое сопровождалось значительным увеличением риска коронарных исходов, инсульта, венозных тромбозов и легочных эмболий, рака молочной железы, заболеваний желчного пузыря, а у женщин в возрасте старше 65 лет – деменции. В связи с этим в настоящее время женщинам постменопаузального возраста не рекомендуется назначать гормонозаместительную терапию с целью кардиопротекции.
7.7.3. Артериальная гипертензия у беременных
АГ у беременных во всем мире остается важной причиной заболеваемости и смертности женщин, плодов и новорожденных. АД в норме снижается во втором триместре и примерно на 15 мм рт. ст. ниже, чем до беременности. Однако в третьем триместре АД повышается до исходных значений или превышает их. Указанные изменения наблюдаются уженщин с нормальным АД, а также у пациенток с АГ, в том числе развившейся во время беременности.
Критерии диагностики АГ во время беременности неоднородны. В прошлом ее критерием служило повышение АД во втором триместре по сравнению со значениями, зарегистрированными в первом триместре и до беременности, однако сегодня АГ предпочитают диагностировать на основании абсолютных значений АД (≥140/90 мм рт. ст.). Диагностировать АД во время беременности следует на основании, по крайней мере, двух повышенных значений. Однако показано, что среднесуточные значения АД имеют преимущества перед стандартными показателями и позволяют предсказать появление протеинурии, риск преждевременных родов, массу тела новорожденного и в целом исходы беременности. Таким образом, с диагностическими и лечебными целями полезно проведение амбулаторного мониторирования АД, особенно у беременных женщин высокого риска с АГ, а также у пациенток с диабетом или нефропатией. До последнего времени диастолическое АД рекомендовали регистрировать в фазу IV Короткова (в этом случае АД теснее коррелирует с интраартериальными значениями), а не в фазу V (исчезновение тонов), когда могут быть зарегистрированы слишком низкие значения. Однако фазу IV труднее идентифицировать, а измеренные значения АД оказываются менее воспроизводимыми. В настоящее время диастолическое АД у беременных рекомендуют измерять в фазу V. В фазу IV его измеряют только, если тоны определяются при давлении в манжете, приближающемся к 0 мм рт. ст.
АГ во время беременности включает в себя следующие формы:
- АГ, имевшаяся до беременности: наблюдается у 1-5% беременных женщин. Критерием служит повышение АД ≥140/90 мм рт. ст. до бременности или в течение первых 20 нед, которое обычно сохраняется в течение более 42 дней после родов. Может сочетаться с протеинурией.
- Гестационная АГ – АГ, индуцированная беременностью и не сопровождающаяся протеинурией. Гестационная АГ, ассоциирующаяся со значительной протеинурией (более 300 мг/л или более 500 мг/сут или, по крайней мере, ++), называется преэклампсией. АГ развивается спустя 20 нед беременности и в большинстве случаев проходит в течение 42 дней после родов. Гестационная АГ характеризуется снижением перфузии органов.
- АГ, имевшаяся до беременности, в сочетании с гестационной гипертензией и протеинурией. АГ, имевшаяся до беременности, которая характеризуется дальнейшим увеличением АД и экскреции белка с мочой более 3 г/сут после 20 нед беременности. Старый термин – «хроническая АГ, сочетающаяся с преэклампсией».
- Неклассифицируемая АГ. АГ, сопровождающаяся или не сопровождающаяся системными проявлениями, которую диагностируют после 20 нед беременности, если предыдущие значения АД неизвестны. В таких случаях необходимо измерять АД в течение 42 дней после родов и в более поздние сроки. Если АГ проходит, то диагностируют гестационную гипертензию с протеинурией или без нее. Если АГ сохраняется, то это свидетельствует о том, что она имелась и до беременности.
Частота отеков достигает 60% при нормальном течении беременности. В настоящее время они не являются критерием диагностики преэклампсии.
АГ у беременных, особенно гестационная АГ с протеинурией и без нее, может привести к изменениям крови, почек и печени и неблагоприятным исходам у новорожденных и женщин.
При повышении систолическогоАДдо 140-149 и/или диастолического АД до 90-95 мм рт. ст. целесообразно использование немедикаментозныхметодов. В зависимости от уровня АД, срока беременности и наличия факторов риска подходы к лечению могут включать в себя тщательное наблюдение и ограничение физической активности. Рекомендуется нормальная диета без ограничения потребления соли. Эффективность некоторых мер профилактики гестационной гипертензии, особенно преэклампсии, таких как применение кальция (2 г/сут), рыбьего жира или ацетилсалициловой кислоты в низких дозах, не подтверждена, поэтому они не рекомендуются. Однако аспирин в низких дозах используется с профилактической целью у женщин с ранней преэклампсией (<28 нед). Снижение массы тела способствует уменьшению АД, однако оно не рекомендуется во время беременности женщинам с ожирением, учитывая возможную ассоциацию с низкой массой тела новорожденного и последующим замедлением его роста. Польза продолжения антигипертензивной терапии у беременных женщин, страдавших легкой или умеренной гипертензией до беременности, продолжает дискутироваться. Во-первых, в таких случаях имеется низкий риск развития сердечно-сосудистых исходов во время беременности, а прогноз для матери и новорожденного является благоприятным. Во-вторых, снижение АД может быть полезным для женщины с АГ, но одновременно может ухудшить перфузию плаценты и, соответственно, оказать неблагоприятное влияние на развитие плода.Наконец, эффективность фармакотерапии у беременных женщин с легкой и умеренной гипертензией в основном изучалась в небольших исследованиях, которые не позволяют выявить возможное небольшое снижение частоты акушерских осложнений. Тем не менее, представляется целесообразным рекомендовать фармакотерапию при повышении систолического АД до ≥150ммрт. ст. или диастолического АД до ≥95ммрт. ст. Однако более низкий пороговый уровень АД (140/90 мм рт. ст.) обоснован у женщин с гестационной гипертензией (в сочетании с протеинурией или без нее), АГ, имевшейся до беременности и сочетающейся с гестационной гипертензией и АГ, которая сопровождается бессимптомным поражением органов-мишеней в любые сроки беременности. При повышении систолического АД до ≥170 мм рт. ст. или диастолического АД до ≥110 мм рт. ст. необходима неотложная госпитализация. В неотложных случаях АД может быть снижено с помощью внутривенного введения лабеталола, перорального приема метилдопы или нифедипина. Внутривенное введение гидралазина больше не рекомендуется, так как оно чаще сопровождается нежелательными перинатальными эффектами. Внутривенная инфузия натрия нитропруссида остается методом выбора в лечении гипертонических кризов, хотя длительное применение препарата повышает риск интоксикации плода цианидами, так как нитропруссид метаболизируется до тиоцианата. При преэклампсии, осложнившейся отеком легких, нитроглицерин является препаратом выбора. При нетяжелой гипертензии предпочтительно применение метилдопы, лабеталола и антагонистов кальция. Атенолол во время беременности следует назначать осторожно, учитывая случаи внутриутробной задержки развития плода, которая зависит от длительности лечения. Ингибиторы АПФ и антагонисты ангиотензиновых рецепторов никогда не следует назначать беременным женщинам. При отсутствии олигурии диуретическая терапия при преэклампсии необоснованна, так как объем плазмы снижен. Доказана эффективность внутривенного введения магния сульфата для профилактики эклампсии и лечении судорог. Индукция родов показана, если гестационная АГ сопровождается протеинурией и другими осложнениями, такими как нарушения зрения и свертывания или дистресс у плода.
Все антигипертензивные средства выводятся с грудным молоком. Однако концентрации большинства препаратов в грудном молоке очень низки, исключая пропранолол и нифедипин, уровни которых соответствуют таковым в плазме.
У женщин, перенесших гестационную гипертензию, повышен риск развития сердечно-сосудистых заболеваний после беременности. Возможно, этот риск отражает относительную гиперандрогению, а также нарушения эндотелиальной функции, обмена углеводов и липидов.
7.8. Метаболический синдром
Метаболический синдром включает различные нарушения обмена глюкозы и липидов, а также АГ. Широко используемые критерии диагностики этого состояния (хотя и не общепринятые) были предложены экспертами Национальной образовательной программы по холестерину. Основными признаками метаболического синдрома являются
следующие:
1) высокая распространенность (до 30-40%) у людей среднего и пожилого возраста;
2) значительное повышение сердечно-сосудистой заболеваемости и смертности;
3) увеличение риска развития сахарного диабета в 3-6 раз, а также более высокий риск формирования АГ;
4) частая ассоциация с бессимптомным поражением органов-мишеней, в частности микроальбуминурией и снижением скорости клубочковой фильтрации, повышением жесткости стенок артерий, гипертрофией левого желудочка, диастолической дисфункцией, дилатацией левого предсердия, и в некоторых исследованиях – утолщением стенки сонных артерий.
Некоторые изменения могут быть выявлены независимо от наличия АГ как компонента метаболического синдрома. Гипертрофия левого желудочка ассоциируется с более высоким риском, как и повышение домашних и амбулаторных значений АД в дополнение к офисным показателям. Метаболический синдром часто сопровождается повышением маркеров воспаления, таких как высокочувствительный СРБ, который может вносить вклад в атерогенный эффект и вызывать дальнейшее повышение сердечно-сосудистого риска.
| Рамка 19. Метаболический синдром |
|---|
|
В современных руководствах первой и главной стратегией лечения метаболического синдрома считают снижение массы тела с помощью низкокалорийной диеты и физических нагрузок. Реалистичная цель – снижение массы тела на 7-10% за 6-12 мес путем относительно небольшого ограничения калорийности пищи (на 500-1 000 калорий день), которое обычно оказывается более эффективным, чем строгая диета. Диетотерапия предполагает также снижение потребления насыщенных жиров, транс-жирных кислот, холестерина и простых углеводов и увеличение потребления фруктов, овощей и хлеба грубого помола. Для стойкого снижения массы тела необходимы также регулярные физические нагрузки (например, средние нагрузки минимум по 30 мин в день). В исследованиях Diabetes Prevention Program и Finnishi Diabetes Prevention Study модификация образа жизни задерживала прогрессирование сахарного диабета почти на 60%; этот эффект превышал таковой метформина. По данным вторичного анализа исследования DPP, частота метаболического синдрома в течение 3,2 лет снизилась с 51 до 43% у больных, которым проводилась модификация образа жизни, и увеличилась с 55 до 61% у пациентов контрольной группы. Таким образом, немедикаментозные меры обладают протективным эффектом.
При наличии АГ, сахарного диабета или дислипидемии больные метаболическим синдромом нуждаются в антигипертензивных, противодиабетических или липидснижающих средствах. У пациентов с АГ и метаболическим синдромом имеется высокий сердечно-сосудистый риск, поэтому в таких случаях целесообразно добиваться снижения АД до более низких значений. Однако оптимальные целевые уровни АД у больных метаболическим синдромом не изучались. Как указано в разделах 4.4.5, 5.5 и 6.2.1, при отсутствии специальных показаний у пациентов с метаболическим синдромом следует избегать назначения бета-блокаторов, которые способствуют развитию сахарного диабета, а также оказывают нежелательное действие на массу тела, чувствительность к инсулину и липидный профиль. Эти эффекты менее выражены или отсутствуют у новых бета-блокаторов, обладающих вазодилатирующими свойствами, таких как карведилол и небиволол. Диабетогенные и другие метаболические эффекты характерны также для тиазидных диуретиков, особенно в высоких дозах, поэтому их не рекомендуется рассматривать как препараты первой линии у больных метаболическим синдромом. Возможно применение антагонистов ангиотензиновых рецепторов или ингибиторов АПФ, лечение которыми ассоциируется с более низкой частотой сахарного диабета по сравнению с другими классами антигипертензивных средств. Кроме того, они оказывают органопротективное действие (см. раздел 4.5). Если монотерапия одним из подобных препаратов не обеспечивает контроль АД, можно добавить дигидропиридиновые или недигидропиридиновые антагонисты кальция, которые метаболически нейтральны и благоприятно влияют на состояние органов-мишеней (см. раздел 4.5). Кроме того, комбинированная терапия блокатором ренин-ангиотензиновой системы и антагонистом кальция сопровождалась более низким риском развития сахарного диабета, чем стандартная терапия диуретиком и бета-блокатором. Больные метаболическим синдромом обычно страдают ожирением и сольчувствительной АГ, поэтому на втором или третьем этапе лечения обоснованно назначение тиазидного диуретика. Хотя тиазидные диуретики в низких дозах могут оказывать неблагоприятное действие на обмен веществ, они в меньшей степени снижают сывороточную концентрацию калия, что нивелирует нежелательное влияние гипокалиемии на инсулинорезистентность, толерантность к углеводам и развитие сахарного диабета. Поддержание уровня калия предупреждало развитие нарушения толерантности к глюкозе под действием тиазидов. Это свидетельствует о том, что комбинация тиазидного и калийсберегающего диуретика может иметь
преимущества перед одним тиазидным диуретиком.
Отсутствие специальных исследований у больных метаболическим синдромом не позволяет однозначно судить о том, следует ли сочетать немедикаментозные меры с антигипертензивной терапии у пациентов, не страдающих АГ или сахарным диабетом, хотя сочетание различных факторов риска и частое поражение органов-мишеней повышает сердечно-сосудистый риск у таких пациентов. Доводы за и против назначения блокатора ренин-ангиотензиновой системы пациентам с высоким нормальным АД обобщены в разделе 5. Сделан вывод о том, что в настоящее время интенсивная модификация образа жизни остается главным подходом к лечению, однако в некоторых случаях возможно применение лекарственных препаратов, в частности блокаторов ренин-ангиотензиновой системы, которые предупреждают развитие АГ и сахарного диабета и оказывают благоприятное влияние на состояние органов-мишеней, особенно часто поражаемых в этой группе высокого риска. Польза применения противодиабетических препаратов у больных метаболическим синдромом, не страдающих сахарным диабетом, убедительно не доказана. При анализе 5 проспективных исследований, в которых изучались ингибиторы альфа-гликозидаз у больных с нарушенной гликемией натощак, было выявлено снижение частоты развития сахарного диабета 2-го типа. Однако авторы не выявили значимой разницы в смертности, частоте других неблагоприятных исходов, уровнях гликированного гемоглобина и АД. Недавно для лечения сахарного диабета 2-го типа были зарегистрированы тиазолидиндионы, которые повышают чувствительность к инсулину благодаря стимуляции PPRγ рецепторов; этот эффект в меньшей степени свойственен некоторым антагонистам ангиотензиновых рецепторов. Один из этих препаратов (розиглитазон) изучали у больных с нарушенной толерантностьюк глюкозе. Была показана его высокая эффективность в профилактике развития сахарного диабета. Однако эти агенты повышают массу тела и вызывают задержку жидкости, что затрудняет оценку коэффициента польза/риск при отсутствии явного сахарного диабета. У больных сахарным диабетом пиоглитазон значительно снижал риск развития основных сердечно-сосудистых исходов. Препараты этого класса оказывали небольшое, но достоверное гипотензивное действие. В плацебоконтролируемых исследованиях блокатора эндоканнабиноидных С1-рецепторов римонабанта было отмечено снижение массы тела и окружности талии, а также благоприятные изменения сердечно-сосудистых факторов риска, таких как уровни глюкозы плазмы, холестерин ЛПВП, сывороточные трилицериды и инсулинорезистентность. Имеются данные о том, что этот препарат не повышает АД и может даже вызвать его снижение. Влияние римонабанта на сердечно-сосудистый риск в настоящее время изучается в проспективном исследовании.
Таким образом, у больных АГ и метаболическим синдромом необходимо проводить более тщательное обследование, учитывая высокую частоту поражения различных органов-мишеней и повышенные уровни маркеров воспаления. Целесообразно использование немедикаментозных методов лечения и антигипертензивных средств, если АД составляет ≥140/90 мм рт. ст. Предпочтительно применение блокаторов ренин-ангиотензиновой системы, к которым при необходимости добавляют антагонист кальция или тиазидный диуретик в низкой дозе. Лечение блокатором ренин-ангиотензиновой системы у больных с высоким нормальным АД с целью защиты органов-мишеней и профилактики АГ или сахарного диабета в настоящее время не может быть рекомендовано. При наличии сахарного диабета 2-го типа назначают сахароснижающие средства, однако четко рекомендовать применение противодиабетических средств или сенситизаторов инсулина у пациентов с нарушенной толерантностью к глюкозе не представляется возможным. Снижение частоты неблагоприятных исходов было отмечено при лечении статинами, что указывает на пользу гиполипидемической терапии. В настоящее время изучаются фармакологические подходы к лечению больных метаболическим синдромом, не страдающих АГ или сахарным диабетом. Следует учитывать, что в реальной жизни приверженность немедикаментозным методам лечения низка, а стойкое снижение массы тела отмечается редко.
7.9. Резистентная гипертензия
АГ обычно считают резистентной или рефрактерной к лечению, если немедикаментозные меры и применение, по крайней мере, трех антигипертензивных препаратов (включая диуретик) в адекватных дозах не приводит к снижению систолического и диастолического АД до целевых значений. Частота резистентной гипертензии, диагностированной на основании указанного критерия, высока: например, в когорте ALLHAT 8% больных АГ получали 4 препарата или более, а частота резистентной гипертензии составила минимум 15%. В таких ситуациях пациента целесообразно направить к специалисту или в специализированный центр, так как рефрактерная АГ часто сочетается с поражением органов-мишеней и высоким сердечно-сосудистым риском.
| Рамка 20. Причины резистентной гипертензии |
|---|
|
| Причины ложной резистентной гипертензии |
|
Одной из самых частых причин резистентной гипертензии (рамка 20) является низкая приверженность антигипертензивной терапии и немедикаментозным мерам (в частности, продолжение злоупотребления алкоголем). В этой ситуации возможны два подхода к лечению. Иногда имеет смысл прекратить всю терапию под тщательным наблюдением врача и назначить новую более простую схему. Возможна также госпитализация на короткий срок. Другой нередкой причиной резистентной АГ является обструктивное апноэ во сне – возможно, за счет поздних эффектов гипоксии и стимуляции хеморецепторов, а также нарушения сна. Кроме того, необходимо исключить причины вторичной гипертензии (см. раздел 9). Например, скрытый стеноз почечной артерии может привести к развитию рефрактерной АГ. Хотя шансы на снижение АД выше у молодых людей, тем не менее, у таких пациентов можно уменьшить потребность в антигипертензивных препаратах в результате реваскуляризации почечной артерии с помощью баллонной ангиопластики и стентирования. Причиной неадекватного снижения АД может быть также необратимое или малообратимое распространенное поражение сердечно-сосудистой системы. Перегрузка объемом может быть следствием прогрессирующей почечной недостаточности, избыточного потребления соли, гиперальдостеронизма и особенно часто – неадекватной диуретической терапии. Наконец, следует учитывать возможность АГ «белого халата» или неадекватного измерения АД (использование манжет недостаточного размера, которое приводит к завышению результатов измерения). У пожилых людей необходимо также исключать псевдогипертензию, когда невозможно сдавить жесткую стенку сосуда с помощью манжеты, а измеренное АД превышает реальное.
Первым этапом ведения больного резистентной гипертензией должны быть тщательное изучение анамнеза и обследование, в первую очередь – с целью исключения причин
вторичной гипертензии. Обследование должно включать в себя амбулаторное мониторирование АД, которое помогает оценить степень повышения АД и сердечно-сосудистый риск. Необходимо оценить приверженность к лечению. При опросе иногда удается установить возможные причины резистентности гипертензии, например, периодическое употребление алкоголя.
В итоге многие больные нуждаются в лечении более чем 3-мя антигипертензивными препаратами. До настоящего времени выбор препаратов третьего, четвертого или пятого ряда в рандомизированных исследованиях не изучался. Результаты последних исследований продемонстрировали значительное снижение АД при добавлении антагониста альдостерона спиронолактона к многокомпонентой схеме лечения больных резистентной гипертензией. В плацебоконтролируемом рандомизированном исследовании С. Saha и соавт. выявили более выраженный дополнительный антигипертензивный эффект амилорида по сравнению с таковым спиронолактона. Однако спиронолактон дает хороший дополнительный антигипертензивный эффект в достаточно небольшой дозе (25-50 мг/сут). Описан также хороший ответ на амилорид. В настоящее время неясно, является ли адекватный ответ на антагонисты альдостерона следствием недиагностированного первичного гиперальдостеронизма или вторичного гиперальдостеронизма, индуцированного комбинированной терапией.Применение низких доз этих препаратов снижает вероятность развития нежелательных эффектов, однако необходимо контролировать сывороточные уровни калия и креатинина, так как у многих таких больных наблюдается снижение функции почек и часто используются блокаторы ренин-ангиотензиновой системы. Эффективность антагонистов эндотелина у больных резистентной гипертензией находится на стадии изучения. Недавно была продемонстрирована возможность снижения АД у таких пациентов с помощью хронической стимуляции каротидного синуса с помощью имплантированных электрических устройств.
7.10. Неотложные ситуации
Неотложные ситуации возникают в тех случаях, когда тяжелая АГ приводит к острому поражению органов-мишеней. Значительное повышение АД, ассоциирующееся с острым нарастанием поражения органов-мишеней, которое иногда наблюдается у пожилых людей с изолированной систолической гипертензией, не следует считать неотложным состоянием. В таких случаях необходима экстренная терапия, однако она соответствует таковой при хроническом повышении АД. Наиболее важные неотложные состояния перечислены в табл. 8. Они встречаются редко, но могут создавать угрозу для жизни.При их развитии необходимо быстрое лечение АГ. Следует, однако, соблюдать осторожность, так как чрезмерно резкое падение АД может осложниться нарушением перфузии головного мозга и развитием церебрального инфаркта или поражения миокарда и почек.
| Гипертоническая энцефалопатия |
| Левожелудочковая недостаточность |
| Инфаркт миокарда |
| Нестабильная стенокардия |
| Расслоение стенки аорты |
| Субарахноидальное кровоизлияние или нарушение мозгового кровоображения |
| Гипертонический криз при феохромоцитоме |
| Применение амфетаминов, ЛСД, кокаина или экстази |
| Периоперационная гипертензия |
| Тяжелая преэклампсия или эклампсия |
Выраженного и резкого снижения АД следует избегать при остром инсульте (см. раздел 7.3.1).
7.11. Злокачественная гипертензия
Хотя существует очевидный перекрест между резистентной и злокачественной гипертензией, в большинстве развитых стран последняя встречается нечасто. В основном ее наблюдают у пациентов, занимающих более низкое социальное положение. Злокачественная АГ характеризуется значительным повышением АД (диастолическое АД обычно, но не всегда, превышает 140 мм рт. ст.) и поражением сосудов, которое может проявляться кровоизлияниями или экссудатами в сетчатку и/или отеком соска зрительного нерва.
Некоторые врачи используют термин «быстро прогрессирующая АГ», если имеется подобный синдром, но отсутствует отек соска зрительного нерва. Злокачественная АГ может наблюдаться при различных состояниях. Тяжелая или плохо контролируемая эссенциальная АГ обычно предшествует ее развитию, хотя в некоторых исследованиях, возможно, недооценивалась важность вторичных причин повышения АД. Сообщалось, что многие пациенты со злокачественной гипертензией являются курильщиками, а у афроамериканцев она встречается чаще, чем у белых. Частота этого состояния среди больных АГ явно снизилась в результате более раннего и эффективного лечения, а также устранения многих предрасполагающихфакторов. В основе злокачественной гипертензии лежит нарушение ауторегуляции в результате постоянного воздействия на стенку артерий очень высокого АД. При морфологическом исследовании в стенке сосудов выявляли пролиферацию миоинтимы и фибриноидный некроз. Выраженность пролиферативных изменений коррелирует с тяжестьюи длительностью значительного повышения АД. Фибриноидный некроз развивается в результате спазма и форсированной дилатации мелких артерий. Протекание жидкости во внеклеточное пространство сопровождается небольшими геморрагиями и поражением органов-мишеней.
Самым опасным осложнением злокачественной фазы гипертензии является гипертоническая энцефалопатия. Она сопровождается обратимыми нарушениями неврологической функции, включая головную боль, нарушение психического состояния и зрения. Кроме того, наблюдается нарушение функции почек, которое имеет важное прогностическое значение. Более тяжелые формы почечной недостаточности ассоциировались со снижением ожидаемой продолжительности жизни, несмотря на своевременное и эффективное лечение гипертензии. У некоторых больных развивается необратимое поражение почек, которое вынуждает начинать лечение программным гемодиализом. Кроме того, злокачественная АГ ассоциируется с гемолизом, фрагментацией эритроцитов и диссеминированным внутрисосудистым свертыванием крови.
Если при злокачественной гипертензии не проводится лечение, то прогноз крайне неблагоприятный. Около 50% больных умирают в течение 12 мес. Однако после разработки эффективных схем лечения частота подобных исходов снизилась, что отражает не только улучшение контроля АД, но и своевременное выявление причин вторичной гипертензии и повышение доступности таких методов, как диализ и трансплантация почки.
Злокачественную фазу гипертензии следует рассматривать как неотложное состояние. С целью снижения АД могут быть использованы пероральные средства, если пациент отвечает на лечение. Целью является снижение диастолического АД до 100-110 мм рт. ст. в течение 24 ч.
8. Лечение сопутствующих факторов риска
8.1. Гиполипидемические средства
В нескольких рандомизированных исследованиях изучалась эффективность статинов в отношение вторичной и первичной профилактики. Хотя эпидемиологические исследования продемонстрировали тесную связь между сывороточным холестерином и коронарными осложнениями, но не инсультом, тем не менее терапия статинами была эффективной в профилактике как коронарных, так и цереброваскулярных осложнений, а результаты лечения были сходными у больных АГ и с нормальным АД. В самом крупном исследовании Heart Protection Study применение симвастатина у пациентов с сердечно-сосудистыми заболеваниями снижало риск сердечных и цереброваскулярных осложнений по сравнению с плацебо. Эффекты препарата проявлялись у пациентов с гипертензией (41% от всей когорты) независимо от схемы проводимой антигипертензивной терапии. Сходные результаты были получены при применении правастатина у пожилых людей в исследовании PROSPER. В этом исследовании 62% больных страдали АГ. Продемонстрирована эффективность профилактической терапии аторвастатином у больных, перенесших инсульт. Следовательно, больным в возрасте, по крайней мере до 80 лет, страдающим ИБС, поражением периферических артерий, инсультом в анамнезе или сахарным диабетом (в течение, по крайней мере, 10 лет), следует назначать статины. Во всех этих случаях целевые уровни общего холестерина и холестерина ЛПНП составляют <4,5 ммоль/л (175 мг%) и <2,5 ммоль/л (100 мг%). Возможно также их снижение до более низких целевых значений – <4,0 и <2 ммоль/л (155 и 80 мг%).
| Рамка 21. Лечение сопутствующих факторов риска |
|---|
| Гиполипидемические средства |
|
| Антитромбоцитарная терапия |
|
| Контроль гликемии |
|
В двух исследованиях (ALLHAT и ASCOT) изучалась эффективность терапии статинами специально у больных АГ. В ALLHAT применение правастатина в дозе 40 мг/сут у 10 000 больных АГ (примерно у 2/3 имелось поражение сосудов) привело к снижению уровней общего холестерина и холестерина ЛПНП (на 11%и 17%, соответственно) по сравнению с обычной терапией, но не оказало существенного влияния на частоту ИБС, инсульта и общую смертность. В исследовании ASCOT терапия аторвастатином в дозе 10 мг/сут более чем у 10 000 больных АГ с дополнительными сердечно-сосудистыми факторами риска и уровнем общего холестерина менее 6,5 ммоль/л привела к его снижению на 19,9%, по сравнению с плацебо. Гиполипидемический эффект сопровождался значительным снижением частоты сердечно-сосудистых исходов (на 36%) и инсульта (на 27%). Положительные результаты исследования ASCOT могли отражать более значительную разницу уровней общего холестерина и холестерина ЛПНП между группой больных, получавших активный препарат, и контрольной группой.
С учетом результатов исследования ASCOT представляется целесообразным применение статинов у больных АГ в возрасте менее 80 лет, если расчетный 10-летний риск сердечно-сосудистых заболеваний составляет ≥ 20%или риск смерти от сердечно-сосудистых причин (с использованием модели SCORE) – ≥5%. Сообщалось о том, что применение статинов у больных АГ может сопровождаться некоторым снижением АД, хотя в исследованиях ASCOT и PHYLLIS присоединение статина к антигипертензивной терапии не оказывало явного гипотензивного действия. Целевые уровни общего холестерина и холестерина ЛПНП составляют, соответственно, <5 ммоль/л (190 мг%) и <3 ммоль/л (115 мг%). У большинства пациентов указанных целевых значений удается достичь при применении адекватных доз статинов в комбинации с немедикаментозными мерами. Если уровни общего холестерина и холестерина ЛПНП не снижаются до целевых значений или остаются измененными уровни холестерина ЛПВП или триглицеридов (<1,0 ммоль/л и >2,3ммоль/л соответственно), целесообразно присоединение эзетимиба или использование других препаратов, а также консультация специалиста.
8.2. Антитромбоцитарная терапия
Антитромбоцитарные средства, прежде всего аспирин в низкой дозе (75-100 мг/сут), снижали риск инсульта и/или инфаркта миокарда в различных выборках пациентов (от людей среднего возраста с низким сердечно-сосудистым риском до пациентов с сердечно-сосудистыми заболеваниями). Риск серьезных сосудистых исходов снижался примерно на 25%. Однако длительная терапия аспирином в низкой дозе примерно в два раза увеличивает риск серьезных внечерепных кровотечений. У больных сердечно-сосудистыми заболеваниями польза низкой дозы аспирина явно перевешивает риск больших кровотечений. Коэффициент польза/риск аспирина у пациентов низкого риска четко не определен. В связи с этим решение о назначении аспирина больным АГ следует принимать с учетом общего сердечно-сосудистого риска и/или наличия поражения органов-мишеней. Польза и возможный вред аспирина в низкой дозе у больных АГ изучались в исследовании HOT. В целом, в этом исследовании было выявлено снижение риска основных сердечно-сосудистых исходов на 15% и риска острого инфаркта миокарда на 36% при отсутствии изменения частоты инсульта и внутричерепных кровоизлияний. Однако риск больших кровотечений повысился на 65%. При ретроспективном анализе результатов исследования HOT были выделены группы больных АГ, у которых абсолютная польза аспирина превышает возможный риск. У больных с сывороточным уровнем креатинина более 115 мкмоль/л (1,3 мг%) было выявлено более значительное снижение частоты сердечно-сосудистых исходов и инфаркта миокарда (на 13 и 7 на 1 000 человеко-лет), в то время как риск кровотечений существенно не увеличился. Коэффициент польза/риск оказался также положительным у больных с более высоким исходным общим сердечно-сосудистым риском и более значительным повышением систолического и диастолического АД (польза: снижение риска сердечно-сосудистых исходов на 3,1-3,3 на 1 000 человеко-лет; вред: 1,0-1,4 кровотечения на 1 000 человеко-лет), тогда как у пациентов с более низким риском нежелательные эффекты аспирина нивелировали его пользу. Эти наблюдения согласуются с результатами нескольких мета-анализов исследований, в которых изучалась эффективность первичной профилактики, в том числе у пациентов без АГ, а также результатами исследования Women Prevention Study в большой когорте пациенток очень низкого риска. Полученные данные продемонстрировали небольшую конечную пользу аспирина. Следовательно, коэффициент польза/риск лечения аспирином в низкой дозе является положительным только у пациентов с достаточно высоким общим сердечно-сосудистым риском (15-20% в течение 10 лет). К ним относятся больные АГ с умеренным повышением сывороточного уровня креатинина, пациенты 50 лет и старше с высоким или очень высоким сердечно-сосудистым риском или более тяжелой АГ. Следует подчеркнуть, что в исследовании HOT аспирин в низкой дозе не снижал гипотензивного действия антигипертензивных средств. Польза аспирина проявлялась у больных с эффективным контролем АД (фактически у всех пациентов диастолическое АД составляло ≤90 мм рт. ст.). Нельзя исключить, что это могло препятствовать увеличению частоты внутричерепных кровоизлияний, которое было отмечено в некоторых исследованиях. Следовательно, больным АГ высокого и очень высокого риска аспирин следует назначать, по-видимому, только после достижения эффективного контроля АД.
8.3. Контроль гликемии
Сахарный диабет и нарушение толерантности к глюкозе являются основными факторами риска сердечно-сосудистых заболеваний. Как указано в разделе 7.2, АГ часто встречается у больных сахарным диабетом. У таких пациентов наблюдается значительное увеличение суммарного сердечно-сосудистого риска. Более того, АГ сама по себе удваивает риск развития сахарного диабета 2-го типа. Эффективный контроль гликемии имеет большое значение для больных АГ и сахарным диабетом. В исследовании UKPDS интенсивный контроль гликемии у больных АГ и сахарным диабетом 2-го типа привел, в основном, к снижению риска развития и прогрессирования микрососудистых осложнений. Однако другие исследования показали, что более интенсивная модификация образа жизни и фармакотерапия, обеспечивающие нормализацию нарушенного метаболизма глюкозы, снижают также риск макрососудистых осложнений. В исследовании EDIC недавно было установлено, что этот эффект, по крайней мере, отмечается у больных сахарным диабетом 1-го типа. Существует прямая связь между частотой макро- и микрососудистых осложнений и средним уровнем HbA1c; при этом отсутствует пороговая концентрация последнего, ниже которой не происходит дальнейшего снижения риска. Согласно рекомендациям по лечению сахарного диабета, целевая концентрация глюкозы натощак составляет ≤6,0 ммоль/л (108 мг%), а уровень гликированного гемоглобина – <6,5%. Учитывая известные эффекты тиазидных диуретиков и бета-блокаторов на метаболизм глюкозы, применение этих антигипертензивных препаратов у больных с нарушенной толерантностью к глюкозе может потребовать более ранней и интенсивной сахароснижающей терапии. Дополнительная информация о благоприятных эффектах более жесткого контроля гликемии будет получена после завершения двух крупных рандомизированных исследований у больных сахарным диабетом 2-го типа – ACCORD (www.accord-trial.org) и ADVANCE, в которых изучаются также дополнительные протективные эффекты более жесткого контроля АД.
9. Скрининг и лечение вторичной гипертензии
У небольшой части взрослых больных АГ удается установить конкретную причину повышения АД. Для простого скрининга вторичных форм гипертензии достаточно сбора анамнеза, физикального обследования и стандартных лабораторных тестов. На наличие вторичной гипертензии могут указывать более значительное повышение АД, внезапное развитие или прогрессирование гипертензии и отсутствие ответа на фармакотерапию. В таких случаях могут потребоваться дополнительные исследования.
9.1. Заболевания паренхимы почек
Паренхиматозные заболевания почек являются самыми распространенными причинами вторичной гипертензии. Наличие пальпируемых двусторонних образований в верхней части живота характерно для поликистоза почек и служит основанием для ультразвукового исследования. Последний метод сегодня практически заменил внутривенную урографию при изучении анатомии почек. При внутривенной урографии приходится вводить потенциально нефротоксичное контрастное вещество, тогда как ультразвуковой метод является неинвазивным и позволяет получить всю необходимую информацию о размерах и форме почки, толщине коркового слоя, наличии обструкции мочевых путей и образований в почках. С целью скрининга паренхиматозных заболеваний почек целесообразно выполнять анализ мочи (белок, эритроциты и лейкоциты) и измерять сывороточную концентрацию креатинина. Эти исследования целесообразно проводить всем больным АГ (см. раздел 3.4). Если повторные анализы мочи и сывороточные уровни креатинина нормальны, то можно исключить наличие паренхиматозного заболевания почек. Наличие эритроцитов и лейкоцитов следует подтвердить с помощью микроскопии мочи. Если результаты указанных тестов оказываются положительными, необходимо детальное обследование почек.
9.2. Реноваскулярная гипертензия
Реноваскулярная АГ находится на втором месте среди причин вторичной гипертензии. В специализированных центрах ее диагностируют примерно у 2% взрослых больных с повышенным АД. Она обусловлена стенозом почечных артерий, который в пожилом возрасте часто имеет атеросклеротическое происхождение. Доля фибромышечной дисплазии среди всех случаев реноваскулярной гипертензии составляет 25%. Ее чаще всего обнаруживают у молодых людей. Реноваскулярную гипертензию следует подозревать при внезапном развитии или прогрессировании АГ, а также при наличии высокой гипертензии, которая плохо поддается лечению. Признаки стеноза почечной артерии включают в себя шум в проекции почечных сосудов, гипокалиемию и прогрессирующее ухудшение функции почек. Однако эти симптомы отсутствуют у многих пациентов. С целью скрининга можно измерять продольный размер почки с помощью ультразвукового метода. Обычно критерием диагноза реноваскулярной гипертензии считают разницу длины двух почек более 1,5 см, хотя этот признак обнаруживают только у 60-70% больных реноваскулярной гипертензией. Цветная допплерография часто позволяет выявить стеноз почечной артерии, особенно локализующийся ближе к месту ее отхождения от аорты. Кроме того, этот метод позволяет определить индекс резистентности, который дает возможность предсказать результаты ангиопластики и стентирования. Методом выбора в диагностике реноваскулярной гипертензии считают трехмерную магнитно-резонансную ангиографию с гадолинием. Высокой чувствительностью обладает спиральная КТ, хотя она предполагает введение контрастного вещества и достаточно высокое облучение. Если велика вероятность наличия стеноза почечной артерии, диагноз должен быть подтвержден с помощью дигитальной ангиографии. Это инвазивное исследование остается золотым стандартом диагностики заболевания. Для определения концентрации ренина в почечных сосудах необходима катетеризация, а инвазивность и сложность метода не компенсируются его чувствительностью или специфичностью. Этот метод не может быть рекомендован для скрининга.
Подходы к лечению реноваскулярной гипертензии вызывают споры, учитывая ограниченное число крупных клинических исследований и трудности оценки вероятного ответа на реваскуляризацию почечных сосудов. Однако имеющиеся данные позволяют дать следующие рекомендации.
1) Рефрактерная АГ (т.е. сохранение повышенного АД, несмотря на лечение, по крайней мере, тремя антигипертензивными препаратами, включая диуретик), а также прогрессирующее снижение функции почек являются показаниями к реваскуляризации.
2) Хирургическая реваскуляризация постепенно вытесняется ангиопластикой.
3) Ангиопластика является методом выбора при фибромышечной дисплазии и характеризуется высокой эффективностью, т.е. стойкой нормализацией АД или улучшением ответа на медикаментозную терапию. Частота ответа ниже при атеросклерозе, при котором чаще развивается рестеноз; его риск можно снизить с помощью стентирования, которое практически всегда выполняют после ангиопластики у больных атеросклеротическим стенозом почечных артерий.
4) В ряде исследований сравнивали результаты медикаментозной терапии и ангиопластики; при их мета-анализе выявлено небольшое, но достоверное преимущество инвазивного лечения. Однако его результаты зависят от навыков и опыта врача, и фармакотерапия сохраняет большое значение для больных атеросклеротическим стенозом почечных артерий.
Фармакотерапию следует считать методом выбора при сохранении функции почек, наличии ответа на лечение, умеренного стеноза почечной артерии и длительного (более 10 лет) анамнеза АГ. Учитывая высокий риск прогрессирования атеросклеротических изменений, лечение должно предполагать интенсивную модификацию образа жизни, применение аспирина в низкой дозе, статинов и различных антигипертензивных препаратов. Целесообразно использование тиазидных диуретиков в адекватных дозах в сочетании с антагонистами кальция, к которым могут быть добавлены блокаторы ренин-ангиотензиновой системы, если отсутствует двусторонний стеноз почечных артерий. Такая терапия позволяет снизить АД у большинства больных с реноваскулярной гипертензией. Лечение может осложниться острым снижением функции почек и нарастанием уровня креатинина за счет ухудшения перфузии дистальнее стеноза. Эти проблемы чаще возникают при применении блокаторов ренин-ангиотензиновой системы, однако уровень креатинина в сыворотке обычно нормализуется после прекращения терапии.
9.3. Феохромоцитома
Феохромоцитома – очень редкая причина вторичной гипертензии (0,2-0,4% случаев повышенного АД). Ее ежегодная распространенность составляет 2-8 на 1 млн населения. Феохромоцитома может быть наследственной или приобретенной. АГ развивается примерно у 70% больных. Примерно у половины пациентов она является стабильной, а у другой половины проявляется гипертоническими кризами, сопровождающимися головной болью, потливостью, сердцебиениями и бледностью. Диагноз устанавливают на основании повышения уровней катехоламинов или их метаболитов в плазме или моче. Дополнительно могут быть проведены функциональные пробы. Самой высокой чувствительностью (97-98%) характеризуется измерение свободных метанефринов в плазме в сочетании с определением фракций метанефринов в моче.Однако первый метод недостаточно доступен, поэтому чаще всего определяют фракции метанефринов и катехоламины в моче. Если их уровни очень высоки, то дополнительные исследования не требуются. С другой стороны, умеренное повышение содержания этих веществ в плазме или моче позволяет заподозрить феохромоцитому, однако в этом случае могут быть выполнены функциональные пробы со стимуляцией глюкагоном или подавлением клонидином. Учитывая ограниченную специфичность функциональных проб, при пограничных изменениях лабораторных показателей многие клиницисты предпочитают сразу проводить визуализирующие исследования. Проба с глюкагоном может быть проведена после эффективного лечения альфа-адреноблокатором для профилактики резкого повышения АДпосле инъекции гормона. Пробу с клонидином считают отрицательной, если отмечается значительное снижение уровней катехоламинов в плазме.
Если установлен диагноз феохромоцитомы, необходимо определить локализацию опухоли. В 95% случаев она находится в надпочечниках или вблизи них. Опухоль часто имеет крупные размеры и иногда может быть выявлена с помощью ультразвукового метода. Однако наиболее чувствительными методами диагностики (98-100%) являются КТ и особенно МРТ, хотя МРТ может характеризоваться низкой специфичностью (50%). В дополнение к КТ или МРТ может быть проведена сцинтиграфия с мета-йодобензилгуанидином, которая позволяет выявить феохромоцитому, локализующуюся вне надпочечников, и метастазы злокачественной опухоли (10% случаев феохромоцитомы), а также подтвердить наличие феохромоцитомы, диагностированной с помощью КТ или МРТ. Существует несколько семейных заболеваний, которые ассоциируются с высокой частотой феохромоцитомы, в том числе множественная эндокринная неоплазия 2-го типа (МЭН2), болезнь Гиппель-Ландау и нейрофиброматоз 1-го типа. Семейные параганглиомы также сочетаются с феохромоцитомой. В связи с этим целесообразно рекомендовать проведение генетических тестов больным и их родственникам, особенно если феохромоцитома ассоциируется с наследственными синдромами. К настоящему времени установлены мутации 5-ти генов, которые приводят к развитию семейных заболеваний, ассоциирующихся с феохромоцитомой. Основным методом лечения является удаление опухоли. Пациента следует подготовить к операции. С этой целью назначают альфа-адреноблокатор. Затем могут быть использованы бета-блокаторы. В последующем может быть выполнена резекция опухоли, которую сегодня часто проводят лапароскопически. После операции показано адекватное возмещение объема жидкости. Это необходимо, так как феохромоцитома вызывает натрийурез, сужение вен и значительное уменьшение объема крови.
9.4. Первичный альдостеронизм
Первичный альдостеронизм вызывает большие споры в последние годы. Это связано с тем, что его распространенность у больных первичной гипертензией в различных исследованиях колеблется от 1 до 11%. В качестве метода скрининга рекомендуется определять уровень калия в сыворотке, однако гипокалиемия на начальной стадии болезни определяется только у небольшого числа больных. В 30% случаев причиной первичного альдостеронизма являются аденомы надпочечников, которые встречаются чаще у женщин и реже у детей. В 70% случаев наблюдается гиперплазия надпочечников. В редких случаях выявляют карциному надпочечников и альдостеронизм, наследуемый по аутосомно-доминантному типу. Клинически развивается умеренная или тяжелая АГ, которая не поддается лечению. Наследственный гиперальдостеронизм обычно проявляется в детском возрасте. Первичный альдостеронизм может сочетаться с феохромоцитомой, гиперпаратиреозом и акромегалией. Высказывалось предположение, что исключать первичный альдостеронизом следует только у пациентов с гипокалиемией и истинной резистентной гипертензией. Для подтверждения диагноза могут быть выполнены проба с флудрокортизоном (применение гормона в течение 4-х дней не приводит к снижению уровня альдостерона в плазме ниже порогового значения) или измерение активности альдостерона и ренина в плазме. В последние годы стали чаще измерять коэффициент альдостерон/ренин. Однако уровень альдостерона может быть высоким, а активность ренина – низкой у пожилых людей и афроамериканцев. Кроме того, высокое значение этого коэффициента наблюдается при хронических заболеваниях почек, когда высокий уровень калия стимулирует секрецию альдостерона, а также при редких генетических мутациях, сопровождающихся повышенными уровнями альдостерона. При мета-анализе 19 исследований у 10 396 больных была выявлена высокая вариабельность коэффициента альдостерон/ренин. Значения его были высокими у 5,5-39% больных, однако аденому выявили только в 0-6,5%случаев. В связи с этим польза показателя остается спорной. С целью визуализации аденомы сегодня используют КТ, МРТ или радиоизотопный метод с меченым холестерином. КТ и МРТ обычно позволяют исключить гиперплазию. Ложноположительные результаты встречаются достаточно часто, так как узелковую гиперплазию клубочковой зоны выявляют даже при наличии аденом, выделяющих гормон, тогда как выявленная аденома может оказаться нефункционирующей. Это означает, что при проведении КТ или МРТ необходимо дополнительно производить забор венозной крови из надпочечников. Без этого у 25% больных аденомой, диагностированной при КТ, адреналэктомия оказывается необоснованной. Резекцию надпочечника проводят лапароскопическим методом. В опубликованных сериях наблюдений случаи смерти зарегистрированы не были, а риск осложнений был минимальным. Средняя длительность пребывания в стационаре после операции составила 2,6 дня. Перед операцией и при гиперплазии надпочечников показано лечение антагонистом альдостерона, таким как спиронолактон. Однако этот препарат вызывает побочные реакции, в частности гинекомастию. В этом случае может быть использован эплеренон, хотя в рекомендуемых дозах он по эффективности уступает спиронолактону.
9.5. Синдром Кушинга
Распространенность синдрома Кушинга в общей популяции составляет менее 0,1%. Частота АГ у таких больных достигает примерно 80% (50% у детей и подростков). Обычно синдром Кушинга диагностируют на основании характерных внешних признаков. Практичным и надежным методом диагностики является измерение суточной экскреции кортизола с мочой. Если она превышает 110 ммоль (40 мкг), то это с высокой вероятностью указывает на синдром Кушинга. Диагноз подтверждают с помощью двухдневной пробы с дексаметазоном в низкой дозе (0,5 мг каждые 6 ч; 8 доз) или ночной пробы с дексаметазоном (1мг в 23.00). В первом случае экскреция кортизола с мочой, превышающая 27 ммоль (10 мкг) на второй день, подтверждает наличие синдрома Кушинга. Во втором случае критерием диагноза является концентрация кортизола в плазме более 140 ммоль/л (5 мкг/дл) в 8.00. Нормальные результаты проб исключают наличие синдрома Кушинга. Недавно в качестве более простого метода диагностики было предложено измерять уровень кортизола в сыворотке или слюне в середине ночи или рано утром. Для дифференциальной диагностики различных форм синдрома используют дополнительные методы исследования.
9.6. Обструктивное апноэ во сне
Обструктивное апноэ во сне характеризуется повторными эпизодами нарушения дыхания, связанным со спадением дыхательных путей на вдохе. Эти эпизоды приводят к снижению насыщения крови кислородом. Обструктивное апноэ во сне следует исключить у больных ожирением, особенно если АГ оказывается резистентной к стандартной фармакотерапии. Кроме того, показанием к исключению этого состояния являются результаты суточного амбулаторного мониторирования АД – non-dippers. Симптомы обструктивного апноэ во сне включают сонливость в течения дня, нарушение концентрации внимания, беспокойный сон, эпизоды нехватки воздуха во время сна, приступы апноэ, зафиксированные свидетелями, никтурию, раздражительность и изменения личности, снижение либидо и увеличение риска дорожно-транспортных происшествий. С целью скрининга целесообразно использование валидированных вопросников (Epworth Sleepiness Scale, Berlin Questionnaire). Золотым стандартом диагностики остается полисомнография. Для оценки наличия и тяжести синдрома используют индекс апноэ-гипопноэ (число эпизодов апноэ или гипопноэ за 1 ч). Значение индекса 5-15 указывает на легкое апноэ, 15-30 – на умеренное, более 30 – на тяжелое. Если не проводится лечение, обструктивное апноэ во сне может оказывать нежелательное действие на сердечно-сосудистую систему, включая активацию симпато-адреналовой системы, окислительный стресс, воспаление и эндотелиальную дисфункцию. Синдром может способствовать повышению АД у значительной части больных АГ. Прессорный эффект обычно связывают с нарушением рефлекторной регуляции функции сердечно-сосудистой системы и изменениями эндотелия . Снижение массы тела у больных ожирением вызывает уменьшение тяжести синдрома. С целью его лечения используют специальные устройства, обеспечивающие дыхание под положительным давлением.
9.7. Коарктация аорты
Коарктация аорты – редкая причина АГ у детей и молодых людей. Диагноз можно заподозрить на основании данных физикального обследования. В области передней поверхности грудной клетки и спины выслушивается среднесистолический шум, которым со временем может стать постоянным. Пульс на бедренной артерии отсутствует и замедлен по сравнению с пульсом на лучевой артерии. АД повышено на руках и снижено или не измеряется на ногах. После восстановления дефекта или стентирования, особенно у взрослых, АГ может сохраняться за счет гемодинамических или сосудистых изменений, поэтому многие больные нуждаются в продолжении антигипертензивной терапии.
9.8. Лекарственная гипертензия
Препаратами, вызывающими повышение АД, являются пероральные контрацептивы, стероиды, нестероидные противовоспалительные препараты, кокаин и амфетамины, эритропоэтин, циклоспорин, такролимус. При сборе анамнеза следует уточнять проводимую терапию.Целесообразно тщательно контролировать прием лекарств, которые могут вызвать увеличение АД.
10. Наблюдение
| Рамка 22. Наблюдение больных |
|---|
|
Во время подбора антигипертензивной терапии пациентов следует наблюдать каждые 2-4 нед, чтобы скорректировать лечение (увеличение доз, присоединение других средств, снижение доз или отмена препарата) с учетом достигнутого АД и переносимости. В этот период желательно, чтобы пациент самостоятельно измерял АД в домашних условиях. Когда достигнуто целевое АД и контроль других факторов риска, кратность визитов можно значительно снизить. Пациентов с низким сердечно-сосудистым риском и легкой АГ можно наблюдать каждые 6 мес, тогда как пациенты с более высоким исходным АД и высоким или очень высоким сердечно-сосудистым риском должны посещать врача чаще. Частые визиты обоснованны у больных, получающих немедикаментозное лечение, так как
1) приверженность лечению низкая;
2) ответ на терапию варьирует;
3) при неэффективности следует своевременно назначить фармакотерапию.
Измерение АД в домашних условиях позволяет увеличить интервалы между визитами к врачу. Упростить схему наблюдения позволяют также современные технологии, например, телепередача результатов измерений АД в офис врача; такой подход позволяет добиться более высокой приверженности лечению. Однако не рекомендуется значительно увеличивать интервалы между визитами, так как они позволяют обеспечить хорошие взаимоотношения между врачом и больным. Если в течение 6 мес не удается достичь целевых показателей АД или контроль АД утрачивается, то пациента следует направить в специализированную клинику. Периодически необходимо оценивать состояние органов-мишеней, так как регресс имеющихся изменений или отсутствие их прогрессирования имеет важное прогностическое значение (см. раздел 4.5). Дать четкие рекомендации по поводу сроков обследования трудно, однако следует помнить, что экскреция белка с мочой может уменьшиться в течение нескольких недель после начала лечения, тогда как уменьшение массы левого желудочка обычно выявляют не ранее, чем через 1 год. В случае прекращения лечения у больных АГ АД рано или поздно вновь увеличивается до исходных значений. Тем не менее, при длительном сохранении контроля АД иногда удается уменьшить число лекарственных препаратов или их дозы, особенно на фоне активного улучшения образа жизни. Это связано с тем, что эффективная антигипертензивная терапия позволяет, по крайней мере частично, уменьшить анатомические изменения сосудов (т.е. ремоделирование артериол), которые поддерживают повышенное АД. Однако подобные попытки необходимо предпринимать под постоянным контролем АД, предпочтительно в домашних условиях.
11. Внедрение рекомендаций
Уменьшение разрыва между рекомендациями экспертов и неадекватным контролем АД в клинической практике
Хотя убедительно установлено, что АГ является одним из главных сердечно-сосудистых факторов риска, а антигипертензивная терапия значительно снижает этот риск, тем не менее исследования, проводившиеся на различных континентах, включая несколько стран Европы, показали, что:
1) значительная часть пациентов не знает о своем заболевании или, если знает, не получает лечение,
2) целевые показатели АД достигаются редко независимо от того, какие антигипертензивные препараты получает больной и кто его наблюдает – специалист или врач общей практики. Особенно редко удается достичь контроля систолического АД, особенно его более низких целевых значений (менее 130 мм рт. ст.) у больных сахарным диабетом и пациентов группы очень высокого риска. Это объясняет, почему АГ остается ведущей причиной смертности и сердечно-сосудистой заболеваемости во всем мире. В связи с этим необходимо чаще диагностировать АГ и чаще проводить эффективную терапию (рамка 23).
| Рамка 23. Как улучшить выполнение рекомендаций |
|---|
|
Настоящие рекомендации должны помочь в осуществлении этой цели.Однако публикация рекомендаций сама по себе не решает поставленных задач. Процесс их внедрения в клиническую практику предполагает постоянное обучение врачей и аудит. Для успешного применения рекомендаций на практике необходимы совместные усилия медицинских работников, которые должны осознавать важность существующей проблемы. Подходы к лечению АГ могут отличаться в разных странах Европы. В некоторых странах профилактика сердечно-сосудистых заболеваний, в частности выявление и контроль АГ, осуществляется врачами общей практики, а также медицинскими сестрами и другими медицинскими работниками. В других странах более активное участие в этом процессе принимают специалистыи врачи стационаров. В связи с этим международные рекомендации должны быть адаптированы к национальным условиями с учетом социально-экономической ситуации и структуры системы здравоохранения.
Чтобы обеспечить внедрение рекомендаций в клиническую практику, необходимо, чтобы они были приняты национальными обществами, занимающимися проблемой АГ. Настоящие рекомендации были подготовлены в тесном сотрудничестве с четвертой рабочей группой Европейских и других обществ по профилактике сердечно-сосудистых болезней. Соответственно, они согласуются с рекомендациями этой рабочей группы, которые также опубликованы в 2007 г. Партнерами ESH и ESC являются Европейское общество атеросклероза, Европейская ассоциация по изучению сахарного диабета, Международная федерация диабета (Европа), Европейское общество общей практики/семейной медицины, Европейская сердечная сеть и Международное общество поведенческой медицины. Это сотрудничество имеет большое значение, так как врачи вряд ли воспримут рекомендации, которые подготовлены неизвестными им организациями.
Необходимо четко представлять себе препятствия внедрению рекомендаций в клиническую практику. Первым барьером является незнание рекомендаций. Этому способствует большое число рекомендаций, которые получают врачи, их дублирования многими научными обществами, национальными организациями и медицинскими агентствами. Причиной путаницы могут быть даже небольшие различия между разными рекомендациями. Кроме того, у врачей часто возникают подозрения, что рекомендации могут отражать неадекватные научные представления экспертов, а также подвержены влиянию внешних факторов, в частности фармацевтических и страховых компаний. Врачи осознают, что они занимаются лечением конкретных больных, которые часто отличаются друг от друга, в то время как рекомендации освещают проблему лечения заболевания в целом. Этот аспект был учтен в рекомендациях ESH/ESC 2003 г. и настоящих рекомендациях.
Препятствия к внедрению рекомендаций возникают не только со стороны врача, но и больного. Основной проблемой является приверженность немедикаментозным методам лечения и длительной комбинированной терапии. Модификация образа жизни часто рассматривается как более дешевая альтернатива затратам на медикаментозное лечение, хотя пациенты часто нуждаются в профессиональной помощи экспертов в области поведенческой медицины.
Барьером к внедрению рекомендаций может служить и сама система медицинской помощи. Организаторы медицинской помощи нередко считают, что лечение АГ предполагает только короткие визиты к врачу и соответствующим образом компенсируют его труд. Они часто рассматривают рекомендации как инструмент снижения затрат и возмещают их только в группах высокого риска, выделенных на основании спорных критериев. В связи с этим к осуществлению всеобъемлющей программы профилактики сердечно-сосудистых заболеваний необходимо активно привлекать организаторов здравоохранения.
Комитет осознает, что факт появления этих рекомендаций сам по себе не приведет к каким-либо изменениям, однако они могут служить частью стратегии сердечно-сосудистой профилактики, благодаря тому, что предполагают:
- согласование действий всех сторон, занимающихся выявлением и контролем АГ;
- основу для обучения и тренинга;
- основу для разработки национальных рекомендаций и/или адаптация рекомендаций с учетом национальной системы здравоохранения и доступных средств;
- идентификацию наиболее адекватных инструментов контроля АГ;
- основу для решения фармакоэкономических вопросов.
- Рабочая группа по лечению артериальной гипертензии Европейского общества гипертензии (ESH) и Европейского общества кардиологов (ESC)
Со списком литературы можно ознакомиться на сайте Европейского общества кардиологов escardio.org


