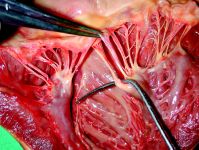
Ишемическая митральная недостаточность – тяжелое заболевание с плохим прогнозом. Прогрессирующее и часто коварное течение, обусловленное коронарной патологией, значительно отличает ишемическую митральную недостаточность от митральной недостаточности, связанной с другими причинами.
Ишемическая митральная недостаточность является следствием инфаркта миокарда, всегда предшествующего появлению митральной регургитации. При этом состояние створок и подклапанных структур не меняется. Таким образом, термин ишемической митральной недостаточности исключает другие этиологические причины митральной недостаточности - инфекционные, дегенеративные заболевания соединительной ткани, разрыв хорд, врожденный пролапс створок и др. Митральная недостаточность, ассоциирующаяся с ишемической кардиомиопатией и дисфункцией левого желудочка - похожее явление, но все же этиологически отличное от истинной ишемической митральной недостаточности. Интермитирующая митральная недостаточность, обусловленная преходящей ишемией, как правило, встречается нечасто и манифестирует параллельно со стенокардией.
Общие сведения
Механизм ишемической митральной недостаточности
Клиника, диагностика и лечение острой ишемической митральной недостаточности
Клиника, диагностика и лечение хронической ишемической митральной недостаточности
Ишемическая митральная недостаточность может развиться остро из-за разрыва папиллярной мышцы или постепенно, вследствие постинфарктного ремоделирования полости левого желудочка. Таким образом, ишемическая митральная недостаточность является болезнью не клапана, а миокарда. Однако, митральная недостаточность, связанная с другими причинами, также оказывает вторичное воздействие на миокард.
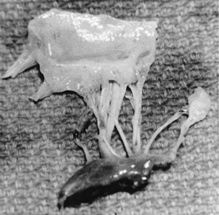
Разрыв папиллярной мышцы
У 17-55% больных после острого инфаркта миокарда появляется систолический шум митральной недостаточности или эхокардиографическое подтверждение митральной регургитации. Среди больных, подвергшихся зондированию сердца в течение 6 часов после инфаркта миокарда, у 18% выявлена митральная недостаточность. У 3,4% этих пациентов наблюдалась митральная недостаточность III ст., у 7,2% - II ст., однако, у многих больных эти явления со временем исчезают. Наиболее характерно появление митральной недостаточности после трансмуральных задних инфарктов миокарда.
Разрыв папиллярной мышцы наиболее опасный прогностический признак. Задняя папиллярная мышца вовлекается в инфаркт миокарда в 3-6 чаще, чем передняя. В большинстве случаев характерен частичный разрыв. Полный разрыв происходит обычно в течение первой недели после острого инфаркта миокарда, в то время как частичный может быть отсрочен до 3 месяцев.
Острый инфаркт миокарда также может привести к развитию выраженной митральной недостаточности и без разрыва папиллярной мышцы. Это обусловлено дисфункцией последней при вовлечении ее в зону инфаркта, чаще геморрагического.
Хроническая митральная недостаточность связана с дисторсией задней папиллярной мышцы вследствие дилатации полости левого желудочка, приобретающей форму шара. Параллельно с этим происходит расширение (> 3 см в диаметре) левого атриовентрикулярного отверстия. Кольцо митрального клапана имеет тенденцию расширяться пропорционально с объемом полости левого желудочка.
Митральный клапан состоит из шести анатомических компонентов: створки, хорды, кольцо, папиллярные мышцы, стенка левого желудочка и левого предсердия. Митральное кольцо имеет форму седла (гиперболический параболоид с двунаправленным искривлением). В области геометрического центра фиброзное кольцо митрального клапана имеет изгиб в цефальном направлении, а в области комиссур - в каудальном.
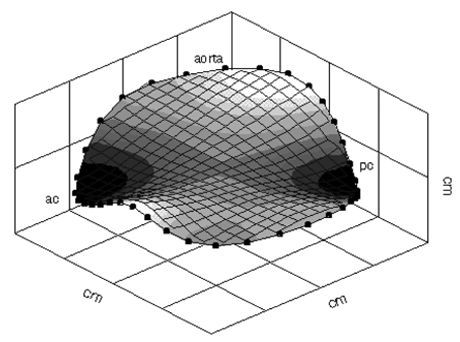
Форма кольца митрального клапана
В течение изоволюмического сокращения левого желудочка и закрытия митрального клапана происходит наполнение левого предсердия до момента открытия аортального клапана. В это время поток через митральный клапан быстро уменьшается, створки смыкаются и выгибаются в сторону предсердия. В течение систолы левое предсердие быстро заполняется, кольцо клапана при этом незначительно смещается в сторону предсердия и затем постепенно опускается в на 1-1,5 см сторону верхушки во время систолы желудочка. Кроме того, кольцо асимметрично сокращается с уменьшением площади клапана в среднем на 27%. Немедленно после окончания систолы предсердия, когда давление в левом желудочке превышает давление в предсердии, створки в течение 20-60 миллисекунд приближаются друг к другу. С учетом того, что площадь створок митрального клапана в два раза больше площади левого атриовентрикулярного отверстия, линия их смыкания находится в плоскости кольца митрального клапана. При закрытии клапана 30% передней и 50% задней створки плотно соприкасаются между собой. Напряжение хорд ограничивает восходящее движение створок, пик напряжения совпадает с ранней систолой, медленно снижается в поздней систоле и быстро падает в начале диастолы. Папиллярные мышцы начинают укорачиваться (2-4 мм) во время поздней диастолы синхронно с миокардом стенки левого желудочка. Во время систолы желудочек закручивается против часовой стрелки.
Площадь митрального клапана достигает максимума во время диастолы (до 3,9±0,7 cм2/м2), при этом его форма изменяется асимметрично: максимум удлинения периметра митрального кольца происходит вследствие увеличения задней полуокружности. Несмотря на то, что пиковый кровоток через клапан регистрируется в диастоле, створки достигают максимально открытого положения прежде, чем достигается пиковый поток и начинают закрываться, в то время как поток все еще ускоряется.
Левый желудочек в течение ранней диастолы и периода быстрого заполнения, расширяется, прежде всего, по поперечной и намного меньше - по продольной оси. В течение ранней диастолы толщина стенки левого желудчка уменьшается и желудочек быстро раскручивается, вращаясь по часовой стрелке, с замедлением к скорости с середине и окончанию диастолы.
Механизм ишемической митральной недостаточности
Острая ишемическая митральная недостаточность
Многочисленные исследования доказали, что потеря только функции сокращения папиллярной мышцы в результате острой ишемии не приводит к митральной регургитации. Возникающие изменения в динамике сокращения папиллярной мышцы, вызывают не только пролапс створок за счет эффекта уменьшения натяжения, но и отражаются на кооптации створок. Таким образом, ишемическая митральная недостаточность – это результат нарушения сложных геометрических и временных параметров работы митрального аппарата, которые не доказуемы стандартными методами диагностики и не могут быть заметными на остановленном сердце во время операции.
Хроническая ишемическая митральная недостаточность
Хроническая ишемическая митральная недостаточность у большинства пациентов развивается из-за ограничения подвижности створок вследствие фиброза и атрофии папиллярных мышц, при этом не наблюдается удлинения хорд и папиллярных мышц. У больных с существовавшим пролапсом митрального клапана, инфаркт миокарда может привести к тому, что на ранее компетентном клапане появляется регургитация. При этом площадь митрального кольца расширяется на 60% в течение всего периода систолического изгнания за счет того, что более подвижная часть основания задней створки растягивается одновременно с дисторсией задней папиллярной мышцы.
Таким образом, геометрические изменения митрального аппарата, которые приводят к его острой недостаточности, являются часто повторяющимися, но чрезвычайно тонкими (< 5 мм) и недоступны клиническим методам исследования. Хроническая митральная недостаточность приводит к большим изменениям (1-2 см), которые вызывают умеренное расширение кольца и комплексное натяжение створок, нарушающее их кооптацию.
Патофизиология
Острая митральная недостаточность немедленно приводит к перегрузке объемом левого желудочка, увеличивает его преднагрузку и уменьшает систолический выброс. Объем регургитации зависит от степени некомпетентности клапана. Митральная недостаточность увеличивает раннее диастолическое заполнение желудочка и уменьшает систолическое напряжение и эластичность его стенки. Потребление кислорода миокардом не изменяется из-за снижения напряжения стенки в поздней систоле. Увеличение минутного объема кровообращения достигается увеличением ударного объема. Однако, если митральная регургитация достаточно большая, поток через аортальный клапан, то есть сердечный выброс, снижается. Давление в левом предсердии и давление заклинивания в легочной артерии повышаются, последнее приводит к правожелудочковой недостаточности.
Естественное течение
Митральная недостаточность после острого инфаркта миокарда исчезает в течение госпитального периода у 15% пациентов, еще у 15% больных симптомы митральной недостаточности ликвидируются в течение нескольких месяцев. В то же время среди больных с отсутствием митральной недостаточности у 12% она появляется в отдаленном периоде после инфаркта миокарда.
Даже умеренная степень митральной регургитации удваивает госпитальную и 3-х летнюю смертность по сравнению с пациентами без митральной недостаточности. Без хирургического вмешательства средняя выживаемость после разрыва папиллярных мышц не превышает 3-4 суток. Некоторые пациенты с частичным разрывом или разрывом одной головки папиллярной мышцы переживают несколько недель или месяцев после инфаркта миокарда. При тяжелой (III или IV) степени митральной недостаточности госпитальная летальность составляет 24%, а годичная - 52%.
Хроническая митральная недостаточность I ст. у пациентов с симптомами коронарной недостаточности увеличивает 1-летнюю смертность до 10%, II ст. – до 17%, III ст. – до 40 %, по сравнению с 6% летальностью у больных без митральной недостаточности.
Клиника, диагностика и лечение острой ишемической митральной недостаточности
Острая тяжелая ишемическая митральная недостаточность осложняет течение заболевания у 0,4-0,9% всех пациентов с инфарктом миокарда. У 2\3 пациентов она связана с разрывом задней папиллярной мышцы, несмотря на то, что передний инфаркт миокарда развивается более часто. Средний возраст больных составляет 60 лет. Митральная недостаточность чаще наблюдается у мужчин, чем у женщин. Разрыв папиллярной мышцы может произойти уже первый день после инфаркта, и почти всегда в течение 7 дней (в среднем – 4 суток).
Острая ишемическая митральная недостаточность обычно проявляется болью в груди и/или одышкой. У большинства больных появляется дующий голосистолический шум с акцентом на верхушке. Разрыв папиллярной мышцы клинически часто проявляется отеком легких или кардиогенным шоком, системной гипотонией, олигурией, ацидозом, и требует быстрого вмешательства для спасения жизни.
У большинства пациентов сохраняется синусовый ритм. У 50% больных присутствуют изменения, характерные для острого инфаркта миокарда - подъем сегмента ST в переднеперегородочной, боковой или чаще задней стенки левогожелудочка. Блокада правой или левой ножки пучка Гиса характерна для больных с постинфарктным ДМЖП.
На рентгенограмме грудной клетки отмечаются явления венозного застоя. Тень сердца, как правило, не увеличена.
Трансторакальная и транспищеводная ЭхоКГ позволяют оценить степень митральной регургитации и подтверждают отсутствие патологии со стороны створок митрального клапана и нарушение сократимости стенки левого желудочка, а также патологию со стороны папиллярных мышц. Левое предсердие, как правило, не увеличено. Фракция выброса снижается, но не отражает степень поражения левого желудочка.
Несмотря на неустойчивость гемодинамики, большинство пациентов требует диагностического зондирования сердца, прежде всего для определения коронарной патологии. Приблизительно у половины пациентов выявляется однососудистое поражение, чаще правой коронарной артерии, у второй половины – трехсосудистое поражение. Левая вентрикулография показывает увеличение объема левого желудочка, выраженную недостаточность митрального клапана, повышение КДД левого желудочка. Фракция выброса, как правило, не снижается менее 40%. Зондирование правых отелов сердца обычно выявляет повышение давления в легочной артерии и "v" волны, достигающие 40 мм рт.ст и выше. Насыщение смешанной венозной крови кислородом часто значительно ниже 50%, что отражает снижение сердечного выброса с уменьшением индекса до 1,0-2,9 л.мин/м2.
Безотлагательность и агрессивность хирургического лечения зависят от наличия или отсутствия кардиогенного шока и/или сердечной недостаточности. В отделении интенсивной терапии должен быть налажен непрерывный мониторинг ЭКГ, центральной гемодинамики (включая давление заклинивания в легочной артерии и сердечного выброса), периферической сатурации кислорода, газов крови (как артериальной, так и венозной), насыщенности кислорода и pH.
Адекватность гемодинамики должна быть оценена до того развития фатальных последствий. Критериями кардиогенного шока являются: системная гипотония (систолическое давление < 80 мм рт.ст., среднее давление < 55 мм рт. ст.), насыщение смешанной венозной крови кислородом < 50%, сердечный индекс < 2,0 л.мин/м2, метаболический ацидоз, олигурия и снижение периферической микроциркуляции (бледность кожных покровов, холодные конечности, слабый периферический пульс). В этой связи, все необходимые диагностические исследования должны быть выполнены настолько быстро насколько возможно.
У пациентов с отсутствием критических изменений гемодинамики возможна дополнительная инфузия кристаллоидных или коллоидных растворов, способных увеличить сердечный выброс и восстановить диурез. Применяются наркотические аналгетики, которые меньше повреждают функцию миокарда или вызывают гипотонию. Инотропные препараты, также как и периферические вазодилататоры, используются для поддержания сердечного выброса. У наиболее критических пациентов отсутствие эффекта от медикаментозной терапии является основанием для применения интрааортальной контрпульсации.
Для пациентов с острым инфарктом миокарда и митральной недостаточностью I или II ст. срочная реваскуляризация миокарда способна предотвратить прогрессирование митральной недостаточности, развитие кардиогенного шока и сердечной недостаточности. Это может быть достигнуто тромболизисом, ЧТКА, или стентированием. Немедленное хирургическое вмешательство является методом выбора для большинства больных, однако у пациентов без разрыва папиллярной мышцы может быть использована ЧТКА или тромболитическая терапия в надежде на уменьшение размера инфаркта миокарда и, соответственно, митральной недостаточности. Теоретически ЧТКА или тромболизис, выполненные в течение 4 часов после начала острого инфаркта миокарда могут уменьшить как размер, так и степень митральной регургитации. Однако, у многих пациентов они не способны обеспечить благоприятный результат.
Операция при острой ишемической митральной недостаточности часто носит экстренный характер. В некоторых случаях у критических больных с целью сокращения времени подключения искусственного кровообращения не проводится забор внутренней грудной артерии. Эстракорпоральное кровообращение проводится в режиме нормотермии, защита миокарда – гипотермическая кровяная анте- и ретроградная кардиоплегия. До манипуляций на митральном клапане проводится наложение дистальных анастомозов на задней и боковой поверхности сердца, так как выполнение этой процедуры после протезирования клапана может привести к разрыву задней стенки левого желудочка.
Большинство пациентов с острой ишемической митральнойнедостаточностью имеют маленькие размеры левого предсердия, что затрудняет манипуляции на клапане, поэтому для лучшей экспозиции можно использовать доступ через правое предсердие с рассечением межпредсердной перегородки и крыши левого предсердия.
Протезирование митрального клапана – операция выбора, особенно для пациентов, находящихся в критическом состоянии, так как пластические процедуры на клапане в случае неуспеха потребуют повторной остановки сердца. Выбор протеза (механический или биологический) зависит от возраста больного, ожидаемой продолжительности жизни, возможных проблем с постоянной антикоагулянтной терапией. При протезировании необходимо сохранение подклапанных структур для предотвращения повреждения фиброзного каркаса левого желудочка и снижения фракции выброса.
В интра- и раннем послеоперационном периоде первоначально используются инотропные препараты и периферические вазодилятаторы, но если с помощью этих препаратов невозможно поддержать адекватный сердечный выброс, необходимо немедленно использовать контрпульсацию или один из вариантов обхода левого желудочка. Если острая сердечная недостаточность и использование механической поддержки кровообращения прогнозируется на дооперационном этапе, то в такой ситуации лучше использовать биопротез, так как он не подвержен тромбозу во время работы устройства вспомогательного кровообращения.
Результаты
Непосредственные результаты экстренного протезирования митрального клапана при ишемической митральной недостаточности до настоящего времени оставляют желать лучшего. Госпитальная летальность колеблется от 31% до 69%. Большинство хирургов не рекомендуют использовать пластические процедуры при экстренном вмешательстве по причинам, изложенным выше. Сохранение хордального аппарата, улучшающее функцию левого желудочка, позволяет снизить летальность до 22%. Вместе с тем, при медикаментозном лечении смертность приближается к 100%. Факторы, влияющие на летальность включают пожилой возраст, кардиогенный шок, сопутствующие заболевания, количество инфарктов миокарда в анамнезе и задержка операции. 5-летняя выживаемость среди пациентов, переживших послеоперационный период составляет 50%.
Клиника, диагностика и лечение хронической ишемической митральной недостаточности
У 10,9-19,0% пациентов с симптомами коронарной патологии и у 3,5-7,0% пациентов, при реваскуляризации миокарда выявляется сопутствующая митральная недостаточность. Большинство из них имеет I или II ст. митральной недостаточности.
У больных с хронической ишемическая митральной недостаточностью спектр клинических проявлений определяют три фактора:
2) степень митральной регургитации и
3) выраженность дисфункции левого желудочка.
У пациентов с окклюзией коронарных артерий может не наблюдаться никаких признаков ишемии или она носит стабильный или прогрессирующий характер. В этой связи, подход и методы лечения существенно не отличаются от пациентов без митральной недостаточности. Митральная недостаточность – второй существенный момент. В настоящее время I или II ст. митральной регургитации у больных без признаков сердечной недостаточности (ФВ > 40%) не требует коррекции последней. Более серьезная степень митральной недостаточности и/или наличие сердечной недостаточности (ФВ < 40%) требуют хирургической коррекции.
Патофизиология
У пациентов с хронической ишемической митральной недостаточностью увеличение объема левого желудочка и напряжение его стенки возрастает без увеличения толщины последней, несмотря на гипертрофию кардиомиоцитов в неповрежденных инфарктом миокарда регионах. У больных с митральной недостаточностью и с близкой к нормальной фракции выброса поддержание сердечного выброса обеспечивается увеличением преднагрузки левого желудочка, в то время как пиковое систолическое напряжение стенки левого желудочка увеличивается, а скорость укорочения миокардиальных волокон снижается. В то же время у больных со сниженной ФВ конечно-систолический и диастолический объемы, а также напряжение стенки увеличиваются, при одновременном снижении ударного объема. При этом увеличение постнагрузки левого желудочка не может быть преодолено увеличением контрактильности и преднагрузки. Давление в левом предсердии, конечно-диастолическое давление левого желудочка и давление заклинивания в легочной артерии возрастает в 2-3 раза. Левое предсердие увеличивается в объеме. С течением времени степень регургитации на митральном клапане и потеря сократительной функции миокарда, обусловленной ремоделированием левого желудочка, увеличивается.
Первичная цель диагностических исследований состоит в том, чтобы определить анатомию и степень коронарной патологии, механизма митральной недостаточности и выраженность дисфункции левого желудочка. При хронической ишемической митральной недостаточност геометрия левого желудочка и его функция отражают ремоделирование левого желудочка вследствие митральной недостаточности.
На ЭКГ характерны признаки предшествующего инфаркта миокарда. Часто наблюдается мерцательная аритмия. У больных без сердечной недостаточности и умеренной митральной регургитацией размеры сердца при рентгенографии не увеличены, а у пациентов с выраженной сердечной недостаточностью выявляется увеличение левого предсердия.
Двумерная эхокардиография позволяет обнаружить разрыв хорд, определить состояние кольца и створок митрального клапана и способна дифференцировать ишемическую митральную недостаточность от другой патологии. ЭхоКГ также эффективно оценивает региональную сократимость и глобальную функцию левого желудочка. Степень митральной недостаточности хорошо определяется цветной допплерографией. Зондирование сердца дает возможность выявить степень коронарной патологии. Оценка результатов тонометрии в левых и правых отделах сердца дает дополнительную информацию о функциональном состоянии левого желудочка.
Пациентам с поражением коронарных артерий, которым невозможно выполнить ЧТКА, показано хирургическое лечение, однако наличие ишемической митральной недостаточности и дисфункции левого желудочка увеличивает риск операции. Решение о коррекции митральной недостаточности I-II ст. принимается до операции по результатам нагрузочной ЭхоКГ. Восстановление компетентности клапана при III-IV ст. митральной регургитации не подлежит сомнению.
Операция
Дооперационная подготовка не отличаются от других операций на сердце, за исключением необходимости транспищеводной ЭхоКГ для оценки функции митрального клапана. После индукции в наркоз вследствие того, что анестезия уменьшает системное сосудистое сопротивление и постнагрузку, провокация увеличением (в 1,5-2,0 раза) преднагрузки левого желудочка дополнительным объемом дает возможность демаскировать скрытую степень митральной недостаточности для принятия правильного решения на операционном столе.
Операция выполняется по стандартной схеме. Доступ к митральному клапану, как правило, осуществляется через левое предсердие. Тщательная ревизия клапана позволяет выявить разорванные, удлиненные, или склерозированные хорды, фиброз и дистрофию папиллярных мышц. Чаще всего клапан оказывается интактным, за исключением дилатации фиброзного кольца.
Решение восстанавливать или заменять клапан часто затруднено. Протезирование рекомендуется у пожилых пациентов с выраженной дисфункцией левого желудочка, которым недопустимо длительное ИК с продленной остановкой сердца. Короткая операция, заканчивающаяся восстановлением компетентности клапана, дает наибольший шанс на успех. У большинства других пациентов предпочтительна реконструкция клапана, если она возможна. Вместе с тем, клапансохраняющая операция всегда имеет риск неудачи, потребующей немедленного или отсроченного протезирования клапана.
Последние сообщения показывают, что пластические процедуры на митральном клапане эффективны у 97% больных, даже при его недостаточности III-IV ст. Кольца для пластики были имплантированы в 98% случаев и у 80% пациентов были единственным хирургическим маневром. Как правило, используется гиперкоррекция с применением колец диаметром менее 30 мм (79%). Ятрогенный митральный стеноз не выявлен ни в одном случае, даже при имплантации 26-мм колец. В последнее время наметилась тенденция использовать полные жесткие кольца с изменой пространственной геометрией, обеспечивающие лучшие результаты в отдаленном послеоперационном периоде.

Стандартное жесткое кольцо Carpentier (1) и кольцо для пластики митрального клапана (2,3)
Сохранение хордального аппарата при протезировании позволяет обеспечить хорошую функцию левого желудочка в раннем послеоперационном периоде, особенно у пациентов с низкой (< 35%) ФВ. Биопротезы позволяют выполнить эту процедуру технически проще, так как их имплантация исключает дисфункцию протеза, связанную с заклиниванием створок, присущую механическим искусственным клапанам сердца. Кроме того, использование биопротезов целесообразно у больных с мерцательной аритмией, пожилых пациентов, больных с ожидаемой продолжительностью жизни меньше 5-6 лет или с прогнозируемым риском постоянной антикоагулянтной терапии.
После окончания ИК при признаках недостаточности левого желудочка решение о применении механической поддержки кровообращения должно приниматься немедленно, так как многократные попытки повторного или продленного экстракорпорального кровообращения бессмысленны.
Результаты
Одна реваскуляризация миокарда без коррекции недостаточности клапана, у пациентов с хронической ишемической митральной недостаточностью дает более высокую госпитальную летальность, чем у больных без недостаточности митрального клапана. Наличие не корригированной ишемической митральной недостаточности I ст. увеличивает летальность до 3,4-4,5 %, недостаточность II ст. – до 6-11%. 2-х летняя выживаемость для этих же пациентов составляет 88% и 78% соответственно, а 5- летняя выживаемость - 60-70%.
Госпитальная летальность при одновременной коррекции хронической митральной недостаточности и реваскуляризации миокарда колеблется от 3% до 33%, составляя в среднем 20%. Выбор протеза клапана не влияет на непосредственные результаты. Факторы риска госпитальной летальности включают возраст, застойную сердечную недостаточность, низкую ФВ, дооперационное использование контрпульсации, тяжелые сопутствующие заболевания. В последнее время с учетом применения улучшенной кардиопротекции и средств вспомогательного кровообращения, наметилась тенденция к значительному снижению летальности в этой группе пациентов.
Несмотря на все усилия 5-летняя выживаемость больных с вызванной инфарктом миокарда сердечной недостаточностью, несмотря на коррекцию митральной регургитации, составляла приблизительно 50% (хуже чем для большинства типов рака). Это означало, что недостаточное понимание основной патофизиологии постинфарктного ремоделирования левого желудочка не позволяло улучшить результаты хирургического лечения указанной когорты больных. Недавние клинические, теоретические, и экспериментальные исследования пролили новый свет на эту проблему.
Оказалось, что региональное увеличение напряжения стенки левого желудочка нормально перфузируемого миокарда, смежного с зоной инфаркта, индуцирует производство свободных радикалов кислорода, апоптоз кардиомиоцитов и изменения в метаболизме коллагена. Несмотря на необходимость дальнейших исследований для доказательства этой гипотезы, стало понятна необходимость ранних хирургических вмешательств, прежде чем наступит патологическое ремоделирование левого желудочка. Реперфузия в зоне состоявшегося инфаркта миокарда слишком запаздывает для спасения миоцитов, но способна предотвратить дилатацию левого желудочка, положительно изменяет метаболизм коллагена и стабилизирует геометрию желудочка.
Таким образом, методы хирургического ремоделирования левого желудочка совместно с реваскуляризацией миокарда и восстановлением компетентности митрального клапана должны занять совершенно определенное место для улучшения результатов лечения осложнений инфаркта миокарда.
Лечение ишемической митральной недостаточности в Беларуси - европейское качество за разумную цену
Профессор, доктор медицинских наук Ю.П. Островский
См. также:
митральная недостаточность в приобретенных пороках сердца
митральная недостаточность в осложнениях инфаркта миокарда
митральная недостаточность в рекомендациях для пациентов
митральная недостаточность во врожденных пороках сердца


