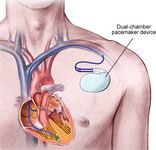
 Электрокардиостимуляция (ЭКС) и лечение желудочковых аритмий посредством имплантации кардиовертеров-дефибрилляторов (ИКД) постоянно усовершенствуются. В настоящее время больные старше 75 лет, которым проведена имплантация стимуляторов, составляют 2,6% от всей популяции, 23% пациентов после имплантации ЭКС и 5% с ИКД находятся в восьмидесятилетнем возрасте.
Электрокардиостимуляция (ЭКС) и лечение желудочковых аритмий посредством имплантации кардиовертеров-дефибрилляторов (ИКД) постоянно усовершенствуются. В настоящее время больные старше 75 лет, которым проведена имплантация стимуляторов, составляют 2,6% от всей популяции, 23% пациентов после имплантации ЭКС и 5% с ИКД находятся в восьмидесятилетнем возрасте.
В США на 1 миллион населения выполняется 600-700 имплантаций электрокардиостимуляторов, в Европе - 300-400, в Беларуси - 100 первичных кардиостимуляций на 1 млн. населения. Несмотря на то, что область лечения аритмий становится прерогативой электрофизиологов, кардиохирурги продолжат играть важную роль и как непосредственные исполнители операций, и как суд последней инстанции для сложных случаев.
Впервые в мире эндокардиальную стимуляцию сердца в клинике в 1958 г. выполнил S.Furman (США), в бывшем СССР в 1962 г. Ю.Бредикис и В.С.Савельев имплантировали электрокардиостимулятор (ЭКС) миокардиальным доступом.
Анатомия проводящей системы сердца
Показания к имплантации электрокардиостимулятора
Осложнения после имплантации кардиостимулятора
Анатомия проводящей системы сердца
Проводящая система сердца состоит из синоатриального узла, межузловых путей, атриовентрикулярного узла или соединения, пучка Гиса, его ножек и волокон Пуркинье. 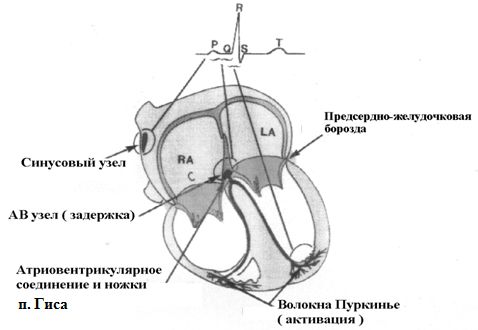
Анатомия проводящей системы сердца
Синоатриальный узел (СА-узел) или узел Кис-Флака представляет собой группу высокоспециализированных клеток, располагающихся субэпикардиально с переднемедиальной стороны в области контакта верхней полой вены и основания ушка правого предсердия. Размеры узла – 16х5х2 мм, его питает одноименная артерия, отходящая от правой (чаще) или левой коронарной артерии.
Межузловые пути (передний, средний, задний) и межпредсердный пучок Бахмана не имеют специализированных клеток, а являются путями предпочтительного проведения импульсов, то есть существуют функционально.
Атриовентрикулярный узел (АВ-узел) или узел Ашоффа-Товара является сложной анатомо-функциональной структурой, где происходит атриовентрикулярная задержка импульса. Он состоит из «переходной зоны» и «компактного» отдела, представленных специализированными клетками, его размеры – 6х3х1,5 мм. Кровоснабжение АВ-узла, в основном, осуществляется ветвью правой коронарной артерии, а в 7-20% случаев – из огибающей ветви левой коронарной артерии. Атриовентрикулярный узел находится в треугольнике Коха, границами которого являются - сухожилие Тодаро, коронарный синус и фиброзное основание перегородочной створки трехстворчатого клапана.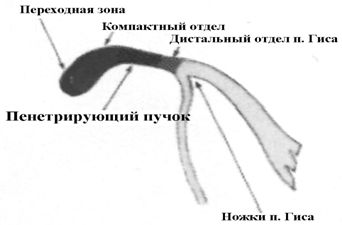
Строение атриовентрикулярного узла
АВ-узел пенетрирует центральное фиброзное тело, в месте контакта фиброзных колец митрального, трехстворчатого и аортального клапанов, и переходит в пучок Гиса, который разветвляется на правую ножку и переднюю и заднюю ветви левой ножки пучка Гиса. Длина пучка варьирует от 5 до 25 мм, а диаметр – от 1 до 3 мм. Пучок Гиса проходит субэндокардиально параллельно задненижнему краю перепончатой части межжелудочковой перегородки. Дистальные части ножек пучка Гиса заканчиваются волокнами Пуркинье с переходом в миофибриллы сократительного миокарда.
Система проводимости уязвима к повреждению во время манипуляций при сердечной хирургии. Полная блокада может развиться в результате наложения швов при операциях на аортальном, митральном, или трехстворчатом клапане, а также во время закрытия дефектов перегородок сердца и резекции миокарда у больных с идиопатическим гипертрофическим субаортальным стенозом. Места этих повреждений схематично обозначены на рисунке:
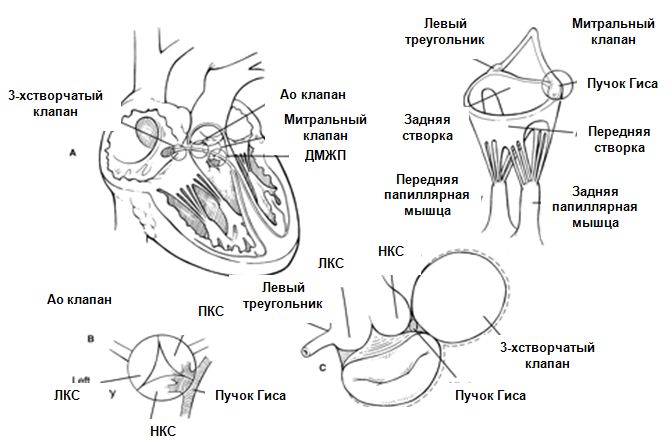
Локализация возможных повреждений проводящей системы сердца во время операций
Брадикардия
К брадикардиям, требующим хирургического лечения, относятся атриовентрикулярные блокады сердца вследствие инфаркта миокарда, хронические би- и трифасцикулярные блокады ножек пучка Гиса, синдром слабости синусового узла, врожденные и ятрогенные (хирургические) АВ блокады.
Атриовентрикулярная блокада сердца встречается в 0,2–0,3% популяции. Инфаркт миокарда, осложненный АВ блокадой сердца III степени, без использования кардиостимуляции в 60–70% случаев заканчивается летальным исходом. Другая разновидность брадикардии – синдром слабости синусового узла (СССУ) наблюдается в 0,024 – 0,034% случаев среди населения.
Методы исследования брадикардий
Диагностика брадиаритмий в настоящее время не представляет сложности. Для этого используются:
- Стандартная ЭКГ (12 отведений).
- Холтеровский мониторинг, на основании которого можно анализировать деятельность сердца по ритму (ЧСС) в течение длительного отрезка времени, выявить и документировать характерные нарушения ритма и проводимости при СССУ и АВ блокаде сердца.
- Чреспищеводное электрофизиологическое исследование сердца позволяет с помощью диагностической стимуляции левого предсердия со стороны пищевода определить электрофизиологические параметры проводящей системы сердца:
• корригированное время восстановления функции синусового узла (в норме < 600- 800 мс);
• атриовентрикулярное проведение (в норме > 130 импульсов в минуту)
Показания к имплантации электрокардиостимулятора
Абсолютные показания
- Приобретенная АВ блокада сердца IIБ-III степени с приступами Морганьи-Адамса-Стокса или без потери сознания. На ЭКГ приступ Морганьи-Адамса-Стокса представлен асистолией или, реже, фибрилляцией желудочков. Для имплантации электрокардиостимулятора достаточно одного эпизода потери сознания, обусловленного нарушениями ритма и документированного по ЭКГ, так как такие больные, как правило, умирают внезапно.
- Приобретенная АВ блокада сердца IIБ-III степени с недостаточностью кровообращения III-IV ф.кл. NYHA. Сердечная недостаточность развивается при снижении ЧСС менее 40 ударов в минуту.
- АВ блокада сердца IIБ-III степени, возникшая и не отстраивающаяся в течение 3-4 недель после инфаркта миокарда. Более плохой прогноз в плане восстановления ритма – при заднем инфаркте миокарда. В остром периоде инфаркта миокарда, как правило, навязывается учащающая временная электрокардиостимуляция сердца.
- Синдром слабости синусового узла с приступами Морганьи-Адамса-Стокса или с недостаточностью кровообращения III-IV ф.кл. NYHA. На ЭКГ синдром слабости синусового узла проявляется чаще всего в виде синусовой брадикардии с желудочковой экстрасистолией, остановкой синусового узла (паузы ≥ 3 сек.), и реже – в виде сино-аурикулярной блокады III ст. Наиболее сложно медикаментозно лечить тахи-брадиформу СССУ. В данной ситуации методом выбора на первом этапе лечения является учащающая постоянная кардиостимуляция.
- Брадиаритмическая форма мерцания и трепетания предсердий, со снижением ЧСС менее 50 уд. в мин., или при паузах между комплексами QRS > 3 с, а также недостаточность кровообращения III-IV ф.кл. NYHA.
Относительные показания
- Врожденная полная АВ-блокада сердца у взрослых пациентов с недостаточностью кровообращения III ф.кл. NYHA. При врожденной АВ-блокаде сердца не наблюдается приступов МАС, однако при снижении ЧСС 50 и менее уд. в мин. с течением времени постепенно развивается сердечная недостаточность. Поэтому, при ухудшении состояния больного с соответствующими клиническими данными (ЭКГ, ЭхоКГ, рентгенография сердца) в плановом порядке показана имплантация ЭКС.
- Хроническая би- и трифасцикулярная блокада сердца. Альтернирующая блокада ножек пучка Гиса указывает на нарушения проведения в обеих ножках, что проявляется, как правило, клинической симптоматикой, включая синкопе.
- Увеличение интервала НV более 100 мсек., расширение комплекса QRS > 0,8 с.
- Врожденная АВ блокада сердца с клинической картиной недостаточности кровообращения III-IV ф.кл. NYHA или СССУ с приступами Морганьи-Адамса-Стокса.
Блокада I степени характеризуется увеличением PQ интервала > 200 мс. Блокада I ст. при низкой частоте предсердий может прогрессировать с развитием периодов Wenckebach. Блокада II степени приводит к неполной диссоциации предсердий и желудочков и замедлению ритма. Блокада III степени - полная атриовентрикулярная диссоциация с частотой предсердий, превышающей частоту желудочков. Развитие АВ блокады IV степени характерно для кардиомиопатии, идиопатического фиброза, ятрогенного повреждения, бактериального эндокардита и врожденной патологии сердца.
Слабость (дисфункция) синусового узла может привести к симптоматической брадикардии при коронарной патологии, кардиомиопатии и назначении наркотиков. Кроме того, СССУ может быть следствием гиперчувствительности каротидной пазухи, вазовагальных обмороков. Имплантация двухкамерного ЭКС (DDD или VDD) показана при асистолических интервалах > 3 с.
Электрокардиостимуляторы
Клеточная мембранная деполяризация и реполяризация обеспечивают механизм автоматизма камер сердца и системы проводимости. В покое внешняя поверхность клетки имеет положительный, а внутренняя - отрицательный заряд. Воздействие отрицательного заряда на внешнюю поверхность клетки приводит к ее деполяризации. Этот механизм лежит в основе электрокардиостимуляции.
Электрокардиостимулятор (permanent pacemaker) представляет собой систему, состоящую из генератора и передающих электродов. Генератор содержит батарею, антенну телеметрии, и интегральные схемы. Источником энергии является литиево-иодный аккумулятор. Интегральные схемы включают программируемые микропроцессоры, осцилляторы, усилители и сенсоры. Современные электрокардиостимуляторы посредством телеметрических датчиков могут сохранять внутренний статус, состояние внешних связей и запрограммированных параметров настройки. К сожалению, каждый стимулятор синхронизируется только с программатором собственного изготовителя.
Номенклатура и режимы электрической стимуляции сердца
В международной практике применяется 5-буквенный номенклатурный код типов электрической стимуляции сердца NBG-NASPE-BPEG (см. табл.), где первая буква обозначает стимулируемую камеру сердца; вторая – камеру, воспринимающую стимул; третья – ответ на восприятие; четвертая – программирование ритмовождения; пятая – антитахикардитические функции.
| Позиция буквы в номенклатуре кода | ||||
| 1 | 2 | 3 | 4 | 5 |
| Функциональное значение буквы в номенклатуре кода | ||||
| Стимулируемая камера | Воспринимающая камера | Ответ на восприятие | Программируемость | Купирование тахиаритмий |
| 0 – нет | 0 – нет | 0 – нет | 0 – нет | 0 – нет |
| А - предсердие | А - предсердие | Т - возбуждение | Р - простое программирование | Р – учащающая или сверхчастая стимуляция |
| V - желудочек | V - желудочек | I - подавление | М - мультипрограммирование | S – дефибрилляция |
| D - обе камеры (A+V) | D - обе камеры (A+V) | D - обе функции (Т+I) | С – коммуникативность R-модуляция частоты |
D - двойная функция (Р+S) |
Примечание. Позиция 1-3 используется для обозначения антибрадиаритмических функций.
Основные характеристики различных режимов стимуляции сердца показаны в следующей таблице.
Основные характеристики режимов стимуляции сердца
| Характеристика различных режимов электрокардиостимуляции | ||||
| Режим ЭКС | АВ-синхронизация | Активация желудочков через нормальную проводящую систему | Зависимая от активности предсердий частотная адаптация | Независимая от активности предсердий частотная адаптация |
| AAI | + | + | - | - |
| VVI | - | - | - | - |
| AAIR | + | + | - | + |
| VVIR | - | - | - | + |
| VAT/VDD | + | +/ | + | + |
| DVI/DDI | +/ | +/ | - | - |
| DDIR | +/ | +/ | - | + |
| DDD | + | +/ | + | - |
| DDDR | + | +/ | + | + |
Однокамерная стимуляция
Вначале были разработаны электрокардиостмуляторы с фиксированной частотой в асинхронном режиме (VOO, АОО). Затем в 1965 г. появились программируемые ЭКС, определяющие собственную активность сердца и работающие в режиме "demand" (VVI) т.е. - по требованию.
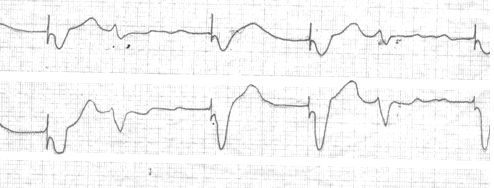
ЭКГ при работе электрокардиостмулятора в режиме “по потребности”.
АВ-синхронзация важна для обеспечения заполнения желудочков. Нормальное сердце производит ударный объем на 5-15% больше, чем при АВ-асинхронии. Сердечная недостаточность, гипертрофия и сниженный диастолический комплайнс левого желудочка увеличивают количественную важность АВ-синхронизации. Апикальная стимуляция правого желудочка нарушает нормальную последовательность активации, так как деполяризация медленно распространяется по стенкам желудочка вместо того, чтобы распространиться быстро и симметрично через проводящую систему.
Гипотеза о том, что нарушение последовательности активации может уменьшить механическую работу левого желудочка, была установлена экспериментально и подтверждена клинически. Это объясняет, почему желудочковый аортальный градиент при идиопатическом гипертрофическом субаортальном стенозе уменьшается при последовательной двухкамерной стимуляции (DDD). Электрокардиостимуляция выходного тракта правого желудочка также может увеличить ударный объем по сравнению с апикальной стимуляцией из-за ее благоприятного эффекта последовательной активации.
Двухкамерная стимуляция
Следующее поколение электрокардиостимуляторов (VDD, AAI, DDD) благодаря автоматическому контролю частоты и увеличению степени наполнения желудочков сердца за счет синхронного сокращения предсердий (вклад предсердий) позволило обеспечить работу сердца в физиологическом режиме. Физиологическая электрокардиостимуляция, особенно в режиме DDD, при которой сохраняется АВ-синхронзация, дает возможность нормализовать сердечный выброс и значительно увеличить функциональные резервы пациента. Однако при синдроме слабости синусового узла, когда в ответ на нагрузку нет спонтанного учащения ритма сердца, этот режим недостаточен. Бивентрикулярная стимуляция у пациентов с кардиомиопатией с нарушением внутри- межжелудочковой проводимости улучшает функцию левого желудочка, восстанавливая одновременное сокращение перегородки и его свободной стенки (желудочковая ресинхронизация).
Программирование двухкамерных ЭКС (DDD) включает установку нижнего и верхнего порогов частоты ритма и задержку АВ-проведения. Если ритм предсердия находится в пределах заданного лимита, электрокардиостимулятор поддержит желудочковую стимуляцию в режиме 1:1. При замедлении ритма предсердий ниже установленного лимита ЭКС добавляет частоту предсердной стимуляции до нижнего порога. Если предсердный ритм быстрее, чем верхний предел, пейсмекер поддерживает частоту сокращений желудочков на верхнем пределе лимита с потерей АВ-синхронизации, напоминая эффект Wenckebach.
Программирование задержки АВ-проведения - создание допустимого интервала между предсердным и желудочковым сокращением. Отсчет времени запуска задержки начинается с зубца Р или предсердного стимула электрокардиостимулятора. Если во время разрешенного интервала задержки отсутствует деполяризация желудочков, пейсмекер подает стимул к желудочкам. При предсердной стимуляции физиологическая P волна может появиться через 100 мс, поэтому необходима более длительная АВ-задержка. 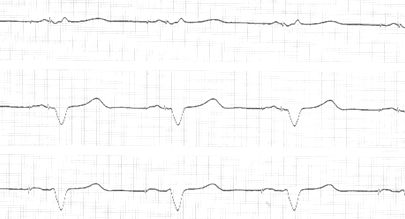
ЭКГ при бифокальной (двухкамерной) кардиостимуляции в режиме DDD
Частотно-адаптивная стимуляция
При повышении метаболических потребностей сердечный выброс увеличивается за счет повышения контрактильности миокарда, увеличения венозного возврата и ЧСС. У пациентов с нормальным ритмом синусового узла при физической нагрузке DDD стимуляторы восстанавливают АВ-синхронизацию, считывая предсердный импульс и передавая его желудочкам. При нарушении функции СА узла или однокамерной стимуляции для поддержания физиологического ответа сердца на нагрузку необходимо изменение частоты стимуляции желудочков для компенсации метаболических потребностей.
Поэтому были разработаны электрокардиостимуляторы с детекторами, реагирующими на механические движения (акселерометр), частоту дыхания и минутную вентиляцию легких, давление в правом желудочке, изменение температуры центральной венозной крови, вызванный интервал QT, которые увеличивают соответственно этому частоту электростимуляции. ЭКС с этой способностью идентифицированы буквой "R" (rate responsive), добавляемую к трехбуквенному коду пейсмекера (DDDR). Все предложенные детекторы приводят к учащению ритма. Вместе с тем, вибрационный сенсор может вызвать тахикардию во время автомобильной поездки по неровной дороге. Пожилые пациенты с сидячим образом жизни вряд ли извлекут от этого пользу, так как за этим могут последовать неблагоприятные эффекты в виде коронарной недостаточности.
В последнее время разработаны ЭКС с несколькими детекторами и двухкамерным режимом электрокардиостимуляции, что позволяет достичь оптимальной частоты ритма сердца в любую фазу нагрузки.
Энтузиазм к двухкамерной стимуляции увеличивается. Пароксизмальная мерцательная аритмия больше не является противопоказанием. Последние модели ЭКС (VVIR) могут распознавать у пациента мерцание и трепетание предсердий и автоматически переключаться на желудочковый частотно-адаптивный режим электростимуляции, так называемая, switch function. Это позволяет избежать «тахикардии кардиостимулятора» так как синусовый ритм, поддержанный стимуляцией желудочков, лучше, чем только желудочковая стимуляция. Точно так же двухкамерная стимуляция рекомендуется при рефлекторных синкопе. VVI или VVIR стимуляция наиболее предпочтительна для пациентов с брадикардией и хронической мерцательной аритмией. AAIR стимуляция хорошо проявила себя после трансплантации сердца с остановкой или брадикардией синусового узла аллотрансплантата.
Однополярные и биполярные электроды
Однополярная система состоит из единственного электрода, несущего отрицательный заряд, при этом тело пациента является анодом. Конструкция биполярных систем включает два электрода, отделенных изоляцией. Биполярные системы более устойчивы к электрическим шумовыми воздействиям и реже вызывают стимуляцию диафрагмы или стенки грудной клетки. Вместе с тем имплантация их по сравнению с однополярными системами более трудна из-за их жесткости. Активная фиксация наконечника электрода обеспечивается выдвижной винтовой спиралью или якорной системой, которая проводится между трабекулами.
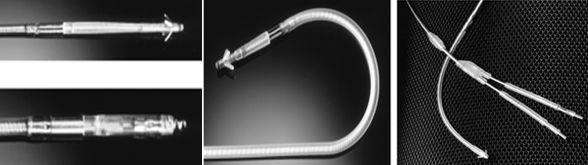
1 2 3
Биполярные желудочковые электроды с якорным и винтовым наконечниками (1); биполярный предсердный J- электрод со стероидным покрытием наконечника (2); биполярное контактное соединение с ЭКС (3)
Выбор способа стимуляции
Использование эндокардиальной стимуляции более предпочтительно. Небольшая поверхность контакта эндокардиальных электродов обеспечивает меньший порог стимуляции, чем у использующихся в настоящее время покрытых стероидами эпикардиальных электродов. При эпикардиальной стимуляции чаще наблюдается перелом электродов, а удаление инфицированных систем требует торакотомии. Фиброз и травма при реоперациях делают эпикардиальную стимуляцию более трудной. В этой связи она показана при врожденной патологии сердца, у пациентов с механическими клапанами в трехстворчатой позиции или проблемами, связанными с венозным доступом. Стимуляция левого желудочка проще достигается при эпикардильной имплантации электродов через миниторакотомию. Стимуляция правого предсердия и желудочка при торакотомии может быть осуществлена введением электродов через стенку предсердия.
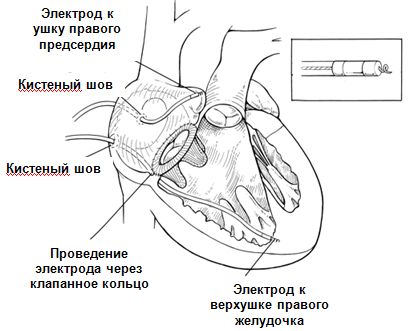
Двухкамерная стимуляция правых отделов сердца
При АВ-блокаде сердца или брадиаритмической форме мерцания и трепетания предсердий основным режимом электрокардиостимуляции остается желудочковая электростимуляция «по потребности» - VVI. Такой режим обеспечивают кардиостимуляторы - ЭКС-501 (Россия), “Premier” - Medtronic Inc. и др. Больным трудоспособного и молодого возраста предпочтительнее имплантировать частотно-адаптивные ЭКС - VVIR, такие как “Microny”, ”Regensy”, ”Dash” - Peisetter Intermedics Inc. При хорошем предсердном ритме с адекватной хронотропной реакцией для АВ-синхронизации используется режим предсердно-управляемой электрокардиостимуляции – VDD: ЭКС «Unity» - Peisetter Intermedics Inc.
При СССУ с сохраненным АВ проведением (более 130 импульсов в мин.) вероятность развития АВ блокады не превышает 5-8%, поэтому показана предсердная электрокардиостимуляция - ААI. При снижении скорости АВ проведения более целесообразна физиологическая (двухкамерная) кардиостимуляция - DDD, DDDR, кардиостимуляторы – “Trilogy” ,” Relay”, ” Thera” - Peisetter Intermedics Inc., Metdtronic Inc.
При хронотропной сердечной недостаточности, обусловленной неадекватным ответом СА-узла или водителей ритма из нижележащих отделов проводящей системы сердца на физическую нагрузку или другие метаболические потребности организма, возможно использование физиологической частотно-адаптивной электрокардиостимуляции – DDDR.
Идиопатический гипертрофический субаортальный стеноз вызывает преграду оттока из левого желудочка со стенокардией и/или обморочными состояниями. Постоянная ЭКС правого желудочка с короткими интервалами АВ-задержки предвозбуждает правый желудочек и уменьшает градиент оттока у некоторых пациентов с идиопатическим гипертрофический субаортальным стенозом.
Брадикардия после кардиохирургических вмешательств корригируется временной предсердно-желудочковой эпикардиальной ЭКС. Проблемы стимуляции в послеоперационном периоде включают потерю сенсорной или стимулирующей функции электрокардиостимулятора вследствие возрастающего порога приема или передачи импульса генератора. Изменение полярности или повышение мощности стимула позволяют устранить эти осложнения. Параметры настройки временного электрокардиостимулятора устанавливаются таким образом, чтобы достичь максимального сердечного выброса и артериального давления.
Учитывая изложенное, в настоящее время режим выбора стимуляции и типа электрокардиостимулятора определяют: возраст больного, желание и возможность пациента к сохранению физической активности или малоподвижного образа жизни, а также стоимость кардиостимулятора.
Техника операции
Постоянная эндокардиальная стимуляция сердца
Под местной анестезией горизонтальным разрезом длиной 6 см на 4 см ниже ключицы с распространением боковой части разреза на s.deltoideopectoralis формируется ложе ЭКС. Это позволяет поместить стимулятор далеко от подмышечной впадины, избегая его смещения при движении руки в плече. Под контролем флюороскопической системы через просвет вены (v. cephalica, v. subclavia, v. jugularis externa или interna) в верхушку правого желудочка или в правое предсердие по методике Seldinger вводится эндокардиальный электрод. Если планируется имплантация двухкамерного стимулятора, проводник второго электрода должен быть повторно вставлен через интродьюсер прежде, чем последний будет удален. 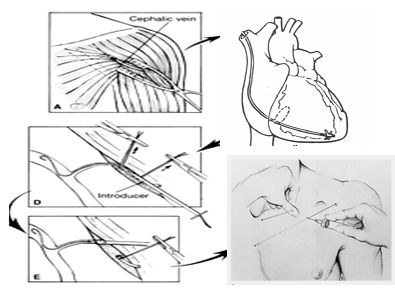
Имплантация эндокардиального электрода
Для предотвращения перфорации правого желудочка при использовании винтового электрода его наконечник должен визуализироваться во время всего процесса фиксации. Активная фиксация позволяет выбрать место расположения как предсердного, так и желудочкового электрода в правых отделах с наименьшим порогом стимуляции. На рисунке представлены наиболее предпочтительные места фиксации электродов.
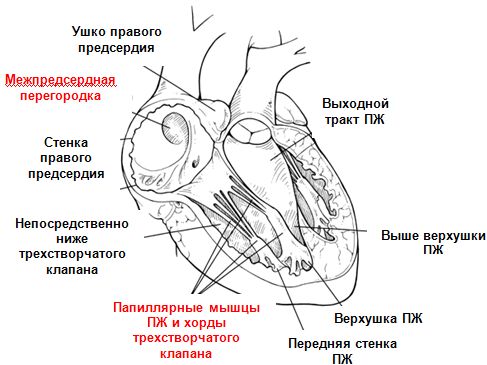
Места фиксации электродов (обозначены черным цветом)
После введения электродов определяется порог электрокардиостимуляции и величина внутрисердечного потенциала (порог < 0,7 В, амплитуда R-волны > 5 мВ, для монополярного электрода импеданс должен быть 400-1 000 Ом). Проводятся провокационные пробы на дислокацию электрода (гипервентиляция и кашель) и стимуляцию диафрагмы. Длина электрода должна быть адекватной, чтобы при глубоком дыхании в вертикальном положении и кашле (при положении на спине) это не приводило к дислокации электрода за счет продольной тракции или образованию петли. К дистальному коннектору электрода присоединяется кардиостимулятор и помещается в сформированное ложе (подкожно или под большую грудную мышцу).
Для двухкамерной стимуляции требуется предсердный электрод "J" формы (для фиксации в области ушка) и "S" формы (при активной фиксации к правой стенке предсердия в области vena cava). Амплитуда P-волны в этих местах лучше, чем в других участках предсердия. Электрограмма P-волны - ахиллесова пята двухкамерной стимуляции. Амплитуда P-волны идеально должна быть больше 1,5 мВ. Измерение амплитуды P-волны с монополярным электродом генератора иногда приводит к ошибке, так как пик 2 мВ, может оказаться не волной P, а комплексом QRS. Одновременное измерение предсердных и желудочковых электрограмм поможет избежать этого. Альтернативным решением является программирование генератора как детектора P-волны. В ЭКС устанавливается чувствительность 2 мВ, более низкая, чем у пациента частота генерации предсердного стимула, а АВ задержка – короче, чем PR-интервал. Когда генератор соединен с предсердным и желудочковым электродом, то каждая волна P, если ее амплитуда > 2 мВ, будет немедленно сопровождаться желудочковым комплексом. ЭКС после этого повторно программируется для достижения адекватных параметров стимуляции с телеметрическим подтверждением ЭКГ.
Стимуляция левого желудочка через коронарный синус становится все более популярной. Так как у больных с сердечной недостаточностью размеры правых отделов сердца значительно увеличены, для имплантации электрода необходимы специальные управляемые катетеры и определенные навыки
Кисетный шов вокруг вены и в мышце обычно обеспечивает адекватный контроль гемостаза и позволяет стабилизировать электрод. ЭКС помещается в карман впереди или сзади большой грудной мышцы. Использование биполярных систем облегчает размещение генератора позади m.pectoralis. Другие места для имплантации генераторов включают подмышечное, ретромаммарное, внутригрудное или предбрюшинное расположение.
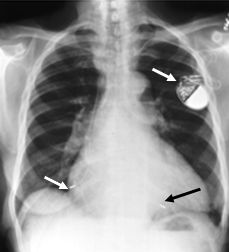
Расположение двухкамерного стимулятора и биполярных электродов
Миокардиальная стимуляция сердца
Миокардиальная стимуляция сердца используется значительно реже (в 2-5%). В основном она применяется в случаях, когда ранее были использованы чрезвенозные доступы или при наличии фиброза эндокарда. Под общим обезболиванием в IV межреберье выполняется левосторонняя (реже - правосторонняя) торакотомия или производится нижнесрединная медиастинотомия. Непосредственно к миокарду желудочка или предсердия фиксируются электроды с интраоперационным определением параметров электрокардиостимуляции. Электрокардиостимулятор помещают под большую грудную или прямую мышцу живота, у женщин – ретромаммарно.
Программирование электрокардиостимулятора осуществляется непосредственно после операции. Программирование двухкамерного стимулятора позволяет регулировать чувствительность, ширину и амплитуду импульса как для предсердия, так и желудочка, пороги верхней и нижней частоты, АВ задержку и невосприимчивые периоды сенсорного восприятия. Эти же параметры контролируются и при необходимости корригируются при каждом посещении клиники.
Замена электрокардиостимулятора
15% функционирующих генераторов нуждаются в замене по различным причинам. Осложнения замены ЭКС включают инфекцию, повреждение электрода и асистолию во время переключения со старого на новый генератор.
Осложнения после имплантации кардиостимулятора
Частота ранних осложнений в среднем составляет 6,7 %. Реоперация требуется у 4%. Для пациентов старше 65 лет частота осложнений и реопераций сопоставима с более молодыми больными - 6,1% и 4,4%, соответственно.
Инфекционные осложнения после имплантации ЭКС проявляются как сепсис, неустойчивая лихорадка с нагноением, или свищом ложа ЭКС. Инфекция может быть подавлена, но редко устраняется антибиотиками и проблема обычно возвращается несколько месяцев спустя. При возникновении гнойных осложнений кардиостимулятор выводится наружу, рана санируется, после чего имплантируется новая система с удалением старого электрода и ЭКС. Использование антибиотиков для профилактики при инвазивных вмешательствах не рекомендуется.
Специфические осложнения
- Дислокация электрода. Частота осложнения при использовании электродов с первичной фиксацией не превышает 1,5-2%. Как правило, она развивается в первый месяц после операции. На ЭКГ отсутствует постоянное ритмовождение из-за плохого контакта электрода с эндокардом, что подтверждается рентгенологическим контролем. Производится репозиция электрода.
- Гемопневмоторакс и тампонада перикарда являются следствием нарушения техники имплантации электрода и требуют повторной операции. Частота осложнения не превышает 0,5-1%.
- Преждевременное истощение питания ЭКС наблюдается раньше окончания срока службы (8-10 лет) кардиостимулятора. Характерным признаком является замедление или учащение заданной частоты электростимуляции на 8-10 импульсов в минуту. Выполняется замена ЭКС.
- Блокада выхода импульса ЭКС (exit block) связана с избыточным формированием соединительной ткани в месте контакта головки электрода с эндокардом, вследствие чего мощности импульса ЭКС недостаточно для стимуляции сокращения сердца. Причинами могут быть воспалительно-дегенеративные изменения миокарда и фиброз эндокарда. На ЭКГ регистрируются низкие стимулы без ответов на фоне спонтанных сокращений сердца. Проводится имплантация нового электрода в другое место сердца.
- Потеря детекторной функции. ЭКС не способен воспринять спонтанное сокращение сердца, как сигнал к отмене выработки собственного стимула. На ЭКГ регистрируются собственные сокращения сердца с наслаивающимися на них стимулами генератора. Это осложнение устраняется перепрограммацией электрокардиостимулятора – повышением чувствительности к кардиосигналу.
- Стимуляция грудной мышцы и диафрагмы. Осложнение развивается при нарушении изоляции электрода, вследствие чего происходит шунтирование энергии на мышцу. В некоторых случаях при однополярной электрокардиостимуляции корпус электрокардиостимулятора замыкается на мышечный нерв и также стимулирует мышцу. При близком расположении кончика электрода в правом желудочке к проекции диафрагмального нерва происходит стимуляция диафрагмы. Во всех случаях производится повторная операция с устранением повреждения изоляции электрода или репозиция электрода в правом желудочке.
- Перелом электрода или нарушение изоляции приводит к нарушению функции электрокардиостимулятора. Импеданс < 300 Ом предполагает нарушение изоляции, а высокое сопротивление (> 1 000 Ом) – перелом электрода. Технические факторы, способствующие перелому электрода, включают избыточную его длину в сердце, давящие лигатуры и перегиб электрода в области ключицы. Диагностика осложнения возможна с помощью рентгенографии грудной клетки и ЭКГ. Требуется замена с удалением поврежденного электрода. Удаление электрода осуществляется с использованием техники Byrd. Для этого на электрод одеваются длинные пластмассовые ножны и проводятся по нему до упора в миокард в месте фиксации электрода. Подтягивание электрода с противоположной тягой ножен обеспечивает успешное удаление 90% электродов при 3% осложнений.
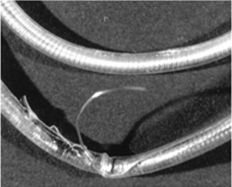
Перелом электрода
- ЭКС-индуцируемая тахикардия. Двухкамерные ЭКС могут вызвать аритмию вследствие ретроградной проводимости через АВ соединение, обусловленное преждевременной желудочковой деполяризацией. Предсердный сенсор ЭКС передает на желудочек стимул из предсердия. Если в ЭКС установлен высокий предел по частоте, волна re-entry через АВ узел способна индуцировать следующее сокращение. Эта проблема может быть минимизирована, снижая верхний порог по частоте таким образом, чтобы ЭКС «игнорировал» предсердный потенциал деполяризации, возникающий раньше 300-350 мсек. после комплекса QRS. Такой же прием правомочен и при мерцательной аритмии.
- Синдром электрокардиостимулятора (pacemaker-syndrome). Осложнение встречается у 30% больных с сохраненной ретроградной вентрикуло-атриальной проводимостью при стимуляции в режиме VVI. При этом нарушается АВ-синхронизация и сокращение предсердий происходит в тот момент, когда митральный и трехстворчатый клапаны закрыты. Вследствие этого развивается регургитация в системных и легочных венах и недостаточность наполнения желудочков, что клинически характеризуется гипотонией, обмороками, головокружением, утомляемостью, пульсацией вен шеи. Если во время операции при пробной желудочковой стимуляции АД снижается > 20 мм рт.ст. в сравнении с исходным при спонтанном ритме, можно прогнозировать развитие pacemaker-syndrome. В такой ситуации показана физиологическая двухкамерная (DVI, DDD) стимуляция c удлинением рефрактерного периода предсердий.
Если у больного с имплантированным однокамерным ЭКС возникли вышеперечисленные жалобы, то рекомендуется измерить АД в положении лежа, сидя и стоя и сравнить с АД, измеренным при спонтанном ритме. С помощью чрезпищеводной диагностической ЭКС можно выявить наличие ретроградной вентрикуло-атриальной проводимости. При подтверждении синдрома электрокардиостимулятора следует:
- уменьшить частоту электростимуляции;
- для снижения конкуренции собственного ритма больного и ЭКС удлинить гистерезис электрокардиостимулятора, т.е. удлинить интервал после воспринимаемого (спонтанного) комплекса QRS на интервал больший, чем следующий за стимулом;
- назначить нестероидные противовоспалительные и препараты калия;
- при отсутствии эффекта от указанных мероприятий показана операция: ликвидация ретроградного проведения или переход на физиологическую систему электрокардиостимуляции (DVI, DDD).
Послеоперационное наблюдение
Больным с ЭКС противопоказано находиться в зоне с сильными электрическими полями, а так же принимать электрофизиопроцедуры и проводить ЯМР-томографию. Интегральные схемы генератора могут быть повреждены радиотерапией. Если ЭКС не может быть защищен от лучевого воздействия, необходимо переместить его в отдаленный участок. Мобильные телефоны должны быть отдалены на 10-15 см от генератора, поэтому лучше ими пользоваться с контралатеральной стороны. Пациентам, работающим в электрически «шумных» окружающих средах, предпочтительно использование биполярных систем. Пациент должен быть обучен самостоятельно ежедневно контролировать частоту пульса и ежегодно консультироваться по месту проведения операции. При подозрении на нарушение работы ЭКС проводится холтеровское мониторирование, эхокардиография, чреспищеводное электрофизиологическое исследование сердца и программирование кардиостимулятора.
В случаях проведения других хирургических вмешательств, особенно с применением электрокоагуляции, необходимо перевести программу ЭКС в режим VOO, DOO, или VVT (асинхронный режим). Другим вариантом предотвращения нарушений работы ЭКС является "способ магнита". Постоянный магнит, помещенный над ЭКС, блокирует его магнитный выключатель и переводит работу генератора в режим VOO. Электрокоагуляция при этом должна использоваться в биполярном режиме. Кардиохирургические вмешательства с остановкой сердца требуют прекращения кардиостимуляции на время кардиоплегии. Это достигается проведением наружной ЭКС внешним генератором с частотой, превышающей установленные лимиты кардиостимулятора.
Современное развитие электрокардиостимуляции позволило снизить смертность и улучшить качество жизни больных с брадикардиями. Повторные инфаркты миокарда, пороки сердца, частые эпизоды желудочковой тахикардии, застойная сердечная и хроническая почечная недостаточность, преклонный возраст снижают продолжительность жизни после имплантации ЭКС.
Профессор, доктор мединских наук Ю.П. Островский


