 Искусственное кровообращение (ИК) - пока единственный способ добиться пустого и обескровленного сердца, в то же время поддерживая кровообращение во всем остальном теле человека.
Искусственное кровообращение (ИК) - пока единственный способ добиться пустого и обескровленного сердца, в то же время поддерживая кровообращение во всем остальном теле человека.
Искусственное кровообращение характеризуется тремя основными функциями: оксигенация крови, газообмен в тканях и поддержание кровотока в тканях.
Кроме того, важной функцией искусственного кровообращения является контроль температуры тела пациента.
Стандартные компоненты контура искусственного кровообращения (рассматриваются по току крови во время проведения ИК):
- венозные канюли (варианты: для канюляции полых вен, правого предсердия, бедренных вен)
- венозная магистраль (диаметр 1/2 дюйма, материал – поливинилхлорид)
- венозный резервуар (может быть соединен с оксигенатором)
- магистраль от выхода венозного резервуара до основного насоса (диаметр 3/8 дюйма, материал – поливинилхлорид)
- магистраль роликового насоса (диаметр 1/2 дюйма, материал – силикон или поливинилхлорид) или насадка для центрифужного насоса
- магистраль от выхода насоса до входа в оксигенатор (диаметр 3/8 дюйма, материал – поливинилхлорид)
- оксигенатор (мембранный оксигенатор, может быть интегрирован с теплообменником)
- магистраль от выхода оксигенатора до входа в артериальный фильтр (диаметр 3/8 дюйма, материал – поливинилхлорид)
- артериальный фильтр (30-60 микрон) с шунтом (диаметр шунта 3/8 дюйма, материал – поливинилхлорид)
- артериальная магистраль (диаметр 3/8 дюйма, материал – поливинилхлорид)
- артериальная канюля (варианты: для канюляции аорты, магистральных артериальных сосудов - бедренной артерии, подключичной артерии и т.д.).
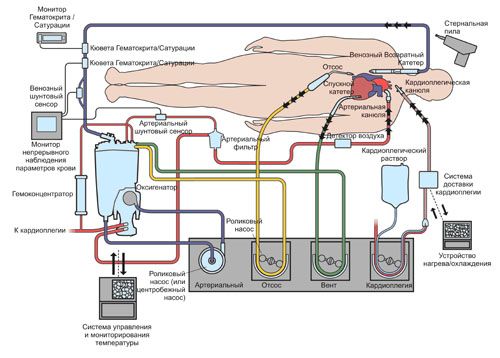
Венозная кровь (с низким содержанием кислорода и высоким содержанием углекислого газа) вытекает из пациента за счет силы гравитации через канюли в полых венах (правом предсердии и т.д.) по венозной магистрали в венозный резервуар. Основной насос аппарата искусственного кровообращения выкачивает эту кровь из венозного резервуара и нагнетает ее в оксигенатор, откуда она попадает в артериальный фильтр и через артериальную линию и соответствующую артериальные канюлю назад в кровеносное русло пациента.
Кроме того, основной контур искусственного кровообращения включает:
- венозный окклюдер/зажим (для регулировки скорости потока по венозной магистрали)
- порты различного диаметра для введения лекарственных препаратов и инфузии растворов на крышке венозного резервуара
- система портов для взятия проб крови для анализа из артериальной и венозной магистралей контура искусственного кровообращения
- система для подключения источников кислорода, воздуха, углекислого газа, газообразных анестетиков
- кардиоплегическая система (как правило, для нее используется дополнительный роликовый насос)
- система температурных датчиков в артериальной, венозной и кардиоплегической линиях
- система магистралей (диаметр 1/3/8 дюйма, материал – поливинилхлорид и силикон) для дренирования крови из операционной раны и/или полостей сердца (как правило, используются дополнительные роликовые насосы)
- система для проведения ультрафильтрации/гемоконцентрации (гемоконцентратор, система магистралей - диаметр 1/дюйма, материал – поливинилхлорид и силикон), может использоваться отдельный роликовый насос
- система для измерения давления крови в магистралях контура искусственного кровообращения (артериальной, венозной, кардиоплегической)
- система контроля уровня крови в резервуарах контура искусственного кровообращения, а так же воздуха в магистралях контура.
Венозные канюли
Техника венозной канюляции описана здесь.
Существует три основных типа венозных канюль: для канюляции полых вен (отдельная канюля для каждой полой вены), канюляции правого предсердия (двухуровневая канюля) и канюляции правого предсердия (канюля типа «Ross basket»).
Канюля типа «Ross basket» представляет собой канюлю большого диаметра с металлическим наконечником, имеющим много боковых отверстий достаточно большого диаметра, предназначена для канюляции правого предсердия, фиксируется турникетом у края металлического наконечника.
Двухуровневая канюля имеет коническую форму, как правило, корпус канюли усилен металлическим каркасом из проволоки для предотвращения перегиба корпуса канюли. Она устанавливается в правом предсердии, так чтобы ее носик находился в нижней полой вене, а проксимальное отверстие располагалось в полости правого предсердия (турникет фиксируется на уровне самого внешнего маркера канюли).
Канюли для отдельной канюляции полых вен устанавливаются или прямо в полые вены (такие канюли, как правило, выбираются изогнутые под 90°, могут так же иметь изогнутый под 90° металлический носик), или через отдельные кисетные швы на правом предсердии (канюли могут быть как прямые, так и изгибаемые) проводятся в полые вены. Кроме того, канюли данного типа для избежания перегиба также могут иметь усиленный металлической проволокой корпус. Как правило, канюли установленные в верхнюю и нижнюю полые вены и обжимаются широкими турникетами (тесьмой) во время проведения искусственного кровообращения для полного дренажа крови пациента в контур ИК. Такое состояние может называться «полное искусственное кровообращение».
Канюляция двухуровневой канюлей выполняется быстрее, может обеспечивать наилучшее дренирование крови из правых отделов сердца в определенных его положениях. При использовании бикавальной канюляции считается, что обеспечивается лучшее охлаждение миокарда, а значит, лучшая защита миокарда от ишемии, предотвращается попадание воздуха в венозную магистраль контура искусственного кровообращения. Этот метод широко используется при планируемом вскрытии «правых» отделов сердца или при вскрытии «левых» отделов и при наличии сообщения между «левыми» и «правыми» отделами (дефект междпредсердной перегородки, открытое овальное окно, дефект межжелудочковой перегородки). При использовании техники «полного ИК» предотвращается согревание миокарда, так как возврат венозной крови идет прямо в контур искусственного кровообращения. Использование канюляции типа «Ross basket» снижает риск повреждения нижней полой вены.
Венозный дренаж
Обычно венозный дренаж происходит по принципу гравитационного сифона: венозный резервуар устанавливается ниже уровня операционного стола пациента, кроме того, венозная линия должна быть полностью заполнена жидкостью (кровь, солевые растворы и т.д.) Неадекватный дренаж (возврат) венозной крови ведет к перерастяжению камер сердца, повышению потребности миокарда в кислороде (т.е. может вызвать или увеличить ишемию миокарда), а так же к неадекватной работе аппарата искусственного кровообращения (снижению объемной скорости перфузии, падению перфузионного давления, нарушению оксигенации тканей пациента и т.д.).
Венозный возврат может быть увеличен путем:
- увеличения объема внутрисосудистой жидкости, снижения комплайнса кровеносных сосудов (все это ведет к росту центрального венозного давления)
- увеличения разницы в уровнях между пациентом и венозным резервуаром
- увеличения диаметра венозных канюль или венозной магистрали.
Проблемы при неадекватном венозном возврате (дренаже) могут быть связаны с:
- неправильной установкой венозных канюль
- неправильным позиционированием сердца при выполнении манипуляций на нем
- перегибом, пережатием венозной линии (например, оставлением зажима)
- гиповолемией или вазодилятацией
- «воздушным замком/пробкой» в венозной линии, нарушающим гравитационный сифон
- повреждением нижней полой вены при установке двухуровневой канюли (редко).
Иногда во время проведения искусственного кровообращения венозный возврат превышает возможность притока крови к полым венам, что происходит к периодическому коллапсу и «присасыванию» полых вен и/или тканей правого предсердия к канюлям, что ведет к снижению (или практически к остановке) венозного дренажа крови в контур искусственного кровообращения. Это выглядит как подергивание сердца, имитирующее сердечные сокращения. Для исправления данной ситуации персоналу следует снизить темп венозного возврата в контур ИК, например увеличив окклюзию венозной линии специальным устройством или зажимом.
Иногда, особенно при использовании длинной бедренной венозной канюли, бывает полезно использовать систему для усиления венозного дренажа. Это может быть выполнено тремя путями:
- использование роликового насоса в венозной линии перед венозным резервуаром (наименее подходящий вариант)
- использование центрифужного насоса в венозной линии перед венозным резервуаром
- использование системы вакуумного усиления венозного возврата.
Очень важно избегать очень сильного разрежения в линии венозного возврата, особенно при использовании роликового насоса.
Артериальная канюля
Техника артериальной канюляции обсуждены здесь.
Существуют различные варианты формы канюли, но всегда самым узким местом контура искусственного кровообращения будет артериальная канюля, установленная в аорту, которая ограничивает кровоток и должна быть настолько короткая, насколько это возможно. Высокий кровоток через узкую артериальную канюлю генерирует высокий градиент давления, турбуленцию и кавитацию. Носик канюли изготовлен так, чтобы снизить скорость потока струи крови на выходе из артериальной канюли, чтобы предотвратить смещение атероматозной бляшки, образование расслоения стенки аорты, снизить скорость кровотока в магистральных сосудах шеи, а также снизить уровень гемолиза крови. Артериальная канюля выбирается на основании лучшего соотношения внутреннего (ID) и внешнего диаметров (OD), а так же показателей ее гидродинамики (соотношение градиента давления на выходе из канюли и потока жидкости/крови).
Кровеносные магистрали и коннекторы
Кровеносные магистрали и коннекторы изготавливаются из нетоксических, неиммуногенных, неаллергических и немутагенных материалов. Они должны быть водонепроницаемы, прозрачные, достаточно гибкие и в то же время прочные, химически инертные, ровные и гладкие, а так же пригодные для производства в большом количестве. Самыми подходящими материалами для этого могут быть поливинилхлорид, тефлон, титан, силикон.
Кровеносные магистрали часто покрываются гепаринсодержащими компонентами. Перед началом искусственного кровообращения для удаления воздуха кровеносные магистрали заполняются кровезамещающими растворами, компонентами крови или их комбинацией. Этот объем жидкости называется объемом первичного заполнения, и для него требуется от 1 000 до 2 000 мл вышеуказанных компонентов. Все эти компоненты первичного заполнения после начала искусственного кровообращения попадают в систему кровообращения пациента. Очень важно для снижения градиента давления в кровеносных магистралях подобрать баланс между диаметром магистралей и получаемым объемом первичного заполнения, чтобы снизить степень гемодилюции. Одним из решением данной проблемы может быть уменьшение длины кровеносных магистралей.
Насосы
Насосы крови могут быть перистальтические или центрифужные.
Перистальтические насосы крови, которые наиболее широко используются в настоящее время, состоят из кровеносной магистрали, расположенной в металлическом корпусе. Два ролика, расположенные на 180° друг от друга, вращаются так, что в каждый момент времени один из роликов сжимает кровеносную магистраль. Движение ролика толкает кровь перед собой, чем и создает поток крови на выходе из насоса. Слишком сильный прижим ролика к стенкам кровеносной магистрали может привести к гемолизу. Недостаточный прижим ролика также может вызывать гемолиз и, кроме того, снижать скорость кровотока, генерируемый насосом. Степень снижения кровотока зависит от диаметра кровеносной магистрали, заправленной в насос, скорости оборотов наоса, а также от степени выраженности недостаточности прижима ролика.
Роликовые насосы используются для создания потока крови в аорте пациента, для введения кардиоплегического раствора, для дренажа крови из операционной раны и полостей сердца. Если кровеносная магистраль будет пережата зажимом или перегнута, роликовые насосы могут создавать очень высокие уровни положительного или отрицательного давления. Для предотвращения разрыва кровеносных магистралей и коннекторов следует проверить их на наличие перегибов (окклюзий) на всех участках, включая стерильные части на операционном столе, исправить найденные проблемы или снизить скорость работы насоса.
Центрифужный насос представляет собой конусообразную камеру, имеющую внутри себя второй конус (с лопатками или без них), который вращается со скоростью 2 000-3 000 оборотов в минуту и создает поток крови. Центрифужные насосы являются насосами неокклюзирующего типа, а также зависят от характера постнагрузки: повышение давления на выходе насоса приводит к снижению производительности насоса, вплоть до возникновения обратного тока жидкости через центрифужный насос. Если центрифужный насос через артериальную магистраль подключен к пациенту и находится в выключенном состоянии, кровеносная магистраль должна быть пережата зажимом, так может возникнуть ретроградный ток крови из пациента в контур искусственного кровообращения, а также попасть воздух. Если внутрь центрифужного насоса попадет более 50 мл воздуха, то это приведет к остановке насосной функции центрифужного насоса.
Оксигенатор
Существует два типа оксигенаторов: мембранные оксигенаторы (наиболее широко используемые) и пузырьковые оксигенаторы (в настоящее время практически не используются). Большинство оксигенаторов являются составной частью систем, в которые интегрированы теплообменник, венозный резервуар, артериальный фильтр, краны, коннекторы для магистралей и т.д.
Мембранный оксигенатор может иметь или «истинную мембрану», которая полностью отделяет кровь от газов, и газы попадают в кровь путем диффузии (так же как это происходит в легких человека), или мембрану, которая содержит микропоры, через которые происходит перемещение молекул газа из/в кровь. Так как площадь поверхности «истинных мембран» для обеспечения адекватного газообмена достаточно большая, то в клинической практике наиболее распространено получило использование оксигенаторов на основе микропористых мембран.
Существуют оксигенаторы с двумя принципиально важными дизайнами:
1 – кровь течет внутри или снаружи полых волокон;
2 – кровь и газ отделены друг от друга многократно сложенными пластинами из пористых мембран.
Пузырьковые оксигенаторы состоят из двух камер. Поток венозной крови попадает в первую смешивающую камеру, где кровь перемешивается с потоком газа, что приводит к формированию огромного количества пузырьков, на поверхности которых и происходит процесс газообмена. После этого кровь попадает в камеру пеногашения, имеющую в своей конструкции пеногасящий элемент. Основным отличием пузырьковых оксигенаторов от мембранных является то, что:
- первые несколько минут работы мембранного оксигенатора происходит активация процессов иммуновоспалительного ответа и системы комплемента, которая снижается после адгезии белков на поверхности мембран, в то время как в пузырьковом оксигенаторе процессы активации возникают в каждом новом пузырьке газа. Таким образом, для большей безопасности пациента и для длительных перфузий, предпочтительно использовать мембранные оксигенаторы
- при использовании мембранных оксигенаторов имеет место больший перепад давления между насосом крови и артериальным фильтром
- уровень вентиляции и оксигенации легче регулируется в мембранном оксигенаторе, чем в пузырьковом (изменением скорости потока газа и величиной процента кислорода в газовой смеси/FiO2).
Теплообменник
Теплообменник может нагревать или охлаждать кровь пациента, таким образом, контролируя температуру тела пациента, а также температуру кардиоплегического раствора. Как правило, теплообменник интегрирован с оксигенатором и расположен проксимально от оксигенатора, для того чтобы предотвратить образование пузырьков газа в потоке крови при изменении ее температуры (например, если подогревать насыщенную кислородом кровь). Температура воды, циркулирующая через теплобменник, может быть составлять от 5 до 42”С (при повышении температуры до 42”С может начаться денатурация белков плазмы человека). Таким образом, кровь может охлаждаться быстрее (0,5-17”С/мин) и большим градиентом, чем согреваться (0,2-0,5”С/мин). Темп охлаждения при снижении температуры крови пациента также должен снижаться по тем же соображениям. Температура тела пациента и температура перфузата (кровь в контуре искусственного кровообращения) не должна отличаться более чем 15°С.



