 До последнего времени функция правого желудочка находилась в тени масштабных исследований функции левого желудочка. Однако в последнее время важность правого желудочка стала очевидной. Первоначально исследователи пытались экстраполировать данные, полученные о левом желудочке, на правый желудочек, но с самого начала стало ясно, что левый и правый желудочки значительно отличаются по многим параметрам.
До последнего времени функция правого желудочка находилась в тени масштабных исследований функции левого желудочка. Однако в последнее время важность правого желудочка стала очевидной. Первоначально исследователи пытались экстраполировать данные, полученные о левом желудочке, на правый желудочек, но с самого начала стало ясно, что левый и правый желудочки значительно отличаются по многим параметрам.
Исторически понимание функции правого желудочка ограничивалось восприятием контрактильной функции правого желудочка как гемодинамически незначительной. Сейчас правожелудочковая недостаточность широко обсуждается среди профессиональных сообществ, однако, многочисленные вопросы касательно данной тематики так и не исследованы в полной мере. Во многом это вызвано различиями в подходах оценки и анализа функции правого желудочка, отсутствием стандартов и базисных знаний. Данный обзор – попытка систематизировать имеющиеся данные, вычленить наиболее важные аспекты правожелудочковой недостаточности, определить дальнейшие направления для исследований.
Этиология
Генетика, эмбриология, патофизиология
Диагностика
Лечение
Заключение. Литература
Этиология
С самого начала нужно отметить, что «чистая», или первичная, правожелудочковая недостаточность выявляется крайне редко и, в большинстве случаев, связана с врожденными пороками сердца. Вторичная правожелудочковая недостаточность ассоциирована с широким кругом заболеваний как сердечной, так и несердечной природы. В общем, правожелудочковая недостаточность является следствием различных патогенетических путей, в конечном итоге приводящая к провалу адаптации: клиническим проявлениям, осложнениям, ошибочным диагнозам и ко всему тому, чего, к сожалению, опасаются клиницисты. Таким образом, правожелудочковую недостаточность можно представить как синдром с различной этиологией. Наиболее полную классификацию этиологических причин мы нашли у Haddad et al. Также в данной работе предлагается таблица патогномичных маркеров дисфункции правого желудочка в сочетании с клиническим статусом и прогнозом. Все причины, учтенные в классификации Haddad, являются предикторами физической невозможности сокращений правого желудочка в данных гемодинамических условиях. Клиницисты, как правило, сталкиваются с комбинацией причин, приводящих к острой правожелудочковой недостаточности, это состояние особенно актуально для кардиохирургии, анестезиологии и реанимации.
Правожелудочковая недостаточность ассоциирована с множеством заболеваний и патологических процессов, включая легочную гипертензию, вызываемую заболеваниями легочной паренхимы и/или заболеваниями сосудов легких (cor pulmonale). Другие заболевания, ведущие к правожелудочковой недостаточности с различным патогенезом, включают: тотальную, левожелудочковую или правожелудочковую кардиомиопатию; правожелудочковую ишемию и/или инфаркт; заболевания трикуспидального и/или клапана легочной артерии; лево-правые шунты. Также необходимо особенно выделить трансплантацию сердца, как состояние с усложненным подходом. Беляков А. В. с соавт. в своих исследованиях определили, что послеоперационный стресс при операциях пульмонэктомии вызывает функциональную миокардиальную недостаточность. Также было установлено, что уровень креатинфосфокиназы (КФК) и сердечный выброс (СВ) напрямую коррелируют с постоперационной депрессией миокарда правого желудочка и продолжительностью адаптации правого желудочка.
В клинической практике наиболее распространенной причиной дисфункции правого желудочка является хроническая левожелудочковая недостаточность. Левожелудочковая недостаточность может провоцировать правожелудочковую через различные механизмы:
- левожелудочковая недостаточность увеличивает постнагрузку через увеличение венозного легочного и, особенно, артериального легочного давления
- кардиомиопатические изменения миокарда могут затрагивать и правый желудочек
- ишемия также может распространяться на оба желудочка
- левожелудочковая дисфункция может приводить к снижению систолического давления наполнения в коронарном бассейне правого желудочка, которое, в свою очередь, может явиться значимой детерминантой правожелудочковой функции
- развитие механизма желудочковой взаимозависимости на фоне дисфункции перегородки
- дилатация левого желудочка в ограниченном перикардиальном компартменте может приводить к нарушению диастолической функции правого желудочка.
С другой стороны, перегрузка объемом правого желудочка, которая может случиться в ситуациях с легочной гипертензией, способна скомпрометировать функцию левого желудочка и, соответственно, привести к недостаточности левого желудочка. Кроме того, при декомпенсации правого желудочка, спровоцированной левожелудочковой недостаточностью, поддержка объемного потока, необходимого для адекватной преднагрузки, становится невыполнимой задачей. Вследствие комплексного влияния на правый желудочек со стороны левого желудочка, оценка состояния правого желудочка может быть чувствительным индикатором предстоящей декомпенсации или плохого прогноза.
Второй по значимости причиной правожелудочковой недостаточности является легочная гипертензия. Пересмотренная классификация легочной гипертензии была принята на третьей мировой конференции в Венеции в 2003 г. (Third World Conference in Venice). Данная классификация разделяет легочную гипертензию на случаи, в которых первично поражаются:
- легочные артерии (артериальная легочная гипертензия)
- легочная венозная система, и
- случаи поражения легочных сосудов в связи с заболеваниями легких, гиповентиляции, ТЭЛА
Наконец, недостаточность правого желудочка сочетается с широким спектром врожденных аномалий, таких как, тетрада Фалло, транспозиция магистральных сосудов, аномалия Эбштейна, синдром Эйзенменгера и другие.
Генетика, эмбриология, патофизиология
Генетические исследования морфогенеза сердца показали, что правый и левый желудочки берут свое происхождение от разных прогениторных клеток и разных сайтов: первичная кардиогенная область образует предсердные камеры и левый желудочек, тогда как клетки передней кардиогенной зоны развиваются в выводящий тракт и правый желудочек. Исследования двух основных камероспецифичных транскрипционных факторов HAND1 и HAND2, и исследования на мышах с выключенными генами привели к открытию камероспецифичной экспрессии генов с различными транскрипционными механизмами, ведущей к правожелудочковой и левожелудочковой формации. Также был открыт фактор транскрипции Bop (регулятор развития правого желудочка), который в настоящее время признан транскрипционной мишенью для гена, усиливающего экспрессию – фактора 2C в миоците. Для экспрессии HAND2 и формирования правого желудочка необходимым является и фактор GATA4, который регулирует экспрессию генов α-миозиновых тяжелых цепей в миокарде и генов, кодирующих предсердный натрийуретический пептид.
Значимость функции правого желудочка проявляется еще во время внутриутробного развития. Наличие овального окна (foramen ovale) и артериального протока (ductus arteriosus) делает пред - и постнагрузку одинаковой для правого и левого желудочка, однако, правый желудочек изгоняет примерно 66% сердечного выброса. На ранних стадиях роста и развития левый и правый желудочки имеют одинаковый коронарный кровоток (в пересчете на грамм миокарда). Тем не менее, с уменьшением легочного сосудистого сопротивления , которое происходит при рождении (закрытие foramen ovale и ductus arteriosus), функция желудочков резко изменяется. Уменьшение легочного сосудистого сопротивления сопровождается редукцией давления и коронарного кровотока в правом желудочке с сопутствующим увеличением кровотока в миокарде левого желудочка. В результате левый желудочек быстро превращается в толстостенную хорошо сокращающуюся камеру. Правый желудочек, наоборот, становится тонкостенной хорошо растяжимой, однако, слабо сокращающейся камерой.
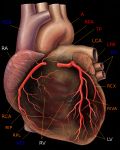
Кровоснабжение правого желудочка в основном осуществляется из системы правой коронарной артерии, которая снабжает кровью свободную стенку правого желудочка на задней, правой латеральной и передней поверхностях сердца. Правая коронарная артерия также кровоснабжает нижнюю треть межжелудочковой перегородки. Сверх того, правый желудочек получает кровь из передней нисходящей ветви левой коронарной артерии. Эта артерия также питает часть передней стенки левого желудочка и передние ⅔ межжелудочковой перегородки. Распределение по времени коронарного кровотока правого желудочка уникально, так как он осуществляется и в систолу, и в диастолу. Напротив, основной коронарный кровоток левого желудочка приходится на диастолу. В этой связи многие авторы выдвигают идею того, что такой «двойной» кровоток правого желудочка является причиной сравнительно малого процента выраженной дисфункции правого желудочка, что имеет значение при окклюзии правой коронарной артерии.
Клетки млекопитающих животных, включая миоциты левого желудочка, адаптируются к гипоксии через положительную регуляцию HIF-1, которая приводит к транскрипции метаболических генов и генов, ответственных за ангиогенез. Это также было подтверждено на животных моделях и человеческих миоцитах, подвергшихся ишемии. Делеция HIF-1 приводит к уменьшению экспрессии данных генов, что, в свою очередь, ведет к фиброзу миокарда, повреждению миоцитов избытком ионов кальция, и, впоследствии, систолической и диастолической дисфункции левого желудочка. Стимуляция HIF-1 с помощью генной терапии, как было показано на крысиных моделях с инфарктом миокарда, приводит к стимуляции экспрессии VEGF и активизирует ангионеогенез. Механизм адаптации к гипоксии для правого желудочка пока не описан. Reddy et al. показали несостоятельность адаптации правого желудочка к гипоксии у пациентов с тетрадой Фалло. Нарастающая гипоксия, несмотря на стимуляцию ангиогенических и метаболических генов, приводила к снижению адаптивных возможностей. Для выяснения вклада мальадаптации правого желудочка в его диастолическую функцию у пациентов с тетрадой Фалло ученые исследовали экспрессию генов, причастных к диастолической дисфункции, таких как, Ca++ связывающие и структурные гены, коллаген и коннектин. Соответствующая экспрессия генов была выражена как кратная разница цианотических и ацианотических правых желудочков.
Гипертрофия, вторичная к перегрузке объемом, также может индуцировать ангиогенические и метаболические гены с целью покрытия нарастающих потребностей в питании. Reddy et al. дифференцируют это состояние путем изучения уровня экспрессии мозгового натрийуретического пептида (brain natriuretic peptide, BNP), маркера желудочковой гипертрофии. Экспрессия BNP не имела существенных отличий между цианотической и ацианотической группами, что свидетельствует о том, что данная разница в экспрессии генов была скорее вторичной к разнице в тяжести гипоксии. Они также показали, что экспрессия антиоксиданта глутатионпероксидазы была ниже у пациентов с более выраженной гипоксией правого желудочка. Более высокие уровни лактата у пациентов с низкой экспрессией метаболических и ангиогенических генов в дальнейшем указывает на слабую способность правого желудочка противостоять окислительному стрессу, связанному с хирургической коррекцией. Таким образом, у пациентов с тетрадой Фалло наблюдается несостоятельность адаптивных механизмов правого желудочка к хронической гипоксии, поэтому, ранняя хирургическая коррекция данной патологии может быть кардиопротективной.
У пациентов с идиопатической артериальной легочной гипертензией степень гипертрофии правого желудочка, измеренной как толщина стенки правого желудочка, варьируется в относительно широких пределах (от 0,6 до 1,5 см.) И, также как при недостаточности левого желудочка, перегрузка давлением правого желудочка является основанием для изменений в экспрессии генов у пациентов с идиопатической артериальной легочной гипертензией. В частности, происходит возврат к фетальному механизму синтеза посредством снижения α-миозиновых тяжелых цепей и увеличением экспрессии тяжелых цепей фетального β-миозина. На функцию правого желудочка оказывают влияние как внутренние, например, контрактильный статус миокарда, так и внешние факторы: преднагрузка, постнагрузка, стесняющий эффект перикарда, интраперикардиальное давление, перфузионное давление правой коронарной артерии, функция левого желудочка и контрактильный статус межжелудочковой перегородки. Для поддержания нормальной функции правого желудочка необходимо учитывать оба вида факторов: определяющих контрактильную функцию и насосную функцию правого желудочка. По существу, при определенных условиях нагрузки, угнетение насосной функции правого желудочка может возникнуть даже при отсутствии какого-либо снижения сократимости миокарда. И наоборот, депрессия миокарда затушевывается на фоне благоприятной нагрузки, в конечном итоге это может приводить к выраженным нарушениям насосной функции. Правый желудочек особенно чувствителен к какому-либо увеличению постнагрузки. По сравнению с левым желудочком, который поддерживает относительно постоянный по объему выброс при изменяющейся в широких пределах постнагрузке, выброс правого желудочка круто падает при минимальных изменениях в постнагрузке. Клинически это манифестирует прогрессивным снижением фракции выброса правого желудочка, которое имеет особенное значение в ситуациях с возросшей постнагрузкой у пациентов с артериальной легочной гипертензией, ТЭЛА, митральных пороках (с вторичной легочной гипертензией), респираторном дистресс-синдроме взрослых.
Особого внимания в нашем обзоре заслуживает правожелудочковая недостаточность у пациентов с трансплантацией сердца. Имеются данные, свидетельствующие о соответствующем увеличении миокардиального фиброза в течение двух постоперационных недель. Ранний фиброз, вызванный состояниями сопутствовавшими трансплантации, т.е. смертью мозга, ишемией, реперфузионной травмой, иммуносупрессией, реакцией отторжения, не может коррелировать с каким-то одним параметром. Триггером для этих изменений может служить субклиническое повреждение донорского сердца. Реципиенты с выраженным фиброзом трансплантата имеют более высокий риск смерти после трансплантации. Другое исследование показало, что смерть мозга вызывает значительное угнетение функции левого и правого желудочков. Повреждение правого желудочка через два часа после смерти мозга более выражено, чем левого желудочка. Эти данные поднимают вопрос первичного повреждения правого желудочка во время поддержания сердца при трансплантации и требуют дальнейших исследований. Более детальные механизмы патогенеза на тканевом и биохимическом уровнях, показывающие роль вегетативной нервной системы, ренин-ангиотензиновой системы, натрийуретического пептида, эндотелиальной системы и воздействие цитокинов у пациентов с правожелудочковой недостаточностью достаточно хорошо описаны и широко изучаются. Все эти механизмы являются универсальными и в данный момент используются для поиска лечебных стратегий.
Диагностика
Диагностика правожелудочковой недостаточности - одна из наиболее важных задач клинической медицины и академических исследований. Тем не менее, общеизвестно, что функцию правого желудочка сложно оценить из-за особенностей геометрии, взаимосвязи с левым желудочком и чувствительности к изменениям легочного давления. Используя гемодинамические параметры, мы можем оценить давление в правом предсердии, конечно-диастолическое давление в правом желудочке, сердечный индекс, давление в легочной артерии и коэффициент потребления кислорода смешанной венозной крови.
При помощи физических упражнений можно провести пробу шестиминутной ходьбы и другие сердечно-легочные нагрузочные тесты. И наконец, по данным эхокардиографии можно определить трикуспидальный градиент, выпот в перикарде, EI левого желудочка, время изгнания правого желудочка, индекс Тei, площадь правого предсердия, трикуспидальную регургитацию объем/площадь, диаметры правого желудочка, приближенный сердечный выброс и др. Измерение давления в легочной артерии повсеместно используется у пациентов с легочной гипертензией, хотя и нет обоснованной связи между давлением, толерантностью к нагрузке и прогнозу.
Давление легочной артерии остается жизненно необходимым параметром, так как нельзя не согласиться с тем, что первопричиной смерти у пациентов с легочной гипертензией является правожелудочковая недостаточность, прямо или косвенно вызванная подъемом давления в легочном стволе. Любое лечебное вмешательство, которое снизит легочное давление до нормальных величин, при сохранении достаточного сердечного выброса и оксигенации, в конечном итоге приведет к приемлемому восстановлению функции правого желудочка. Как это наблюдается у пациентов после трансплантации легких, операциях легочной эндартерэктомии и малой порции пациентов, которые отвечают на медикаментозную терапию. Несмотря на это, давление легочной артерии дает нам немного меньше информации о функции правого желудочка, чем системное артериальное давление говорит нам о функции левого желудочка. Кроме того, измерения, которые не зависят напрямую от функции правого желудочка, например, давление легочной артерии и легочное сосудистое сопротивление, являются плохими показателями прогноза, даже тогда, когда постнагрузка выступает доминирующей причиной правожелудочковой недостаточности. По-видимому, существует пороговый уровень постнагрузки, выше которого реакция правого желудочка становится главной детерминантой выживания и качества жизни.
Другие диагностические методики оценки систолической и диастолической функции правого желудочка, которые пока еще не нашли широкого применения в клинической практике включают: фракция выброса правого желудочка, напряжение на стенку правого желудочка (wall stress), индекс Tei, tricuspidannular plane systolic excursion (TAPSE), измерение систолического подъема плоскости кольца трехстворчатого клапана (measurement of systolic elevation of tricuspid annular plane), tricuspid deceleration duration, соотношение E/E0, tricuspid annular velocity. Несмотря на возможность обследования большинства пациентов, ценность данных методов до конца не ясна, а результаты исследований противоречивы. Сейчас трудно предсказать потенциальную роль данных показателей в будущем. J.G. Coghlan в своей работе предлагает методики для оценки функции правого желудочка, включая эхокардиографию, МРТ, медицинскую радиологию, прерывистый и/или постоянный гемодинамический мониторинг, анализ уровня натрийуретического пептида, наряду с использованием сердечно-легочных нагрузочных тестов. Проба шестиминутной ходьбы, 2D и доплеровская эхокардиография, инвазивный гемодинамический мониторинг, несмотря на их очевидные ограничения, остаются камнем преткновения в оценке функции правого желудочка в настоящий момент. Быстро нарастает роль КТ и МРТ, однако стандартизация оценок и нормальных значений требует дальнейшей работы.
Несмотря на отсутствие хорошо организованных проспективных исследований, натрийуретический пептид вошел в клиническую практику благодаря плотности опубликованных на сегодняшний день работ и сравнительной легкости в применении. Gregory D. Lewis et al. изучили неэффективную вентиляцию во время упражнений и установили аномальную связь между вентиляцией и продукцией углекислого газа (VE/VCO2 градиент). Они обнаружили, что во время физической нагрузки у пациентов с систолической сердечной недостаточностью и вторичной легочной гипертензией эффективность вентиляции тесно связана с функцией правого желудочка и легочным сосудистым тонусом. Эта находка в будущем может отразиться на развитии стратегий оценки функции правого желудочка и легчной гипертензии и, возможно, войдет в клиническое применение.
В заключение, интраоперационная диагностика и донорское сердце. Birks et al. исследовали экспрессию фактора некроза опухолей (TNF-α) в кардиомиоцитах донорского сердца. Они предполагают, что экспрессия TNF-α в донорском сердце является важным предиктором развития ранней правожелудочковой недостаточности после трансплантации, и что TNF-a может способствовать дисфункции миокарда. Также данные указывают, что TNF-a оказывает воздействие не через NO-зависимый механизм, а имеет иные точки приложения. Фармакологическая модуляция экспрессии TNF-α в донорском органе уменьшает посттрансплантационную дисфункцию желудочков. Simone et al в своем исследовании об интраоперационной оценке объема и функции правого желудочка пришли к выводу, что трехмерная эхокардиография и волюметрическая термодилюция являются легкодоступными инструментами для интраоперационной оценки функции правого желудочка.
Все эти исследования открывают новые перспективы для анализа функции правого желудочка, целью которых, в конечном счете, является улучшение качества лечения пациентов с нарушенной сердечной функцией. Для оценки функции правого желудочка было предложено масса критериев и мер, с их помощью получены различные результаты. Но в данный момент, ни один из критериев не дает клиницисту исчерпывающей информации о систолической и диастолической функции правого желудочка.
Более того для практической медицины требуется методики, которые широко доступны, легко внедряемы, обладают высокой производительностью и дают четкую информацию о прогнозе, эффективности лечения, и, таким образом, обеспечивают обратную связь при оценке качества лечебного вмешательства. Нет сомнений, любые методики должны быть унифицированы, и точная оценка функции правого желудочка имеет первостепенное значение в развитии логичной пациент центрированной стратегии. Особого внимания заслуживают инструменты, которые могут использоваться для мониторинга функции правого желудочка повседневно во время кардиохирургических вмешательств и у кровати больного.
Лечение
Для обращения вспять этого потенциально смертельного процесса нужно выявить потенциально обратимую этиологию. Haddad et al. рассматривают общий механизм терапии правожелудочковой недостаточности и анализируют существующие стратегии. В целом, авторы придерживаются разных точек зрения на этот счет. Одни принимают за отправную точку функцию правого желудочка, другие – взаимосвязь правого и левого желудочков, третьи – функцию правого желудочка в тесной связи с легочной артерией.
Комбинированный подход должен основываться на одновременной элиминации индукторов и синдромальной терапии. Для решения вопроса о выборе терапевтического подхода мы первоначально должны определиться с эффектом, которого мы хотим достичь. Однако сих пор существует масса противоречий, требующих скорейшего пересмотра. Блок проблем связан с «неидеальной» диагностикой. Ошибочные диагнозы с течением времени приводят к необратимым состояниям, поэтому своевременная диагностика правожелудочковой недостаточности является первостепенной задачей для клинициста. Ведь профилактика – лучшее лечение! Отсюда и усилия многих хирургов найти подходящую технику операции для данного заболевания. Наблюдения об увеличении выживаемости пациентов с легочной гипертензией и открытым овальным окном привели к гипотезе, что предсердная септостомия, которая приводит к декомпрессии правого желудочка и увеличению шунта справа налево, может оказаться полезной при правожелудочковой недостаточности. Реакция на септостомию при легочной гипертензии сильно варьирует. И на данный момент эту операцию нужно рассматривать как паллиативную.
Masami Takagaki et al. в своем исследовании врожденных пороков со стойкой перегрузкой объемом правого желудочка выяснили: процедура тотального исключения правого желудочка обеспечивает эффективную нагрузку объемом, восстанавливает цилиндрическую форму и улучшает систолическую функцию левого желудочка, что в итоге приводит к увеличению сердечного выброса. Они считают данную процедуру перспективной для пациентов с изолированной декомпенсированной правожелудочковой недостаточностью, вызванной перегрузкой объемом.
Frigiola et al. использовали противоположный подход – операция по реставрации правого желудочка во время имплантации клапана легочной артерии. Они позиционируют данную операцию как безопасную, простую и эффективную процедуру, которая может сочетаться с операцией имплантации клапана легочной артерии у пациентов с серьезной дилатацией правого желудочка и аневризматичеким/акинетическим выносящим трактом правого желудочка. Авторы считают, что в случае недостаточности правого желудочка в сочетании с дилатацией необходима концепция «клапан-желудочек». Данные полученные в исследовании обнадеживают, однако требуются большее число случаев наблюдений и более длительные сроки, чтобы подтвердить обоснованность их подхода. Текущие терапевтические стратегии, направленные на элиминацию легочной вазоконстрикции, клеточной пролиферации и тромботических факторов, ставят своей задачей улучшение качества жизни и увеличение выживаемости большего числа пациентов с тяжелой легочной артериальной гипертензией.
Подобно тому, как терапия с использованием снижающих постнагрузку агентов, антагонистов β-рецепторов, инотропов и диуретиков улучшает функциональный статус и прогноз у пациентов с левожелудочковой недостаточностью. Более того, хорошая чувствительность к легочным вазодилататорам ассоциирована с лучшим прогнозом и выживанием пациентов с высокой степенью сердечной недостаточности. К сожалению, снижение постнагрузки не может быть достигнуто во многих случаях. Другие возможности, как, например, утолщение стенки правого желудочка либо уход от фетальной программы экспрессии генов пока еще не были исследованы в качестве потенциального лечения. Постоянная внутривенная инфузия эпопростенола у пациентов с легочной гипертензией улучшает функцию правого желудочка. Также как и использование неселективного антагониста эндотелиновых рецепторов бозентана приводит к схожему улучшению функции правого желудочка, что подтверждается эхокардиографически.
Тем не менее, конкретные эффекты и последствия для миокарда после применения данных лекарственных средств до конца не изучены. В любом случае, в клинической практике прежде всего необходимо нормализовать объем и функцию левых отделов. Правый желудочек подчиняется собственному закону Старлинга, и, несмотря на то, что дисфункция правого желудочка обычно требует большего объема для адекватного наполнения левой половины сердца, перерастяжение правого желудочка также ухудшает его функцию. Рациональное использование позитивного давления в конце выдоха (PEEP) с целью расправления ателектазов и гипервентиляции может снизить вклад легочной вазоконстрикции, вызванной гипоксией и гиперкарбией. Использование внутривенных вазодилататоров (нитропруссид, нитроглицерин, толазолин (PGI2), гидралазин, простациклин, аденозин, никардипин и др.) для уменьшения легочного сосудистого сопротивления часто ограничено системной гипертензией. Инотропные средства (чаще всего милринон, который также обладает и вазодилатирующим эффектом) могут быть полезны. Поскольку внутривенные вазодилятаторы не селективны к легочным сосудам, возможно, местное их введение может быть более эффективным в снижении легочного сосудистого сопротивления без системной гипотензии. Ингаляции оксида азота (NO) и PGI2 обладают сопоставимым эффектом. Такая терапия также может улучшить оксигенацию посредством шунтирования крови в вентилируемые отделы легких.
И в конце об имплантации искусственного желудочка и трансплантации. У пациентов с острой правожелудочковой недостаточностью, рефрактерной к медикаментозной терапии, механическая поддержка с использованием искусственного правого желудочка может служить как мост к трансплантации или выздоровлению. Наиболее общими показанием к использованию поддерживающего устройства является: правожелудочковая недостаточность, ассоциированная с искусственным левым желудочком, трансплантация сердца, массивная ТЭЛА. Использование поддерживающего устройства на постоянной основе у пациентов с высокой степенью правожелудочковой недостаточности до настоящего времени не изучено. Trumble et al. описывает начальные испытания на свиньях временного правожелудочкового поддерживающего устройства, которое работает по принципу прямой компрессии правого желудочка. Система представляет собой блинобразный силиконовый баллон (5 см в диаметре), соединенный с приводом консоли, который обеспечивает 65-мл пневматический пульс во время систолы сердца. В своем исследовании они пришли к выводу, что данный метод, так называемой копульсации, эффективен для краткосрочной поддержки правого желудочка. Однако трудно поверить в то, что данное устройство может конкурировать с помповыми поддерживающими устройствами и в будущем может иметь хоть какое-либо применение.
Трансплантация сердца может рассматриваться у отдельных больных с прогрессирующей и рефрактерной к другой терапии правожелудочковой недостаточности. Первоначально считалось, что такие пациенты с правожелудочковой недостаточностью, вторичной к легочной гипертензии могут быть кандидатами только для трансплантации комплекса сердце-легкие. Однако, в связи с нехваткой органов, пересадка легких была произведена многим пациентах и с хорошим результатом. Однолетняя выживаемость пациентов с легочной гипертензией и трансплантацией легких составляет ≈ 65% - 75%. Предикторы стойкой правожелудочковой недостаточности после трансплантации легких на данный момент не изучены в достаточной мере. Пациентов со сложными врожденными пороками сердца в сочетании с легочной гипертензией необходимо рассматривать как кандидатов для трансплантации сердце-легкие. Пациенты с рефрактерной правожелудочковой недостаточностью в сочетании с левожелудочковой недостаточностью или пациенты с аритмогенной дисплазией правого желудочка и рефрактерной тахиаритмией могут рассматриваться для трансплантации сердца даже при отсутствии серьезной легочной гипертензии.
В последние годы появилось множество работ с использованием стволовых клеток. Тысячи исследователей с большим энтузиазмом постоянно работают по этой теме. Большинство работ, конечно же, относятся к исследованиям левого желудочка. Возможно, в ближайшем будущем ученые добьются успеха, тогда мы сможем обсудить альтернативные методики лечения правожелудочковой недостаточности.
Заключение
Кардиология одна из наиболее быстро развивающихся отраслей медицины. С течением времени некоторые проблемы, такие как правожелудочковая недостаточность, которые ранее казались незначительными, начинают занимать доминирующие позиции. В нашем обзоре мы постарались показать важность правого желудочка и правожелудочковой недостаточности, определить существующие тенденции и подходы. В соответствии с этим, в будущем ученые должны уделить пристальное внимание исследованиям, связанным с данной проблемой. Развитие технологий, особенно компьютеризированных методов диагностики, как трехмерная эхокардиография, МРТ и миниинвазивный мониторинг в сочетании с биомаркерами, даст нам достаточно полное представление о правом желудочке и правожелудочковой недостаточности. Исследователи в области молекулярной биологии и патофизиологии должны быть нацелены на поиск тригерных механизмов, которые ведут к потере адаптации и правожелудочковой недостаточности. Стратегия лечения данной патологии должна быть пересмотрена в деталях. Даже на теперешнем этапе, взаимодействие медицинских сообществ может дать начало новой концепции правожелудочковой недостаточности, создать новые стандарты и протоколы для диагностики и лечения правожелудочковой недостаточности.
Хирургическое лечение сердечной недостаточности в Беларуси - европейское качество за разумную цену
Медицинский институт при Шанхайском университете транспорта, Шанхай, Китай
Литература
1. François Haddad, Ramona Doyle, Daniel J. Murphy and Sharon A. Hunt: Right Ventricular Function in Cardiovascular Disease, Part II: Pathophysiology, Clinical Importance, and Management of Right Ventricular Failure. Circ. 2008;117;1717-1731
2. Norbert F. Voelkel, Robert A. Quaife, Leslie A. Leinwand et al.: Right Ventricular Function and Failure: Report of a National Heart, Lung, and Blood Institute Working Group on Cellular and Molecular Mechanisms of Right Heart Failure. Circ. 2006;114;1883-1891
3. Achim Koch, Cornelius Geil-Bierschenk, Ralf Rieker et al.: Morphometric changes of the right ventricle in the first two weeks after clinical heart transplantation: analysis of myocardial biopsies from patients with complicated versus uncomplicated course. Eur J Cardiothorac Surg 2006;30:370-378
4. А V. Belyakov, V. T. Sеlivanenko, P. P. Shipulin: postoperative stress as the cause of functional myocardial failure. Ukr. J of biology and medicine progress. 2006,1(7); 20-24.
5. Simonneau G, Galie N, Rubin LJ, Langleben D, Seeger W, Domenighetti G, Gibbs S, Lebrec D, Speich R, Beghetti M, Rich S, Fishman A: Clinical classification of pulmonary hypertension. J Am Coll Cardiol. 2004;43:5S–12S.
6. Klima UP, Guerrero JL, Vlahakes GJ. Myocardial perfusion and right ventricular function: Ann Thorac Cardiovasc Surg. 1999;5:74–80.
7. Verzi MP, McCulley DJ, De Val S, Dodou E, Black BL: The right ventricle, outflow tract, and ventricular septum comprise a restricted expression domain within the secondary/anterior heart field. Dev Biol. 2005; 287:134 –145.
8. Zaffran S, Kelly RG, Meilhac SM, Buckingham ME, Brown NA: Right ventricular myocardium derives from the anterior heart field. Circ Res. 2004; 95:261–268.
9. Thomas T, Yamagishi H, Overbeek PA, Olson EN, Srivastava D: The bHLH factors, dHAND and eHAND, specify pulmonary and systemic cardiac ventricles independent of left-right sidedness. Dev Biol. 1998; 196:228 –236.
10. McFadden DG, Barbosa AC, Richardson JA, Schneider MD, Srivastava D, Olson EN: The Hand1 and Hand2 transcription factors regulate expansion of the embryonic cardiac ventricles in a gene dosagedependent manner. Development. 2005;132:189 –201.
11. Phan D, Rasmussen TL, Nakagawa O, McAnally J, Gottlieb PD, Tucker PW, Richardson JA, Bassel-Duby R, Olson EN: BOP, a regulator of right ventricular heart development, is a direct transcriptional target of MEF2C in the developing heart. Development. 2005;132:2669 –2678.
12. Zeisberg EM, Ma Q, Juraszek AL, Moses K, Schwartz RJ, Izumo S, Pu WT: Morphogenesis of the right ventricle requires myocardial expression of Gata4. J Clin Invest. 2005;115:1522–1531.
13. Molkentin JD, Kalvakolanu DV, Markham BE: Transcription factor GATA-4 regulates cardiac muscle-specific expression of the alphamyosin heavy-chain gene. Mol Cell Biol. 2004;14:4947– 4957.
14. Small EM, Krieg PA: Transgenic analysis of the atrial natriuretic factor (ANF) promoter: Nkx2–5 and GATA-4 binding sites are required for atrial specific expression of ANF. Dev Biol. 2003;261:116 –131
15. Semenza GL. Regulation of mammalian O2 homeostasis by hypoxiainducible factor 1: Ann Rev Cell Develop Biol. 1999;15:551–578.
16. Iyer NV, Kotch LE, Agani F, Leung SW, Laughner E, Wenger RH, Gassmann M, Gearhart JD, Lawler AM, Yu AY, Semenza GL. Cellular and developmental control of O2 homeostasis by hypoxia-inducible factor 1alpha: Genes Dev. 1998;12:149 –162.
17. Elson DA, Thurston G, Huang LE, Ginzinger DG, McDonald DM, Johnson RS, Arbeit JM: Induction of hypervascularity without leakage or inflammation in transgenic mice overexpressing hypoxia-inducible factor-1{alpha}. Genes Dev. 2001;15:2520 –2532.
18. Shyu K-G, Wang M-T, Wang B-W, Chang C-C, Leu J-G, Kuan P, Chang H: Intramyocardial injection of naked DNA encoding HIF-1[alpha]/VP16 hybrid to enhance angiogenesis in an acute myocardial infarction model in the rat. Cardiovasc Res. 2002;54:576 –583.
19. Sushma Reddy, Juan Carlos Osorio, Ana M. Duque, Beth D. Kaufman, et al.: Failure of Right Ventricular Adaptation in Children With Tetralogy of Fallot. Circ. 2006;114;I-37-I-42
20. Lowes BD, Minobe W, Abraham WT, Rizeq MN, Bohlmeyer TJ, Quaife RA, Roden RL, Dutcher DL, Robertson AD, Voelkel NF, Badesch DB, Groves BM, Gilbert EM, Bristow MR: Changes in gene expression in the intact human heart: downregulation of alpha-myosin heavy chain in hypertrophied, failing ventricular myocardium. J Clin Invest. 1997;100: 2315–2324.
21. Sack, Peter Schirmacher, Siegfried Hagl and Philipp A. Schnabel Achim Koch, Cornelius Geil-Bierschenk, Ralf Rieker, Thomas J. Dengler, Falk-Udo: Morphometric changes of the right ventricle in the first two weeks after clinical heart transplantation: analysis of myocardial biopsies from patients with complicated versus uncomplicated course. Eur J Cardiothorac Surg 2006;30:370-378
22. SW Kendall, HB Bittner, DS Peterseim, KA Campbell and P Van Trigt: Right ventricular function in the donor heart. Eur J Cardiothorac Surg 1997;11:609-615
23. Kiely DG, Cargill RI, Lipworth BJ.: Angiotensin II receptor blockade and effects on pulmonary hemodynamics and hypoxic pulmonary vasoconstriction in humans. Chest. 1996;110:698 –703.
24. Mulder P, Richard V, Derumeaux G, Hogie M, Henry JP, Lallemand F, Compagnon P, Mace B, Comoy E, Letac B, Thuillez C.:Role of endogenous endothelin in chronic heart failure: effect of long-term treatment with an endothelin antagonist on survival, hemodynamics, and cardiac
remodeling. Circulation. 1997;96:1976 –1982.
25. Nagaya N, Nishikimi T, Uematsu M, Satoh T, Kyotani S, Sakamaki F, Kakishita M, Fukushima K, Okano Y, Nakanishi N, Miyatake K, Kangawa K.: Plasma brain natriuretic peptide as a prognostic indicator in patients with primary pulmonary hypertension. Circ.. 2000;102:865–870.
26. J.G.Coghlan1, and J. Davar: How should we assess right ventricular function in 2008?
European Heart J Supplements 2007, 9 Sup. H), H22–H28
27. Sitbon O, Humbert M, Jais X, Ioos V, Hamid AM, Provencher S, Garcia G, Parent F, Herve P, Simonneau G.: Long-term response to calcium channel blockers in idiopathic pulmonary arterial hypertension. Circ. 2005;111:3105–3111.
28. Quaife RA, Chen MY, Lynch D, Badesch DB, Groves BM, Wolfel E, Robertson AD, Bristow MR, Voelkel NF.: Importance of right ventricular end-systolic regional wall stress in idiopathic pulmonary arterial hypertension: a new method for estimation of right ventricular wall
stress. Eur J Med Res 2006;11:214–220.
29. Yeo TC, Dujardin KS, Tei C, Mahoney DW, McGoon MD, Seward JB.: Value of a Doppler derived index combining systolic and diastolic time intervals in predicting outcome in primary pulmonary hypertension. Am J Cardiol 1998;81:1157–1161.
30. Meluzı´n J, Spinarova´ L, Bakala J, Toman J, Krejcı´ J, Hude P, Ka´ra T, Soucek M. Pulsed: Doppler tissue imaging of the velocity of tricuspid annular systolic motion; a new rapid, and non invasive method of evaluating right ventricular systolic function. Eur Heart J 2001;22:340–348
31. Gregory D. Lewis, Ravi V. Shah, Paul P. Pappagianopolas, David M. Systrom and Marc J. Semigran: Determinants of ventilatory efficiency in heart failure: the role of right
ventricular performance and pulmonary vascular tone. Circ Heart Fail 2008;1;227-233
32. Emma J. Birks, Virginia J. Owen, Paul B.J. Burton, Anne E. Bishop, Nicholas R. Banner, Asghar Khaghani, Julia M. Polak, Magdi H. Yacoub: Tumor necrosis factor-a is expressed in donor heart and predicts right ventricular failure after human heart transplantation. Circ. 2000;102:326-331.
33. Raffaele De Simone, Ivo Wolf, Sibylle Mottl-Link, Bernd W. Böttiger, Helmuth Rauch, Hans-Peter Meinzer and Siegfried Hagl: Intraoperative assessment of right ventricular volume and function. Eur J Cardiothorac Surg 2005;27:988-993
34. Sandoval J, Gaspar J, Pulido T, Bautista E, Martinez-Guerra ML, Zeballos M, Palomar A, Gomez A. Graded balloon dilation atrial septostomy in severe primary pulmonary hypertension: a therapeutic alternative for patients nonresponsive to vasodilator treatment. J Am Coll
Cardiol. 1998;32:297–304.
35. Masami Takagaki, Kozo Ishino, Masaaki Kawada, Shin-ichi Ohtsuki, Masan Hirota, Takeo Tedoriya, Yasuharu Tanabe, Mikizo Nakai and Shunji Sano: Total right ventricular exclusion improves left ventricular function in patients with end-stage congestive right ventricular failure.
Circ. 2003;108;II-226-II-229
36. Alessandro Frigiola, Alessandro Giamberti, Massimo Chessa, Marisa Di Donato, Raul Abella, Sara Foresti, Concettina Carlucci, Diana Negura, Mario Carminati, Gerald Buckberg, Lorenzo Menicanti and the RESTORE group: Right ventricular restoration during pulmonary valve implantation in adults with congenital heart disease. Eur J Cardiothorac Surg 2006;29:279-285
37. Mettauer B, Lampert E, Charloux A, Zhao QM, Epailly E, Oswald M, Frans A, Piquard F, Lonsdorfer J: Lung membrane diffusing capacity, heart failure, and heart transplantation. Am J Cardiol. 1999;83:62– 67
38. Badesch DB, Abman SH, Ahearn GS, Barst RJ, McCrory DC, Simonneau G, McLaughlin VV. Medical therapy for pulmonary arterial hypertension: ACCP evidence-based clinical practice guidelines. Chest. 2004;126:35S–62S.
39. Gavazzi A, Ghio S, Scelsi L, Campana C, Klersy C, Serio A, Raineri C, Tavazzi L. Response of the right ventricle to acute pulmonary vasodilation predicts the outcome in patients with advanced heart failure and pulmonary hypertension. Am Heart J. 2003;145:310 –316.
40. Kisch-Wedel H, Kemming G, Meisner F, Flondor M, Kuebler WM, Bruhn S, Koehler C, Zwissler B: The prostaglandins epoprostenol and iloprost increase left ventricular contractility in vivo. Intensive Care Med. 2003;29:1574 –1583.
41. Montalescot G, Drobinski G, Meurin P, Maclouf J, Sotirov I, Philippe F, Choussat R, Morin E, Thomas D: Effects of prostacyclin on the pulmonary vascular tone and cardiac contractility of patients with pulmonary hypertension secondary to end-stage heart failure. Am J Cardiol. 1998;
82:749 –755.
42. Galie N, Hinderliter AL, Torbicki A, Fourme T, Simonneau G, Pulido T, Espinola-Zavaleta N, Rocchi G, Manes A, Frantz R, Kurzyna M, Nagueh SF, Barst R, Channick R, Dujardin K, Kronenberg A, Leconte I, Rainisio M, Rubin L: Effects of the oral endothelin-receptor antagonist bosentan on echocardiographic and Doppler measures in patients with pulmonary
arterial hypertension. J Am Coll Cardiol. 2003;41:1380 –1386.
43. Kaul TK, Fields BL.: Postoperative acute refractory right ventricular failure: incidence, pathogenesis, management and prognosis. Cardiovasc. Surg. 2000;8:1–9.
44. Dennis R. Trumble, Chong S. Park, James A. Magovern: Copulsation balloon for right ventricular assistance. Preliminary trials. Circ. 1999;99;2815-2818
45. McLaughlin VV, Rich S: Pulmonary hypertension. Curr Probl Cardiol. 2004;29:575– 634.
46. Mendeloff EN, Meyers BF, Sundt TM, Guthrie TJ, Sweet SC, de la Morena M, Shapiro S, Balzer DT, Trulock EP, Lynch JP, Pasque MK, Cooper JD, Huddleston CB, Patterson GA.: Lung transplantation for pulmonary vascular disease. Ann Thorac Surg. 2002;73:209 –217.


